Ngâm một lá đồng vào dd AgNO3 . Sau phản ứng khối lượng lá đồng tăng 0,76g. Tính số gam đồng tham gia vào phản ứng

Những câu hỏi liên quan
Nhúng một miếng đồng vào dung dịch chứa 100 ml AgNO3 0,3M. Sau một thời gian lấy miếng đồng ra thấy khối lượng tăng lên 1,52 gam. Vậy nồng độ của AgNO3 sau phản ứng là: A. 0,1M B. 0,2M C. 0,5M D. 0,04M
Đọc tiếp
Nhúng một miếng đồng vào dung dịch chứa 100 ml AgNO3 0,3M. Sau một thời gian lấy miếng đồng ra thấy khối lượng tăng lên 1,52 gam. Vậy nồng độ của AgNO3 sau phản ứng là:
A. 0,1M
B. 0,2M
C. 0,5M
D. 0,04M
Đáp án A
Số mol AgNO3 = 0,03 (mol)
Phương trình phản ứng:

Ta có: 108.2a - 64a = 152a = 1,52 → a = 0,01 (mol)
Số mol AgNO3 còn lại = 0,03 -2.a = 0,03 - 2.0,01 = 0,01 mol
Nồng độ AgNO3 = 0,01/0,1 = 0,1M
Đúng 0
Bình luận (0)
1 . Ngâm một lá đồng vào dd AgNO3 . Sau phản ứng khối lượng lá đồng tăng 0,76g. Tính số gam đồng tham gia vào phản ứng
2. Ngâm đinh sắt vào để CuSO4, sau một thời gian lấy ra rửa sạch, sấy khô,cân nặng hơn lúc đầu 0,4g
a) tính khối lượng sắt và CuSO4 đã tham gia phản ứng?
b)nếu khối lượng dd CuSO4 đã dùng ở trên là 210g có khối lượng riêng là 1,05g/ml. Xác định nồng độ mol ban đầu của dd CuSO4
Đọc tiếp
1 . Ngâm một lá đồng vào dd AgNO3 . Sau phản ứng khối lượng lá đồng tăng 0,76g. Tính số gam đồng tham gia vào phản ứng
2. Ngâm đinh sắt vào để CuSO4, sau một thời gian lấy ra rửa sạch, sấy khô,cân nặng hơn lúc đầu 0,4g
a) tính khối lượng sắt và CuSO4 đã tham gia phản ứng?
b)nếu khối lượng dd CuSO4 đã dùng ở trên là 210g có khối lượng riêng là 1,05g/ml. Xác định nồng độ mol ban đầu của dd CuSO4
Ngâm một lá Zn trong dung dịch có hòa tan 8,32 gam CdSO4. Phản ứng xong thấy khối lượng là Zn tăng 2,35%. Vậy khối lượng của là Zn trước khi tham gia phản ứng là bao nhiêu?
cho 5gam hỗn hợp bột bạc và đồng vào dung dịch AgNo3 dư , phản ứng hoàn toàn , thu 8,8 gam chất rắn . Tính thành phần trăm về khối lượng của đồng trong hỗn hợp ban đầu ?
Ag + AgNO3 (không phản ứng)
Cu + 2AgNO3 -> 2Ag +Cu(NO3)2
0.04 0.08
n(Ag)=8.8/108=0.08 mol
m(Cu)=0.04*64=2.56(g)
%m(Cu)=(2.56*100)/5=51.2%
Đúng 0
Bình luận (0)
Ngâm một vật bằng đồng có khối lượng 10 gam trong 250 gam dung dịch AgNO3 4%. Khi lấy vật ra thì lượng AgNO3 trong dung dịch giảm 17%. Vậy khối lượng của vật sau phản ứng là:
A. 10,5g
B. 10,76g
C. 11,2g
D. 12,8g
Đáp án B
Khối lượng AgNO3 = 250.4/100 = 10 (g)
Khối lượng AgNO3 trong dung dịch giảm 17% = khối lượng AgNO3 phản ứng = 1,7 (g)
⇒ Số mol AgNO3 = 0,01 mol
Phương trình phản ứng:
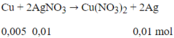
Khối lượng vật bằng Cu = 10 - 0,005.64 + 0,01.108 = 10,76 (g)
Đúng 0
Bình luận (0)
Ngâm một vật bằng đồng có khối lượng 10 gam trong 250 gam dung dịch AgNO3 4%. Khi lấy vật ra thì lượng AgNO3 trong dung dịch giảm 17%. Vậy khối lượng của vật sau phản ứng là:
A. 10,5g
B. 10,76g
C. 11,2g
D. 12,8g
Đáp án B
Khối lượng AgNO3 = 250.4/100 = 10 (g)
Khối lượng AgNO3 trong dung dịch giảm 17% = khối lượng AgNO3 phản ứng = 1,7 (g)
⇒Số mol AgNO3 = 0,01 mol
Phương trình phản ứng:
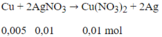
Khối lượng vật bằng Cu = 10 - 0,005.64 + 0,01.108 = 10,76 (g)
Đúng 0
Bình luận (0)
khi hòa tan 6g hỗn hợp các kim loại gồm đồng ,sắt,nhôm trong axit clohidric dư thì tạo thành 3,024l hidro (đktc) và còn lại 1,86g kim loại không tan .Biết đồng không tham gia phản ứnga) viết pt phản ứngb)xác định thành phần % khối lượng mỗi kim loại trong hỗn hợpc) tính khối lượng axit đã tham gia phản ứng và khối lượng của các muối clorua tạo thành
Đọc tiếp
khi hòa tan 6g hỗn hợp các kim loại gồm đồng ,sắt,nhôm trong axit clohidric dư thì tạo thành 3,024l hidro (đktc) và còn lại 1,86g kim loại không tan .Biết đồng không tham gia phản ứng
a) viết pt phản ứng
b)xác định thành phần % khối lượng mỗi kim loại trong hỗn hợp
c) tính khối lượng axit đã tham gia phản ứng và khối lượng của các muối clorua tạo thành
số mol của HCl là 2x và 3y sao bạn ko nhân cho 2 và 3
Đúng 0
Bình luận (0)
Ngâm 1 lá Cu trong 20ml dd AgNO3 phản ứng xong lấy lá Cu ra rửa nhẹ làm khô khối lượng lá Cu tăng thêm 1.52g
a) Tính CM AgNO3
b) Tính C% của dung dịch thu được sau phản ứng biết khối lượng riêng bằng 1.1g/ml và thể tích dung dịch sau phản ứng thay đổi không đáng kể
Cu+ 2AgNO3 -----> Cu(NO3)2+ 2Ag
a.......2a.........................a...............2a
a)Gọi a là số mol Cu p/ ư
Ta có ▲mtăng=mAg-mCu=108*2a-64a=1.52 g
<=>152a=1.52=>a=0.01 mol
=>CmANO3=2a/0.02=0.02/0.02=1M
b) Ta có mdd CuNO3=D*V=20*1.1=22 g
mCuNO3=126*a=126*0.01=1.26 g
=>C%CUNO3=1.26*100/22=5.72%
Đúng 0
Bình luận (1)
cho 1 lá Zn vào 42,5 gam dd AgNO3 x%. Khi phản ứng hết khối lượng Zn tăng 1,51 giá trị x=?
A.8
B.4
C.16
D.10
Gọi a là số mol của Zn phản ứng
Zn (a) + 2AgNO3 (2a) -----> Zn(NO3)2 + 2Ag (2a)
=> nAg(tạo) = 2a (mol)
mZn (pư) = 65a (gam)
mAg (tạo) = 216a (gam)
=> 216a - 65a =1,51
=> a = 0,01 (mol)
- Theo pthh: nAgNO3 = 2a = 0,02 (mol)
=> mAgNO3 = 170.0,02 = 3,4 gam
=> C%AgNO3 = (3,4.100)/42,5 = 8%
=> x = 8
Chọn A
Đúng 0
Bình luận (0)















