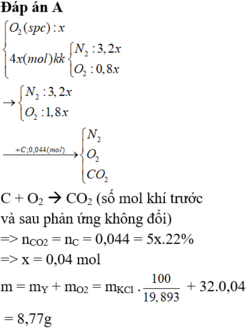nung KMnO4→K2MnO4+MnO2+O2.toàn bộ lượng O2 thu được đủ để đốt cháy biêst 1 lượng khí CH4→8,96l khí CO2+H2O.Tính khối lượng KMnO4=? biết hiệu suất của quá trình là 90%

Những câu hỏi liên quan
nung KMnO4→K2MnO4+MnO2+O2.toàn bộ lượng O2 thu được đủ để đốt cháy biêst 1 lượng khí CH4→8,96l khí CO2+H2O.Tính khối lượng KMnO4=? biết hiệu suất của quá trình là 90%
\(n_{CO_2}=\dfrac{8,96}{22,4}=0,4mol\)
Đốt cháy \(CH_4\):
\(CH_4+\dfrac{3}{2}O_2\rightarrow CO_2+2H_2O\)
0,6 \(\leftarrow\) 0,4
\(2KMnO_4\rightarrow K_2MnO_4+MnO_2+O_2\)
1,2 \(\leftarrow\) 0,6
Hiệu suất quá trình 90%\(\Rightarrow n_{KMnO_4}=1,2\cdot90\%=1,08mol\)
\(m_{KMnO_4}=1,08\cdot158=170,64g\)
Đúng 1
Bình luận (0)
Nhiệt phân hoàn toàn 31,6 g KMnO4 thu được K2MnO4, MnO2 và khí oxygen O2.
a) Viết phương trình hóa học và tính khối lượng K2MnO4 thu được.
b) Tính thể tích khí O2 thu được (ở đkc).
c) Dùng toàn bộ khí O2 ở trên tác dụng với khí methane CH4 thu được khí carbon dioxide và nước. Tính thể tích khí CO2 thu được (ở đkc) và khối lượng H2O thu được.
a, PT: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
Ta có: \(n_{KMnO_4}=\dfrac{31,6}{158}=0,2\left(mol\right)\)
Theo PT: \(n_{K_2MnO_4}=\dfrac{1}{2}n_{KMnO_4}=0,1\left(mol\right)\)
\(\Rightarrow m_{K_2MnO_4}=0,1.197=19,7\left(g\right)\)
b, Theo PT: \(n_{O_2}=\dfrac{1}{2}n_{KMnO_4}=0,1\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,1.24,79=2,479\left(l\right)\)
c, PT: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
Theo PT: \(\left\{{}\begin{matrix}n_{CO_2}=\dfrac{1}{2}n_{O_2}=0,05\left(mol\right)\\n_{H_2O}=n_{O_2}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow V_{CO_2}=0,05.24,79=1,2395\left(l\right)\)
\(m_{H_2O}=0,1.18=1,8\left(g\right)\)
Đúng 2
Bình luận (1)
Nung m gam hỗn hợp A gồm KMnO4 và KClO3 ta thu được chất rắn B và khí O2. Biết KClO3 bị phân hủy hoàn toàn theo phản ứng KClO3 →KCl + O2; còn KMnO4 bị phân hủy 1 phần theo phản ứng KMnO4 →K2MnO4 + MnO2 + O2. Trong B có 0,894 gam KCl chiếm 8,127% khối lượng, khí O2 thu được vừa đủ đốt cháy hết 1,728 gam nhôm. Khối lượng của K2MnO4 trong B bằng?
ĐỀ DÀI THẾ??????????
Nung m gam hỗn hợp X gồm KClO3 và KMnO4, thu được chất rắn Y (KCl, K2MnO4, MnO2, KMnO4) và O2. Trong Y có 1,49 gam KCl chiếm 19,893% theo khối lượng. Trộn lượng O2 ở trên với không khí theo tỉ lệ thể tích tương ứng là 1:4 thu được hỗn hợp khí Z. Đốt cháy hết 0,528 gam cacbon bằng hỗn hợp Z thu được hỗn hợp khí T gồm 3 khí O2, N2, CO2, trong đó CO2 chiếm 22% về thể tích. Biết trong không khí có 80% N2 và 20% O2 theo thể tích. Giá trị của m là: A. 8,77. B. 8,53. C. 8,70. D. 8,91.
Đọc tiếp
Nung m gam hỗn hợp X gồm KClO3 và KMnO4, thu được chất rắn Y (KCl, K2MnO4, MnO2, KMnO4) và O2. Trong Y có 1,49 gam KCl chiếm 19,893% theo khối lượng. Trộn lượng O2 ở trên với không khí theo tỉ lệ thể tích tương ứng là 1:4 thu được hỗn hợp khí Z. Đốt cháy hết 0,528 gam cacbon bằng hỗn hợp Z thu được hỗn hợp khí T gồm 3 khí O2, N2, CO2, trong đó CO2 chiếm 22% về thể tích. Biết trong không khí có 80% N2 và 20% O2 theo thể tích. Giá trị của m là:
A. 8,77.
B. 8,53.
C. 8,70.
D. 8,91.
Nung m gam hỗn hợp X gồm KClO3 và KMnO4 thu được chất rắn Y (KCl, K2MnO4, MnO2, KMnO4) và O2. Trong Y có 1,49 gam KCl chiếm 19,893% theo khối lượng. Trộn lượng O2 ở trên với không khí theo tỉ lệ thể tích tương ứng là 1:4 thu được hỗn hợp khí Z. Đốt cháy hết 0,528 gam cacbon bằng hỗn hợp Z thu được hỗn hợp khí T gồm 3 khí O2, N2, CO2, trong đó CO2 chiếm 22% về thể tích. Biết trong không khí có 80% N2 và 20% O2 theo thể tích. Giá trị của m là A. 8,70. B. 8,77. C. 8,91. D. 8,53.
Đọc tiếp
Nung m gam hỗn hợp X gồm KClO3 và KMnO4 thu được chất rắn Y (KCl, K2MnO4, MnO2, KMnO4) và O2. Trong Y có 1,49 gam KCl chiếm 19,893% theo khối lượng. Trộn lượng O2 ở trên với không khí theo tỉ lệ thể tích tương ứng là 1:4 thu được hỗn hợp khí Z. Đốt cháy hết 0,528 gam cacbon bằng hỗn hợp Z thu được hỗn hợp khí T gồm 3 khí O2, N2, CO2, trong đó CO2 chiếm 22% về thể tích. Biết trong không khí có 80% N2 và 20% O2 theo thể tích. Giá trị của m là
A. 8,70.
B. 8,77.
C. 8,91.
D. 8,53.
Nung m gam hỗn hợp X gồm KClO3 và KMnO4 thu được chất rắn Y (KCl, K2MnO4, MnO2, KMnO4) và O2. Trong Y có 1,49 gam KCl chiếm 19,893% theo khối lượng. Trộn lượng O2 ở trên với không khí theo tỉ lệ thể tích tương ứng là 1:4 thu được hỗn hợp khí Z. Đốt cháy hết 0,528 gam cacbon bằng hỗn hợp Z thu được hỗn hợp khí T gồm 3 khí O2, N2, CO2, trong đó CO2 chiếm 22% về thể tích. Biết trong không khí có 80% N2 và 20% O2 theo thể tích. Giá trị của m là A. 8,77 B. 8,53 C. 8,70 D. 8,91
Đọc tiếp
Nung m gam hỗn hợp X gồm KClO3 và KMnO4 thu được chất rắn Y (KCl, K2MnO4, MnO2, KMnO4) và O2. Trong Y có 1,49 gam KCl chiếm 19,893% theo khối lượng. Trộn lượng O2 ở trên với không khí theo tỉ lệ thể tích tương ứng là 1:4 thu được hỗn hợp khí Z. Đốt cháy hết 0,528 gam cacbon bằng hỗn hợp Z thu được hỗn hợp khí T gồm 3 khí O2, N2, CO2, trong đó CO2 chiếm 22% về thể tích. Biết trong không khí có 80% N2 và 20% O2 theo thể tích. Giá trị của m là
A. 8,77
B. 8,53
C. 8,70
D. 8,91
Nung m gam hỗn hợp X gồm KClO3 và KMnO4 thu được chất rắn Y (KCl, K2MnO4, MnO2, KMnO4) và O2. Trong Y có 1,49 gam KCl chiếm 19,893% theo khối lượng. Trộn lượng O2 ở trên với không khí theo tỉ lệ thể tích tương ứng là 1:4 thu được hỗn hợp khí Z. Đốt cháy hết 0,528 gam cacbon bằng hỗn hợp Z thu được hỗn hợp khí T gồm 3 khí O2, N2, CO2, trong đó CO2 chiếm 22% về thể tích. Biết trong không khí có 80% N2 và 20% O2 theo thể tích. Giá trị của m là A. 8,77. B. 8,53. ...
Đọc tiếp
Nung m gam hỗn hợp X gồm KClO3 và KMnO4 thu được chất rắn Y (KCl, K2MnO4, MnO2, KMnO4) và O2. Trong Y có 1,49 gam KCl chiếm 19,893% theo khối lượng. Trộn lượng O2 ở trên với không khí theo tỉ lệ thể tích tương ứng là 1:4 thu được hỗn hợp khí Z. Đốt cháy hết 0,528 gam cacbon bằng hỗn hợp Z thu được hỗn hợp khí T gồm 3 khí O2, N2, CO2, trong đó CO2 chiếm 22% về thể tích. Biết trong không khí có 80% N2 và 20% O2 theo thể tích. Giá trị của m là
A. 8,77.
B. 8,53.
C. 8,91.
D. 8,70.
Đáp án : A
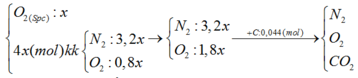
C + O2 à CO2 ( số mol khí trước và sau phản ứng không đổi)
=> nCO2 = nC = 0,044 = 5x.22% => x = 0,04 mol
m = mY + mO2 = mKCl. 100 19 , 893 + 32.0,04 = 8,77g
Đúng 0
Bình luận (0)
người ta điều chế khí Oxi bằng cách nhiệt phân 94,8 KMnO4 : KMnO4 đốt cháy K2MnO4 + MnO2 + O2
a) tính thể tích Oxi thu đc ( đktc)
b) lượng khí Oxi trên đó đủ đốt cháy hết 12,8g bột S không?
Xem chi tiết
\(n_{KMnO_4}=\dfrac{94.8}{158}=0.6\left(mol\right)\)
\(2KMnO_4\underrightarrow{t^0}K_2MnO_4+MnO_2+O_2\)
\(0.6................................................0.3\)
\(V_{O_2}=0.3\cdot22.4=6.72\left(l\right)\)
\(n_S=\dfrac{12.8}{32}=0.4\left(mol\right)\)
\(S+O_2\underrightarrow{t^0}SO_2\)
\(0.3....0.3\)
\(n_{S\left(dư\right)}=0.4-0.3=0.1\left(mol\right)\)
Vậy: lượng S vẫn còn dư sau phản ứng
Đúng 1
Bình luận (0)
Nhiệt phân hoàn toàn KMnO4 để thu được khí O2 theo sơ đồ phản ứng sau:
KMnO4 ---> K2MnO4 + MnO2 + O2
Kết thúc phản ứng thu được 2,24 lít khí oxi (dktc). Tính khối lượng KMnO4 đã sử dụng.
\(PTHH:2KMnO_4\rightarrow K_2MnO_4+MnO_2+O_2\)
Ta có : \(n_{O2}=\dfrac{V}{22,4}=0,1\left(mol\right)\)
\(TheoPTHH:n_{KMnO4}=2n_{O2}=0,2\left(mol\right)\)
\(\Rightarrow m=n.M=31,6\left(g\right)\)
Đúng 2
Bình luận (0)