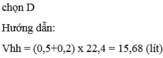có một hỗn hợp khí gồm: 0,25 mol khí O2, 0,1 mol khí N2, 0,45 khí CO2 ( biết các khí điều ở điều kiện tiêu chuẩn). hãy tính thể tích của hỗn hợp khí trên

Những câu hỏi liên quan
a. Thể tích của 0,8 mol khí NH3 (đktc) b. Thể tích ở đktc của 140 g khí Nitơ ; 96g khí Oxi c. Thể tích của hỗn hợp khí gồm 0,5 mol Cl2 và 0,2 mol N2 ở điều kiện tiêu chuẩn. d. Khối lượng của hỗn hợp 0,25 mol khí NH3 , 28lit khí CO.
\(a.V_{NH_3}=0,8.22,4=17,92\left(l\right)\\ b.n_{N_2}=\dfrac{140}{28}=5\left(mol\right)\\ V_{N_2}=112\left(l\right)\\ n_{O_2}=\dfrac{96}{32}=3\left(mol\right)\\ V_{O_2}=22,4.3=67,2\left(l\right)\)
\(c.n_{hh}=0,5+0,2=0,7\left(mol\right)\\ V_{hh}=0,7.22,4=15,68\left(l\right)\\ d.m_{NH_3}=4,25\left(g\right)\\ n_{CO}=\dfrac{28}{22,4}=1,25\left(mol\right)\\ m_{CO}=1,25.28=35\left(g\right)\\ m_{hh}=4,25+35=39,25\left(g\right)\)
Đúng 0
Bình luận (0)
a. Thể tích của 0,8 mol khí NH3 (đktc)
=>VNH3=0,8.22,4=17,92l
b. Thể tích ở đktc của 140 g khí Nitơ ; 96g khí Oxi
nN2=140\14.2=5 mol
nO2=96\32=3 mol
=>Vhh=(5+3).22,4=179,2l
c. Thể tích của hỗn hợp khí gồm 0,5 mol Cl2 và 0,2 mol N2 ở điều kiện tiêu chuẩn.
=>Vhh=(0,5+0,2).22,4=15,68l
d. Khối lượng của hỗn hợp 0,25 mol khí NH3 , 28lit khí CO.
n CO=28\22,4=1,25 mol
=>mhh=0,25.17+1,25.28=39,25g
Đúng 1
Bình luận (0)
Hãy tìm thể tích của những lượng khí sau ở điều kiện tiêu chuẩn :
a)0,4 mol phân tử CO2
b) Hỗn hợp khí gồm có : 0,25 mol N2 và 0,5 mol O2
c) 0,5 mol phân tử H2S
\(a,V_{CO_2}=0,4.22,4=8,96(l)\\ b,V_{hh}=22,4.(0,25+0,5)=16,8(l)\\ c,V_{H_2S}=0,5.22,4=11,2(l)\)
Đúng 1
Bình luận (0)
Thể tích hỗn hợp khí gồm 0,5 mol C O 2 và 0,2 mol O 2 ở điều kiện tiêu chuẩn là:
A. 11,2 lít
B. 22,4 lít
C. 4,48 lít
D. 15,68 lít
1 hỗn hợp khí X x 6,72 lít H2 ; 16,8 lít O2 ; 17,92 lít N2 ; 3,36 lít CO2 (điều kiện tiêu chuẩn)
a) Tính % số mol mỗi khí trong hỗn hợp
b) Tính % thể tích mỗi khí trong hỗn hợp
c) So sánh tỉ lệ số mol và tỉ lệ thể tích mỗi khí
Một hỗn hợp gồm 0,15 mol khí O2; 0,25 mol khí N2 và 6,4 g khí SO2. a. Tính thể tích của hỗn hợp khí đó ở đktc. b. Tính khối lượng của hỗn hợp khí trên.
Cho hỗn hợp khí ở điều kiện tiêu chuẩn gồm: 11,2 lít khí CO2 và 0,6.1023 phân tử khí SO2
a/Tính số mol của các khí có trong hỗn hợp.
b/Tính khối lượng hỗn hợp.
1.tính số mol có trong 6,72 lít khí oxi ở điều kiện tiêu chuẩn?
2.tính thể tích của hỗn hợp khí gồm 4,4 gam CO2 và 3,2 gam O2?
1. \(n_{O_2}=\frac{V}{22,4}=\frac{6,72}{22,4}=0,3\left(mol\right)\)
2.
\(n_{CO_2}=\frac{m}{M}=\frac{4,4}{44}=0,1\left(mol\right)\)
\(n_{O_2}=\frac{m}{M}=\frac{3,2}{32}=0,1\left(mol\right)\)
\(V_{HC}=n.22,4=\left(0,1+0,1\right).22,4=4,48\left(l\right)\)
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Hãy tìm thể tích của những lượng khí sau ở đktc: Hỗn hợp khí gồm có: 0,75 mol C O 2 ; 0,25 mol N 2 ; và 0,5 mol O 2 .
V h h = 22,4 n O 2 + n H 2 + n O 2 = 22,4(0,75 + 0,25 + 0,5) = 33,6(l)
Đúng 0
Bình luận (0)
Biết X là axit cacboxylic đơn chức, Y là ancol no, cả hai chất đều mạch hở, có cùng số nguyên tử cacbon. Đốt cháy hoàn toàn 0,4 mol hỗn hợp gồm X và Y (trong đó số mol của X lớn hơn số mol của Y) cần vừa đủ 30,24 lít khí O2, thu được 26,88 lít khí CO2 và 19,8 gam H2O. Biết thể tích các khí đo ở điều kiện tiêu chuẩn. Khối lượng của Y trong 0,4 mol hỗn hợp trên là A. 11,4 gam. B. 19,0 gam. C. 9,0 gam. D. 17,7 gam.
Đọc tiếp
Biết X là axit cacboxylic đơn chức, Y là ancol no, cả hai chất đều mạch hở, có cùng số nguyên tử cacbon. Đốt cháy hoàn toàn 0,4 mol hỗn hợp gồm X và Y (trong đó số mol của X lớn hơn số mol của Y) cần vừa đủ 30,24 lít khí O2, thu được 26,88 lít khí CO2 và 19,8 gam H2O. Biết thể tích các khí đo ở điều kiện tiêu chuẩn. Khối lượng của Y trong 0,4 mol hỗn hợp trên là
A. 11,4 gam.
B. 19,0 gam.
C. 9,0 gam.
D. 17,7 gam.