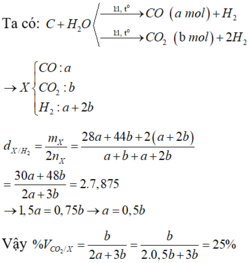Hỗn hợp khí X gồm CO2 và CO có tỉ khối so với khí H2 bằng 20,67. Phần trăm thể
tích của CO trong X là

Những câu hỏi liên quan
Cho hơi nước đi qua than nóng đỏ, thu được V lít (đktc) hỗn hợp khí X gồm CO2, CO và H2, có tỉ khối so với H2 là 7,875. Phần trăm thể tích của CO2 trong hỗn hợp X là A. 12,5%. B. 37,5%. C. 25,0%. D. 50,0%.
Đọc tiếp
Cho hơi nước đi qua than nóng đỏ, thu được V lít (đktc) hỗn hợp khí X gồm CO2, CO và H2, có tỉ khối so với H2 là 7,875. Phần trăm thể tích của CO2 trong hỗn hợp X là
A. 12,5%.
B. 37,5%.
C. 25,0%.
D. 50,0%.
cho hỗn hợp khí X gồm CO, CO2, SO2 có tỉ khối so với H2 là 20,5. Biết số mol của So2 và số mol của CO2 trong hỗn hợp bằng nhau . Tính thàn phần % theo thể tích của CO và CO2 là
a) 50% và 25%
b) 50% và 30%
c) 25% và 25%
Hỗn hợp khí A gồm có
O
2
và
O
3
tỉ khối của hỗn hợp khí A đối với khí
H
2
là 19,2. Hỗn hợp khí B gồm có
H
2
và khí CO, tỉ khối của hỗn hợp khí B đối với
H
2...
Đọc tiếp
Hỗn hợp khí A gồm có O 2 và O 3 tỉ khối của hỗn hợp khí A đối với khí H 2 là 19,2. Hỗn hợp khí B gồm có H 2 và khí CO, tỉ khối của hỗn hợp khí B đối với H 2 là 3,6.
Tính thành phần phần trăm theo thể tích của mỗi khí có trong hỗn hợp khí A và B.
Đặt x và y là số mol O 3 và O 2 có trong 1 mol hỗn hợp khí
Hỗn hợp khí A : (48x + 32y)/(x+y) = 19,2 x 2 = 38,4
→ 3x = 2y → 40% O 3 và 60% O 2
Đặt x và y là số mol H 2 và CO có trong 1 mol hỗn hợp khí
Hỗn hợp khí B : (2x + 28y)/(x+y) = 3,6 x 2 = 7,2
→ x = 4y → 80% H 2 và 20% CO
Đúng 0
Bình luận (1)
hỗn hợp X gồm CO và CO2 có tỉ khối hơi so với H2 bằng 16. phần trăm thể tích CO,CO2 lần lượt là
\(\dfrac{28n_{CO}+44n_{CO_2}}{n_{CO}+n_{CO_2}}=32\)
\(\Leftrightarrow28n_{CO}+44n_{CO_2}=32n_{CO}+32n_{CO_2}\)
\(\Leftrightarrow4n_{CO}-12n_{CO_2}=0\)
\(\Leftrightarrow n_{CO}=3n_{CO_2}\)
\(\Rightarrow\%V_{CO}=\dfrac{n_{CO}}{n_{CO}+n_{CO_2}}.100\%=\dfrac{3n_{CO_2}}{4n_{CO_2}}.100\%=75\%\)
\(\Rightarrow\%V_{CO_2}=25\%\)
Đúng 1
Bình luận (0)
1 Cho hỗn hợp khí Z gồm CO và H2 có tỉ khối so với khí hidro là 7,5 . Cần thêm bao nhiêu lít khí H2 vào 50 lít hỗn hợp Z để cho tỉ khối giảm đi 2 lần2 Hỗn hợp khí X gồm O2 và Co2 X có tỉ khối so với khí SO2 là 0,725 . Tính khối lượng từng khí có trong 11,2 lít hỗn hợp X (dktc)3 Đốt cháy 6,72 lít CO ở Dktc Khi phản ứng kết thúc thu được hỗn hợp khí X có tỉ khối so với hidro là 20 . Tính % theo V và khối lượng mỗi khí trong X
Đọc tiếp
1 Cho hỗn hợp khí Z gồm CO và H2 có tỉ khối so với khí hidro là 7,5 . Cần thêm bao nhiêu lít khí H2 vào 50 lít hỗn hợp Z để cho tỉ khối giảm đi 2 lần
2 Hỗn hợp khí X gồm O2 và Co2 X có tỉ khối so với khí SO2 là 0,725 . Tính khối lượng từng khí có trong 11,2 lít hỗn hợp X (dktc)
3 Đốt cháy 6,72 lít CO ở Dktc Khi phản ứng kết thúc thu được hỗn hợp khí X có tỉ khối so với hidro là 20 . Tính % theo V và khối lượng mỗi khí trong X
Cho 0,2 mol hỗn hợp khí Y gồm CO và
H
2
(có tỉ khối so với
H
2
bằng 4,25) tác dụng với 20 gam hỗn hợp X gồm Fe,
F
e
C
O
3
,
F
e
2
O
3
sau một thời gian thu được hỗn hợp rắn
X
1
và hỗn hợp khí
Y...
Đọc tiếp
Cho 0,2 mol hỗn hợp khí Y gồm CO và H 2 (có tỉ khối so với H 2 bằng 4,25) tác dụng với 20 gam hỗn hợp X gồm Fe, F e C O 3 , F e 2 O 3 sau một thời gian thu được hỗn hợp rắn X 1 và hỗn hợp khí Y 1 . Cho Y 1 hấp thụ vào dung dịch dư, sau phản ứng thu được 7 gam kết tủa và thoát ra 0,06 mol hỗn hợp khí Y 2 (có tỉ khối so với H 2 bằng 7,5). Hòa tan X 1 bằng lượng dư dung dịch H N O 3 thu được dung dịch Z và 0,62 mol hỗn hợp hai khí trong đó có một khí màu nâu đỏ là sản phẩm khứ duy nhất của N + 5 Nếu cho 20 gam X tác dụng với dung dịch H 2 S O 4 (đặc, nóng, dư) thì thu được 0,225 mol hỗn hợp S O 2 và C O 2 Phần trăm khối lượng của F e 2 O 3 trong X là
A. 32%
B. 48%
C. 16%
D. 40%
Cho 0,2 mol hỗn hợp khí Y gồm CO và
H
2
(có tỉ khối so với
H
2
bằng 4,25) tác dụng với 20 gam hỗn hợp X gồm sau một thời gian thu được hỗn hợp rắn
X
1
và hỗn hợp khí
Y
1
. Cho
Y
1
hấp thụ vào dung dịch Ca...
Đọc tiếp
Cho 0,2 mol hỗn hợp khí Y gồm CO và
H
2
(có tỉ khối so với
H
2
bằng 4,25) tác dụng với 20 gam hỗn hợp X gồm ![]()
sau một thời gian thu được hỗn hợp rắn X 1 và hỗn hợp khí Y 1 . Cho Y 1 hấp thụ vào dung dịch Ca ( O H ) 2 dư, sau phản ứng thu được 7 gam kết tủa và thoát ra 0,06 mol hỗn hợp khí Y 2 (có tỉ khối so với H 2 bằng 7,5). Hòa tan X 1 bằng lượng dư dung dịch H N O 3 thu được dung dịch Z và 0,62 mol hỗn hợp hai khí trong đó có một khí màu nâu đỏ là sản phẩm khứ duy nhất của N + 5 Nếu cho 20 gam X tác dụng với dung dịch H 2 S O 4 (đặc, nóng, dư) thì thu được 0,225 mol hỗn hợp S O 2 và C O 2 Phần trăm khối lượng của F e 2 O 3 trong X là
A. 32%
B. 48%
C. 16%
D. 40%
Cho 5,6 lít hỗn hợp khí X gồm CO và CO2 (đktc). Biết X có tỉ khối so với H2 là 18,8. Tính số mol và % số mol mỗi khí trong hỗn hợp X.
Gọi $n_{CO} = a(mol) ; n_{CO_2} = b(mol)$
Ta có :
$n_X = a + b = 0,25(mol)$
$m_X = 28a + 44b = 18,8.2.0,25 = 9,4(gam)$
$\Rightarrow a = 0,1 ; b = 0,15
$\%n_{CO} = \dfrac{0,1}{0,25}.100\% = 40\%$
$\%n_{CO_2} = 100\% -40\% = 60\%$
Đúng 1
Bình luận (0)
hỗn hợp khí A gồm N2 và CO2 có tỉ khối so với khí Hiđro là 18. Tính thành phần phần trăm khối lượng của mỗi khí trong hợp chất .Cần thêm bao nhiêu gam CO2 vào 0,2 mol hỗn hợp A để tỉ khối của hỗn hợp B thu được có tỉ khối so với H2 là 20
Xem chi tiết
\(a.\)
\(GS:\)
\(n_{hh}=1\left(mol\right)\)
\(Đặt:n_{N_2}=a\left(mol\right),n_{CO_2}=b\left(mol\right)\)
\(\Rightarrow a+b=1\left(1\right)\)
\(m_A=28a+44b=18\cdot2=36\left(2\right)\)
\(\left(1\right),\left(2\right):\)
\(a=b=0.5\)
\(\%m_{N_2}=\dfrac{0.5\cdot28}{0.5\cdot28+0.5\cdot44}\cdot100\%=38.89\%\)
\(\%m_{CO_2}=61.11\%\)
\(b.\)
\(\dfrac{n_{N_2}}{n_{CO_2}}=\dfrac{0.5}{0.5}=\dfrac{1}{1}\)
\(n_{N_2}=n_{CO_2}=\dfrac{1}{2}\cdot n_A=\dfrac{0.2}{2}=0.1\left(mol\right)\)
\(Đặt:n_{CO_2}=x\left(mol\right)\)
\(\overline{M}=\dfrac{0.1\cdot28+0.1\cdot44+44x}{0.2+x}=20\cdot2=40\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow x=0.2\)
\(m_{CO_2\left(cầnthêm\right)}=0.2\cdot44=8.8\left(g\right)\)
Đúng 1
Bình luận (6)