Đốt cháy hoàn toàn hợp chất hữu cơ X, thu được CO 2 và H 2 O. Biết trong X có 52,17%C, 13,04%H (về khối lượng). Xác định công thức đơn giản nhất của X
Đốt cháy hoàn toàn 18 gam hợp chất hữu cơ (X) thu được 26,4 gam CO2 và
10,8 gam H2O.
Tỉ khối của X so với H2 là 45.
Xác định công thức phân tử và công
thức đơn giản nhất của X. (Cho biết C = 12, H = 1; O =16, N= 14
\(n_{CO_2}=\dfrac{26.4}{44}=0.6\left(mol\right)\)
\(n_{H_2O}=\dfrac{10.8}{18}=0.6\left(mol\right)\)
\(n_O=\dfrac{18-0.6\cdot12-0.6\cdot2}{16}=0.6\left(mol\right)\)
\(n_C:n_H:n_O=0.6:1.2:0.6=1:2:1\)
CT đơn giản nhất : \(CH_2O\)
\(M_X=45\cdot2=90\left(\dfrac{g}{mol}\right)\)
\(\Leftrightarrow30n=90\)
\(\Leftrightarrow n=3\)
\(CT:C_3H_6O_3\)
Đốt cháy hoàn toàn 2,9 gam chất hữu cơ X thu được 3,36 lít khí CO2 (đktc)
và 2,7 gam H2O.
a. Xác định công thức đơn giản nhất của X.
b. Xác định công thức phân tử của X, biết tỉ khối hơi của X so với H2 là 29.
(O = 16; C = 12; H = 1)
nCO2=0,15(mol) -> nC= 0,15(mol)
nH2O=0,15(mol) -> nH= 0,3(mol)
Giả sử X có 3 nguyên tố tạo thành: C,H và O.
mX=mC+mH+mO= 0,15.12+ 0,3.1+mO
<=> 2,9=2,1+mO
<=>mO=0,8(g) => nO=0,05(mol)
Gọi CTTQ : CxHyOz (x,y,z: nguyên, dương)
x:y:z=nC:nH:nO= 0,15:0,3:0,05=3:6:1
=> CTĐGN X: C3H6O
b) M(X)=29.2=58(g/mol)
Ta có: M(X)= M(C3H6O)a= 58a
=> 58a=58
<=>a=1
=> CTPT X: C3H6O
Đốt cháy hoàn toàn 5.4g một hợp chất hữu cơ A thu được 8.4 lít co2 và 8.1g nước a. Tính khối lượng gam và phần trăm khối lượng nguyên tố có trong Á b. Xác định công thức đơn giản nhất của A c. Xác định công thức phân tử của A. Biết tỉ khối hơi của A so với oxi là 2.25 d. Viết các công thức cấu tạo của A
a)
\(n_{CO_2}=\dfrac{8,4}{22,4}=0,375\left(mol\right)\)
\(n_{H_2O}=\dfrac{8,1}{18}=0,45\left(mol\right)\)
Bảo toàn C: nC = 0,375 (mol)
Bảo toàn H: nH = 0,9 (mol)
mC = 0,375.12 = 4,5 (g)
mH = 0,9.1 = 0,9 (g)
=> mO = 5,4 - 4,5 - 0,9 = 0 (g)
=> \(\left\{{}\begin{matrix}\%C=\dfrac{4,5}{5,4}.100\%=83,33\%\\\%H=\dfrac{0,9}{5,4}.100\%=16,67\%\end{matrix}\right.\)
b)
nC : nH = 0,375 : 0,9 = 5 : 12
=> CTDGN: C5H12
c)
CTPT: (C5H12)n
Mà M = 2,25.32 = 72 (g/mol)
=> n = 1
=> CTPT: C5H12
Để đốt cháy hoàn toàn 2,85 g chất hữu cơ X phải dùng vừa hết 4,20 lít O 2 (đktc). Sản phẩm cháy chỉ có C O 2 và H 2 O theo tỉ lệ 44 : 15 về khối lượng.
1. Xác định công thức đơn giản nhất của chất X.
2. Xác định công thức phân tử của X biết rằng tỉ khối hơi của X đối với C 2 H 6 là 3,80.
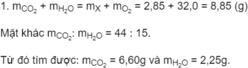
Khối lương C: 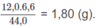
Khối lượng H: 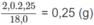
Khối lượng O: 2,85 - 1,80 - 0,25 = 0,80 (g).
Chất X có dạng CxHyOz
x : y : z = 0,150 : 0,25 : 0,050 = 3 : 5 : 1
Công thức đơn giản nhất của X là C 3 H 5 O .
2, M X = 3,80 x 30,0 = 114,0 (g/mol)
( C 3 H 5 O ) n = 114; 57n = 114 ⇒ n = 2.
Công thức phân tử C 6 H 10 O 2 .
Thủy phân hoàn toàn 2,85 gam hợp chất hữu cơ A (chứa C, H, O) thu được m1 gam chất X và m2 gam chất Y chỉ chứa một loại nhóm chức. Đốt cháy hết m1 gam X tạo ra 0,09 mol CO2 và 0,09 mol H2O, còn khi đốt cháy hết m2 gam Y thu được 0,03 mol CO2 và 0,045 mol H2O. Tổng lượng oxi tiêu tốn cho cả hai phản ứng cháy trên đúng bằng lượng oxi tạo ra khi nhiệt phân hoàn toàn 42,66 gam KMnO4. Biết phân tử khối của X là 90(u); Y không hòa tan Cu(OH)2. Xác định công thức phân tử của các chất A, X, Y biết A có công thức phân tử trùng với công thức đơn giản nhất.
Khi phân tích một hợp chất hữu cơ (X) có thành phần như sau: %C = 52,17%; %H = 13,04% và %O = 34,78%. Công thức phân tử của (X) nào sau đây đúng ? Biết công thức đơn giản nhất trùng với công thức phân tử
A. C2H6O
B. CH4O
C. C3H8O
D. C4H10O
Đốt cháy hoàn toàn 9,2 gam chất hữu cơ X thu được 13,2 gam CO2 và 7,2 gam
H2O.
a. Xác định công thức đơn giản nhất của X.
b. Xác định công thức phân tử của X, biết tỉ khối hơi của X so với H2 là 46.
\(n_{CO_2}=\dfrac{13.2}{44}=0.3\left(mol\right)\)
\(n_{H_2O}=\dfrac{7.2}{18}=0.4\left(mol\right)\)
\(n_O=\dfrac{9.2-0.3\cdot12-0.4\cdot2}{16}=0.3\left(mol\right)\)
\(n_C:n_H:n_O=0.3:0.8:0.3=3:8:3\)
CT đơn giản nhất : C3H8O3
\(M_X=46\cdot2=92\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow92n=92\)
\(\Rightarrow n=1\)
\(CT:C_3H_8O_3\)
a)
$n_C = n_{CO_2} = \dfrac{13,2}{44} = 0,3(mol)$
$n_H = 2n_{H_2O} = 2.\dfrac{7,2}{18} = 0,8(mol)$
$n_O = \dfrac{9,2 -0,3.12 - 0,8.1}{16} = 0,3(mol)$
Ta có :
$n_C : n_H : n_O = 0,3: 0,8 : 0,3 = 3 : 8:3$
Vậy CTĐGN là $C_3H_8O_3$
b)
CTPT : $(C_3H_8O_3)_n$
Ta có :
$M_X = (12.3 + 8 + 16.3)n = 46.2 \Rightarrow n = 1$
Vậy CTPT là $C_3H_8O_3$
Đốt cháy hoàn toàn 1,8 gam hợp chất hữu cơ (A) thu được 1,792 lít CO2
(đktc) và 1,8 gam H2O. Tỉ khối của A so với H2 là 45. Xác định công thức phân tử
và công thức đơn giản nhất của A. (Cho biết C = 12, H = 1; O =16, N= 14)
$n_C = n_{CO_2} = \dfrac{1,792}{22,4} = 0,08(mol)$
$n_H = 2n_{H_2O} = 2.\dfrac{1,8}{18} = 0,2(mol)$
$n_O = \dfrac{1,8 - 0,08.12 - 0,2.1}{16} = 0,04(mol)$
Ta có :
$n_C : n_H : n_O = 0,08 : 0,2 : 0,04 = 2 : 5 : 1$
Vậy CTĐGN là $C_2H_5O$
CTPT : $(C_2H_5O)_n$
$M_A = (12.2 + 5 + 16)n = 45.2 \Rightarrow n = 2$
Vậy CTPT là $C_4H_{10}O_2$
\(n_{CO_2}=\dfrac{1.792}{22.4}=0.08\left(mol\right)\)
\(n_{H_2O}=\dfrac{1.8}{18}=0.1\left(mol\right)\)
\(n_O=\dfrac{1.8-0.08\cdot12-0.1\cdot2}{16}=0.04\left(mol\right)\)
\(n_C:n_H:n_O=0.08:0.2:0.04=2:5:1\)
Công thức đơn giản nhất : C2H5O
\(M_A=2\cdot45=90\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow45n=90\)
\(\Rightarrow n=2\)
\(CT:C_4H_{10}O_2\)
Đốt cháy hoàn toàn 24,4 gam hợp chất hữu cơ (A) thu được 17,92 lít CO2
(đktc) và 18 gam H2O. Tỉ khối của A so với H2 là 61. Xác định công thức phân tử
và công thức đơn giản nhất của A. (Cho biết C = 12, H = 1; O =16, N= 14)
\(n_{CO_2}=\dfrac{17.92}{22.4}=0.8\left(mol\right)\)
\(n_{H_2O}=\dfrac{1.8}{18}=0.1\left(mol\right)\)
\(n_O=\dfrac{24.4-0.8\cdot12-1\cdot2}{16}=0.8\left(mol\right)\)
\(n_C:n_H:n_O=0.8:2:0.8=4:10:4\)
CT đơn giản nhất : C4H10O4
\(M_A=61\cdot2=122\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow122n=122\)
\(\Rightarrow n=1\)
\(CT:C_4H_{10}O_4\)