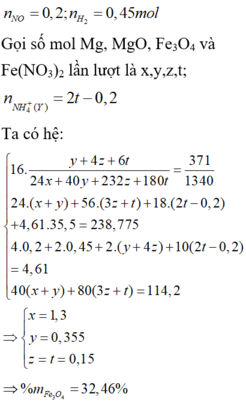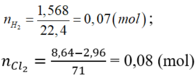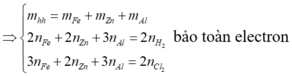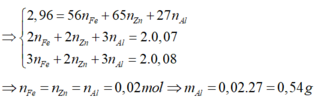Cho 1,53g X gồm Mg; Fe; Zn và Al phản ứng hoàn toàn với dung dịch HCl dư thấy tạo ra 448ml khí H2 đktc. Khối lượng muối clorua tạo ra sau phản ứng là

Những câu hỏi liên quan
Hòa tan hoàn toàn hỗn hợp X gồm Mg, MgO, Fe3O4 và Fe(NO3)2 (trong đó oxi chiếm
371
1340
khối lượng hỗn hợp X) trong dung dịch HCl dư thấy có 4,61 mol HCl phản ứng. Sau khi các phản ứng xảy ra xong thu được dung dịch Y chỉ chứa 238,775 gam muối clorua và 14,56 lít (đktc) hỗn hợp khí gồm NO, H2. Hỗn hợp Z có tỉ khối so với H2 là
69
12
.Thêm dung dịch NaOH dư vào Y, sau phản ứng thu được kết tủa Z. Nung Z trong không...
Đọc tiếp
Hòa tan hoàn toàn hỗn hợp X gồm Mg, MgO, Fe3O4 và Fe(NO3)2 (trong đó oxi chiếm 371 1340 khối lượng hỗn hợp X) trong dung dịch HCl dư thấy có 4,61 mol HCl phản ứng. Sau khi các phản ứng xảy ra xong thu được dung dịch Y chỉ chứa 238,775 gam muối clorua và 14,56 lít (đktc) hỗn hợp khí gồm NO, H2. Hỗn hợp Z có tỉ khối so với H2 là 69 12 .Thêm dung dịch NaOH dư vào Y, sau phản ứng thu được kết tủa Z. Nung Z trong không khí đến khối lượng không đổi được 114,2 gam chất rắn T. Phần trăm khối lượng Fe3O4 trong X gần nhất với giá trị nào sau đây?
A. 13%
B. 32%
C. 24%
D. 27%
Hòa tan hoàn toàn m gam hỗn hợp X gồm Al, Fe, Zn bằng dung dịch HCl dư. Dung dịch thu được sau phản ứng tăng lên so với ban đầu (m – 2) gam. Khối lượng (gam) muối clorua tạo thành trong dung dịch là A. m +71. B. m + 36,5. C. m + 35,5. D. m + 73.
Đọc tiếp
Hòa tan hoàn toàn m gam hỗn hợp X gồm Al, Fe, Zn bằng dung dịch HCl dư. Dung dịch thu được sau phản ứng tăng lên so với ban đầu (m – 2) gam. Khối lượng (gam) muối clorua tạo thành trong dung dịch là
A. m +71.
B. m + 36,5.
C. m + 35,5.
D. m + 73.
Hòa tan hoàn toàn hỗn hợp X gồm Fe(NO3)2, Fe3O4, MgO và Mg trong dung dịch chứa 9,22 mol HCl loãng. Sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch Y chỉ chứa 463,15 gam muối clorua và 29,12 lít (đktc) khí Z gồm NO và H2 có tỉ khối so với H2 là 69/13. Thêm NaOH dư vào dung dịch Y, sau phản ứng thấy xuất hiện kết tủa T. Nung T trong không khí đến khối lượng không đổi được 204,4 gam chất rắn M. Biết trong X, oxi chiếm 29,68% theo khối lượng. Phần trăm khối lượng MgO trong X gần nhất với g...
Đọc tiếp
Hòa tan hoàn toàn hỗn hợp X gồm Fe(NO3)2, Fe3O4, MgO và Mg trong dung dịch chứa 9,22 mol HCl loãng. Sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch Y chỉ chứa 463,15 gam muối clorua và 29,12 lít (đktc) khí Z gồm NO và H2 có tỉ khối so với H2 là 69/13. Thêm NaOH dư vào dung dịch Y, sau phản ứng thấy xuất hiện kết tủa T. Nung T trong không khí đến khối lượng không đổi được 204,4 gam chất rắn M. Biết trong X, oxi chiếm 29,68% theo khối lượng. Phần trăm khối lượng MgO trong X gần nhất với giá trị nào dưới đây?
A. 13,33%.
B. 33,33%.
C. 20,00%.
D. 6,80%.
Z gồm NO (0,4) và H2 (0,9)
Ban đầu đặt mX =m → nO= 29,68%m/16.
Do chỉ thu được muối clorua nên bảo toàn O: nH2O = 29,68%m/16 - 0,4
Bảo toàn khối lượng:
m+9,22.36,5 = 463,15 + 1,3.2.69/13 +18(29,68%m/16 - 0,4) → m=200
Vậy nO = 3,71 và nH2O = 3,31
Bảo toàn H → nNH4+ = 0,2
Bảo toàn N → nFe(NO3)2 = 0,3
Đặt a, b, c là số mol Mg, MO, Fe3O4 trong X → nO =b+4c +0,3.6 = 3,71
mX = 24a + 40b + 232c + 180.0,3 = 200
mT = 40(a + b) + 160(3c + 0,3)/2 = 204,4
→ a = 2; b = 0,71; c = 0,3
→ %MgO=142%
Đáp án A
Đúng 0
Bình luận (0)
Cho 11,7 gam hỗn hợp X gồm Mg và Al phản ứng với dung dịch H2SO4 (loãng, dư), thu được 0,6 mol khí H2 ( đktc). Tính khối lượng muối tạo ra từ các phản ứng.
Mg+H2SO4->MgSO4+H2
x-------------------------------x
2Al+3H2SO4->Al2(SO4)3+3H2
y-------------------------------------3\2y
Ta có :
\(\left\{{}\begin{matrix}24x+27y=11,7\\x+\dfrac{3}{2}y=0,6\end{matrix}\right.\)
=>x=0,15 mol , y=0,3 mol
=>m MgSO4=0,15.120=18g
=>m Al2(SO4)3=0,15.342=51,3g
Đúng 3
Bình luận (1)
Cho 4,69g hỗn hợp Mg và Zn tác dụng hết với dung dịch HCl thấy thoát ra 2,464 lít H2 ở đktC. Khối lượng muối tạo ra trong dung dịch sau phản ứng là
A. 10,68
B. 10,74
C. 12,72
D. 12,5
Đáp án D
Xét sơ đồ: Kim loại + 2HCl → Muối clorua + H2
Ta có nH2 = 2,464/22,4 = 0,11 mol => nHCl = 0,22 mol
Bảo toàn khối lượng, ta rút ra được:
mmuối = mkim loại + mHCl – mH2 = 4,69 + 36,5.0,22 – 2.0,11 = 12,5g
Cách khác: Sử dụng công thức tính nhanh:
mmuối clorua = mkim loại + 71nH2 = 4,69 + 71.0,11 = 12,5
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 2,96 gam hỗn hợp X gồm Fe, Zn, Al bằng dung dịch HCl dư, thu được 1,568 lít khí
H
2
(đktc). Mặt khác, cho 2,96 gam X phản ứng hoàn toàn với khí
C
l
2
dư, thu được 8,64 gam muối. Khối lượng Al trong 2,96 gam X là A. 0,54 gam. B. 0,81 gam. C. 0,27 gam. D. 1,08 gam.
Đọc tiếp
Hòa tan hoàn toàn 2,96 gam hỗn hợp X gồm Fe, Zn, Al bằng dung dịch HCl dư, thu được 1,568 lít khí H 2 (đktc). Mặt khác, cho 2,96 gam X phản ứng hoàn toàn với khí C l 2 dư, thu được 8,64 gam muối. Khối lượng Al trong 2,96 gam X là
A. 0,54 gam.
B. 0,81 gam.
C. 0,27 gam.
D. 1,08 gam.
Cho 0,87 gam hỗn hợp gồm Fe, Cu và Al vào bình đựng 300ml dung dịch H2SO4 0,1M. Sau khi các phản ứng xảy ra hoàn toàn thu được 0,32 gam chất rắn và có 448ml khí (đktc) thoát ra. Thêm tiếp vào bình 0,425 gam NaNO3, khi các phản ứng kết thúc thì thể tích khí NO (đktc, sản phẩm khử duy nhất) tạo thành và khối lượng muối trong dung dịch là: A.0,224 lít và 3,750 gam B. 0,112 lít và 3,750 gam C. 0,224 lít và 3,865 gam D. 0,112 lít và 3,865 gam
Đọc tiếp
Cho 0,87 gam hỗn hợp gồm Fe, Cu và Al vào bình đựng 300ml dung dịch H2SO4 0,1M. Sau khi các phản ứng xảy ra hoàn toàn thu được 0,32 gam chất rắn và có 448ml khí (đktc) thoát ra. Thêm tiếp vào bình 0,425 gam NaNO3, khi các phản ứng kết thúc thì thể tích khí NO (đktc, sản phẩm khử duy nhất) tạo thành và khối lượng muối trong dung dịch là:
A.0,224 lít và 3,750 gam
B. 0,112 lít và 3,750 gam
C. 0,224 lít và 3,865 gam
D. 0,112 lít và 3,865 gam
Cho 0,87 gam hỗn hợp gồm Fe, Cu và Al vào dung dịch H2SO4
→ Chất rắn không tan là Cu, mCu= 0,32 gam, nCu=0,005 mol
2Al+ 3H2SO4 → Al2(SO4)3+ 3H2
Fe+ H2SO4 → FeSO4+ H2
Ta có mFe + mAl = 0,87 - 0,32 = 0,55 gam
Đặt nFe= x mol, nAl= y mol → 56x + 27y= 0,55
nH2= 1,5.x+ y= 0,448/22,4= 0,02 mol
=> x = 0,005; y= 0,01
ta có nH2SO4 ban đầu= 0,3.0,1=0,03 mol, nH2= 0,448/22,4=0,02 mol
nH+ còn lại = nH+ ban đầu- nH+ pứ= 2.nH2SO4- 2.nH2= 2. 0,03- 2.0,02= 0,02 mol
nNO3- =nNaNO3= 0,005 mol
Ta có các bán phản ứng sau
Fe2+ → Fe3+ + 1e
0,005 0,005
Cu -→ Cu2+ + 2e
0,005 0,01
=> ne cho = 0,015 mol= n e nhận
4H+ + NO3- + 3e → NO + 2H2O (3)
0,02 0,005 0,015 0,005
V = 0,005.22,4 = 0,112 lít
Theo bán phản ứng (3) thì cả H+ và NO3- đều hết
Khối lượng muối=Khối lượng kim loại + mNa+ + mSO4
= 0,87 + 0,005.23 + 0,03.96 = 3,865 gam
Đáp án D
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 13,47 gam hỗn hợp X gồm Mg, Fe, Zn và Al vào dung dịch HCl dư, phản ứng hoàn toàn thu được 40,45 gam muối clorua. Mặt khác, đốt 13,47 gam hỗn hợp X trong khí Cl2 dư thu được 44 gam muối clorua. Thành phần phần trăm khối lượng Fe có trong hỗn hợp X là
A. 41,57%. B. 26,35%. C. 33,26%. D. 37,42%.
Xem chi tiết
Đặt \(\left\{{}\begin{matrix}n_{Mg}=a\left(mol\right)\\n_{Fe}=b\left(mol\right)\\n_{Zn}=c\left(mol\right)\\n_{Al}=d\left(mol\right)\end{matrix}\right.\) \(\Rightarrow95a+127b+136c+133,5d=40,45\) (1)
Sau p/ứ với Clo, ta được: \(95a+162,5b+136c+133,5d=44\) (2)
Lấy PT (2) trừ PT (1) \(\Rightarrow35,5b=3,55\) \(\Rightarrow b=n_{Fe}=0,1\left(mol\right)\)
\(\Rightarrow\%m_{Fe}=\dfrac{0,1\cdot56}{13,47}\cdot100\%\approx41,57\%\)
Đúng 1
Bình luận (0)
Hòa tan m gam hỗn hợp X (gồm Al, Fe, Zn và Mg) bằng dung dịch HCl dư. Sau phản ứng, khối lượng dung dịch axit tăng thêm (m – 0,8) gam. Khối lượng (gam) của muối tạo thành trong dung dịch sau phản ứng là
A. m + 14,2
B. m +28,4
C. m + 42,6
D. m + 71