Đốt cháy hoàn toàn 0,15 mol anken X thu được 6,72 lít khí CO2 (đktc). Tìm CTPT, CTCT và gọi tên X.

Những câu hỏi liên quan
Bài 1: Đốt cháy hoàn toàn một hidrocacbon X thu được 0,1 mol CO2 và 0,15 mol H2O. Tìm tên gọi của X
Bài 2: Khi đốt cháy hoàn toàn 4,48 lít hỗn hợp khí gồm CH4, C2H6, C3H8 (đktc) thu được V lít khí CO2(đktc) và 18g H2O. Tìm V
Bài 1 :
\(n_{H_2O}>n_{CO_2}\Rightarrow X:ankan\)
\(Đặt:CTHH:C_nH_{2n+2}\)
\(\dfrac{n}{2n+2}=\dfrac{0.1}{0.3}\Rightarrow n=2\)
\(Vậy:Xlà:C_2H_6\left(etan\right)\)
Đúng 1
Bình luận (0)
Bài 1
\(n_{CO_2} < n_{H_2O} \to\) X là ankan (CnH2n+2)
\(n_X = n_{H_2O} - n_{CO_2} = 0,15 - 0,1 = 0,05(mol)\)
Suy ra: \(n = \dfrac{n_{CO_2}}{n_X} = \dfrac{0,1}{0,05} = 2\)
Vậy X là C2H6(etan)
Bài 2 :
Hỗn hợp có dạng CnH2n+2
\(n_{hỗn\ hợp} = \dfrac{4,48}{22,4} = 0,2(mol)\\ n_{H_2O} = \dfrac{18}{18} = 1(mol)\\ \Rightarrow n + 2 = \dfrac{2n_{H_2O}}{n_{hh}} = 5\\ Suy\ ra\ n = 3\)
\(\Rightarrow n_{CO_2} = 3n_{hh} = 0,2.3 = 0,6(mol)\\ \Rightarrow V = 0,6.22,4 = 13,44(lít)\)
Đúng 1
Bình luận (0)
Bài 2 :
\(n_{H_2O}=\dfrac{18}{18}=1\left(mol\right)\)
\(n_{ankan}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(n_{CO_2}=n_{H_2O}-n_{ankan}=1-0.2=0.8\left(mol\right)\)
\(V_{CO_2}=0.8\cdot22.4=17.92\left(l\right)\)
Đúng 0
Bình luận (0)
Khi đốt cháy hoàn toàn một hidrocacbon X thu được 8,96 lít khí CO2(đktc) và 9 gam nước.Xác định CTPT, CTCT, gọi tên ankan X?
\(n_{H_2O} = \dfrac{9}{18} = 0,5(mol)\\ n_{CO_2} = \dfrac{8,96}{22,4} = 0,4(mol)\\ \Rightarrow n_X = n_{H_2O} - n_{CO_2}= 0,5 - 0,4 = 0,1(mol)\\ X\ :\ C_nH_{2n+2}(n \geq 1)\\ n = \dfrac{n_{CO_2}}{n_X} = \dfrac{0,4}{0,1} = 4\\ \Rightarrow CTPT\ X\ : C_4H_{10}\)
CTCT :
\(CH_3-CH_2-CH_2-CH_3 : butan\\ CH_3-CH(CH_3)-CH_3 : 2-metylpropan\)
Đúng 3
Bình luận (0)
Khi đốt cháy hoàn toàn 3,6g ankan X thu được 5,6 lít khí CO2 (đktc). Xác định CTPT, CTCT, gọi tên ankan X?
X : CnH2n+2
\(n_{CO_2} = \dfrac{5,6}{22,4} = 0,25(mol)\\ \Rightarrow n_X = \dfrac{0,25}{n}(mol)\\ \Rightarrow M_X = 14n + 2 = \dfrac{3,6}{\dfrac{0,25}{n}} = 14,4n\\ \Rightarrow n = 5\)
Vậy CTPT của X: C5H12
CTCT :
\(CH_3-CH_2-CH_2-CH_2-CH_3\ : pentan\\ CH_3-CH(CH_3)-CH_2-CH_3 : 2-metylbutan\\ CH_3-C(CH_3)_2-CH_3 : 2,2-đimetylpropan\\ \)
Đúng 3
Bình luận (0)
Đốt cháy hoàn toàn 5,8 gam một ankan thu được 8,96 lít khí CO2 ở đktc a) xác định CTPT, CTCT gọi tên ankan b) đốt cháy hoàn toàn lượng anken trên, dẫn sản phẩm cháy vào Ca(OH)2 dư. Tính khối lượng kết tủa thu được
nCO2=8,96/22,4=0,4 mol
=> nC=nCO2=0,4 mol
mC=0,4.12=4,8g
=> mH=5,8-4,8=1g
nH=1 mol -> nH2O=0,5
nH=0,5 mol
Pt: CnH2n+2 + (3n+1/2)O2-> nCO2 + (n+1)H2O
0,4 0,5 mol
=> n/0,4=n+1/0,5 -> n=4
Vậy cthh cần tìm là C4H10
Đúng 3
Bình luận (0)
Đốt cháy hoàn toàn 0,15 mol ancol no đơn chức thu được 6,72 lít khí CO2 ở đktc. Vậy CTPT của ancol là:
A. CH3OH
B. C2H5OH
C. C3H7OH
D. C3H5OH
Đáp án B
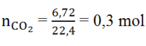
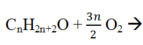
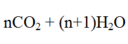
1mol n mol
0,15 0,3
=> 0,15n = 0,3 ó n = 2
Vậy CTCT của rượu là C2H5OH
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 0,1 mol một hiđrocacbon mạch hở X thu được 4,48 lít CO2 (đktc) và 3,6 gam H2O1. Xác định CTPT, viết CTCT và gọi tên của X.2. Dẫn 3,36 lít hỗn hợp gồm axetilen và X đi vào một lượng dư dung dịch AgNO3 trong NH3 thấy còn 0,84 lít khí thoát ra và có m gam kết tủa. Các thể tích khí đo ở đktc. a. Tính phần trăm thể tích của X trong hỗn hợp. b. Viết PTHH xảy ra và tính m. ( Cho Ag108, C12, H1, O16) Mọi người giúp mình với ạ, mình cảm ơn
Đọc tiếp
Đốt cháy hoàn toàn 0,1 mol một hiđrocacbon mạch hở X thu được 4,48 lít CO2 (đktc) và 3,6 gam H2O
1. Xác định CTPT, viết CTCT và gọi tên của X.
2. Dẫn 3,36 lít hỗn hợp gồm axetilen và X đi vào một lượng dư dung dịch AgNO3 trong NH3 thấy còn 0,84 lít khí thoát ra và có m gam kết tủa. Các thể tích khí đo ở đktc.
a. Tính phần trăm thể tích của X trong hỗn hợp.
b. Viết PTHH xảy ra và tính m. ( Cho Ag=108, C=12, H=1, O=16) Mọi người giúp mình với ạ, mình cảm ơn
1)
\(n_{CO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
=> nC = 0,2 (mol)
Số nguyên tử C = \(\dfrac{0,2}{0,1}=2\) (nguyên tử)
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\)
=> nH = 0,4 (mol)
Số nguyên tử H = \(\dfrac{0,4}{0,1}=4\) (nguyên tử)
CTPT: C2H4
CTCT: \(CH_2=CH_2\) (etilen)
2)
a) Khí thoát ra là C2H4
\(\%V_{C_2H_4}=\dfrac{0,84}{3,36}.100\%=25\%\)
b)
PTHH: \(CH\equiv CH+2AgNO_3+2NH_3\rightarrow CAg\equiv CAg\downarrow+2NH_4NO_3\)
\(n_{C_2H_2}=\dfrac{3,36-0,84}{22,4}=0,1125\left(mol\right)\)
=> \(n_{C_2Ag_2}=0,1125\left(mol\right)\)
=> m = 0,1125.240 = 27 (g)
Đúng 3
Bình luận (0)
1)
\(n_{CO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
=> nC = 0,2 (mol)
Số nguyên tử C = \(\dfrac{0,2}{0,1}=2\) (nguyên tử)
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\)
=> nH = 0,4 (mol)
Số nguyên tử H = \(\dfrac{0,4}{0,1}=4\) (nguyên tử)
CTPT: C2H4
CTCT: \(CH_2=CH_2\) (etilen)
2)
Đốt cháy hoàn toàn 10,8g một ankin X. Sau phản ứng thu được 17,92 lít khí CO2(Đktc) a) Hãy xác định CTPT của ankin X b) viết các CTCT có thể có và gọi tên(thay thế)
a) CTPT: CnH2n-2
\(n_{C_nH_{2n-2}}=\dfrac{10,8}{14n-2}\left(mol\right)\)
=> \(n_{CO_2}=\dfrac{10,8}{14n-2}.n=\dfrac{17,92}{22,4}=0,8\)
=> n = 4
=> CTPT: C4H6
b)
CTCT:
(1) \(CH\equiv C-CH_2-CH_3\) (but-1-in)
(2) \(CH_3-C\equiv C-CH_3\) (but-2-in)
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 10 lít hh X gồm 2 anken đồng đẳng kế tiếp thu được 26 lít CO2(đktc). Các thể tích khí đo ở cùng điều kiện nhiệt độ và áp suất
a)Xác định CTCT và gọi tên 2 anken
b)Tính % khối lượng mỗi anken trong hh
c)Hiđrat hóa hoàn toàn hh X thu được tối đa bao nhiêu ancol?
a) Gọi 2 anken có công thức chung: CnH2n;
CnH2n + O2 ---> nCO2 + nH2O
Vì ở cùng đk nhiệt độ và áp suất nên tỉ lệ về thể tích cũng chính là tỉ lệ về số mol. Do đó ta có: 10n = 26 nên n = 2,6 (số nguyên tử C trung bình).
Vì 2 anken kế tiếp nên chúng là: C2H4 (etilen) và C3H6 (propilen).
b) Gọi x, y tương ứng là số mol của 2 anken nói trên. Ta có: x + y = 10/22,4 = 0,446 và 2x + 3y = 26/22,4 = 1,16.
Tính được: x = 0,178 và y = 0,268 mol.
Vậy: mC2H4 = 28.0,178 = 4,984 g; mC3H6 = 42.0,268 = 11,256 g.
c) Hidrat hóa hoàn toàn X thu được 2 ancol: C2H5OH và C3H7OH có khối lượng là m = 46.0,178 + 60.0,268 = 24,268 g.
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 6,72 lít hỗn hợp khí X (đktc) gồm 1 ankan A và 1 anken B thu được 22g khí CO2 (đktc) và 12,6 gam H2O. CTPT của A và B là:
A. C2H6 và C2H4. B. CH4 và C2H4. C. C2H6 và C3H6. D. CH4 và C3H6
$n_{CO_2} = 0,5(mol) ; n_{H_2O} = 0,5625(mol)$
$\Rightarrow n_A = 0,5625 - 0,5 = 0,0625(mol)$
$\Rightarrow n_B = 0,3 - 0,0625 = 0,2375(mol)$
Bảo toàn C :
$0,0625.C_A + 0,2375.C_B = 0,5$
Không có số nguyên $C_A,C_B$ nào thỏa mãn
Đúng 1
Bình luận (1)

















