hòa tan hỗn hợp bột fe và feo trong dung dịch h2so4 loãng , sau đó làm bay hơi dung dịch thu đc 111,2 g feso4. 7h2o .tính thành phần % khối lượng các chất trong hỗn hợp ban đầu
hòa tan 27,2 gam hỗn hợp bột Fe và FeO trong dung dịch axit sunfuric loãng, sau đó làm bay hơi dung dịch thu được 111,2 gam FeSO4.7H2O. Thành phần phần trăm khối lượng các chất trong hỗn hợp là bao nhiêu ?
Gọi x, y lần lượt là số mol của Fe, FeO
nFeSO4.7H2O=111,2/278=0,4(mol)
Fe+H2SO4\(\rightarrow\)FeSO4+H2
x.......................x
FeO+H2SO4\(\rightarrow\)FeSO4+H2O
y.............................y
Ta có: nFeSO4=nFeSO4.7H2O=0,4(mol)
\(\Rightarrow\left\{{}\begin{matrix}x+y=0,4\\56x+72y=27,2\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,3\end{matrix}\right.\)
%mFe=\(\dfrac{0,1.56}{27,2}.100=20,59\%\)
%mFeO=79,41%
Chúc bạn học tốt!
Hòa tan hoàn toàn 20 g hỗn hợp Zn ,FeO bằng dung dịch H2SO4 loãng, dư. Phản ứng kết thúc thu được 4,48 lít khí h2 ở điều kiện tiêu chuẩn. Tính thành phần trăm theo khối lượng của mỗi chất có trong hỗn hợp ban đầu
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2mol\\ Zn+H_2SO_4\rightarrow ZnSO_4+H_2\\ FeO+H_2SO_4\rightarrow FeSO_4+H_2O\\ n_{Zn}=n_{H_2}=0,2mol\\ \%m_{Zn}=\dfrac{0,2.65}{20}\cdot100\%=65\%\\ \%m_{Fe}=100\%-65\%=35\%\)
Hòa tan hoàn toàn 18,2 g hỗn hợp gồm bột Al và Fe trong lọ đựng dung dịch NaOH dư sau phản ứng thu được 12,8 g chất rắn Tính thành phần phần trăm theo khối lượng của kim loại Al có trong hỗn hợp ban đầu
\(m_{cr}=m_{Fe}=12.8\left(g\right)\)
\(NaOH+Al+H_2O\rightarrow NaAlO_2+\dfrac{3}{2}H_2\)
\(m_{Al}=m_{hh}-m_{Fe}=18.2-12.8=5.4\left(g\right)\)
\(\%m_{Al}=\dfrac{5.4}{18.2}\cdot100\%=29.67\%\)
Al pư NaOH, Fe không pư NaOH nhé, nên chất rắn sau pư là Fe
\(2Al + 2NaOH + 2H_2O \rightarrow 2NaAlO_2 + 3H_2\)
\(m_{Al}= m_{hh} - m_{Fe}= 18,2 - 12,8 = 5,4 g\)
%mAl=\(\dfrac{5,4}{18,2} . 100\)% = 29,67%
hòa tan hoàn toàn 13,45g hỗn hợp X gồm Al, Fe, Cu trong dung dịch H2SO4 0,5M loãng, dư thì thu được 5,6l khí bay ra ở ĐKTC và còn lại 8g phần rắn Y không tan.
A/ tính phần trăm khối lượng mỗi chất ban đầu
B/ tính thể tích dung dịch H2SO4 tham gia phản ứng
a) Y là Cu
$m_{Cu} = 8(gam)$
Gọi $n_{Al} = a(mol) ; n_{Fe} = b(mol)$
Ta có : $27a + 56b + 8 = 13,45(1)$
$2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2$
$Fe + H_2SO_4 \to FeSO_4 + H_2$
$n_{H_2} = 1,5a + b = \dfrac{5,6}{22,4} = 0,25(2)$
Từ (1)(2) suy ra a = 0,15 ; b = 0,025$
$\%m_{Cu} = \dfrac{8}{13,45}.100\% = 59,47\%$
$\%m_{Al} = \dfrac{0,15.27}{13,45}.100\% = 30,11\%$
$\%m_{Fe} = 10,42\%$
b)
$n_{H_2SO_4} = n_{H_2} = 0,25(mol)$
$V_{dd\ H_2SO_4} = \dfrac{0,25}{0,5} = 0,5(lít)$
Hòa tan hoàn toàn 8 gam hỗn hợp các chất Fe và Fe2O3 bằng dung dịch H2SO4 loãng người ta thu được 2,24 l khí H2(đktc) a.viết các phương trình hóa học b.xác định thành phần phần trăm theo khối lượng của các chất trong hỗn hợp ban đầu
\(a) \\ Fe + H_2SO_4 \to FeSO_4 + H_2\\ Fe_2O_3 + 3H_2SO_4 \to Fe_2(SO_4)_3 + 3H_2O\\ b) \text{Theo PTHH} : \\ n_{Fe} = n_{H_2} = \dfrac{2,24}{22,4} = 0,1(mol)\\ \%m_{Fe} = \dfrac{0,1.56}{8} .100\% = 70\%\\ \%m_{Fe_2O_3} = 100\% -70\% = 30\%\)
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ PTHH:Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ \left(mol\right).....0,1...........................\leftarrow0,1\\ m_{Fe}=0,1.56=5,6\left(g\right)\\ m_{Fe_2O_3}=\Sigma m_{hh}-m_{Fe}=8-5,6=2,4\left(g\right)\\ PTHH:Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\\ \left\{{}\begin{matrix}\%m_{Fe}=\dfrac{5,6}{8}.100\%=70\%\\\%m_{Fe_2O_3}=\dfrac{2,4}{8}.100\%=30\%\end{matrix}\right.\)
Nung nóng 3,72g hỗn hợp bột các kim loại Zn và Fe trong bột S dư. Chất rắn thu được sau phản ứng được hòa tan hoàn toàn bằng dung dịch H2SO4 loãng, nhận thấy có 1,344 lít khí (đktc) thoát ra. Xác định khối lượng mỗi kim loại trong hỗn hợp ban đầu.
Đặt nZn = x mol; nFe = y mol.
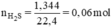
Ta có hệ phương trình: 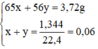
Giải hệ phương trình trên ta được:
x = 0,04 mol, y = 0,02 mol.
mZn = 65 × 0,04 = 2,6g
mFe = 56 × 0,02 = 1,12g
X là hỗn hợp rắn gồm Mg, NaNO3 và FeO (trong đó oxi chiếm 26,4% về khối lượng). Hòa tan hết m gam X trong 2107 gam H2SO4 loãng, nồng độ 10% thu được dung dịch Y chỉ chứa muối sunfat trung hòa và 11,2 lít (đktc) hỗn hợp khí NO, H2 có tỉ khối hơi so với H2 là 6,6. Cô cạn dung dịch dung sau phản ứng được rắn khan Z và 1922,4 gam H2O. Phần trăm khối lượng của FeO trong hỗn hợp ban đầu gần nhất với giá trị nào sau dây?
A. 50%.
B. 12%.
C. 33%.
D. 40%.
Có hỗn hợp gồm NaI và NaBr. Hòa tan hỗn hợp vào nước. Cho Br dư vào dung dịch, làm khô sản phẩm, thì thấy khối lượng của sản phẩm nhỏ hơn khối lượng hỗn hợp ban đầu là m (g). Lại hòa tan sản phẩm vào nước và clo lội qua cho đến dư. Làm bay hơi dung dịch và làm khô chất còn lại người ta thấy khối lượng chất thu được lại nhỏ hơn khối lượng muối phản ứng là m gam. Thành phần phần trăm về khối lượng của NaBr trong hỗn hợp đầu là?
A. 3,7%.
B. 7,3%.
C. 5,7%.
D. 20%.
Gọi a, b lần lượt là số mol của NaI và NaBr ban đầu, ta có : Sơ đồ phản ứng:
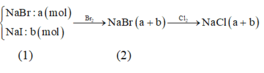

Đáp án A
hòa tan 54,4gam hỗn hợp X gồm Fe và FeO vào dd H2SO4loãng,sau đó làm bay hơi dd người ta thu đc 222,4gam chất rắn FeSO4.7H2O.
Viết các phương trình phản ứng và tính thành phần phần trăm theo khối lượng của mỗi chất trong hỗn hợp X.Biết các phản ứng xảy ra hoàn toàn
a)
$Fe + H_2SO_4 \to FeSO_4 + H_2$
$FeO + H_2SO_4 \to FeSO_4 + H_2O$
$FeSO_4 + 7H_2O \to FeSO_4.7H_2O$
b)
n Fe = a(mol) ; n FeO = b(mol)
=> 56a + 72b = 54,4(1)
Theo PTHH :
n FeSO4.7H2O = a + b = 222,4/278 = 0,8(2)
Từ (1)(2) suy ra a = 0,2 ; b = 0,6
Suy ra :
%m Fe = 0,2.56/54,4 .100% = 20,59%
%m FeO = 100% -20,59% = 79,41%