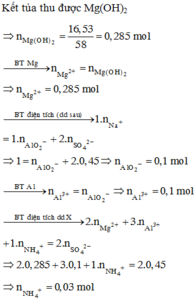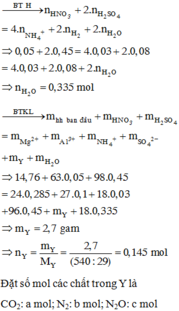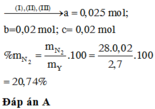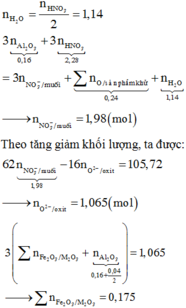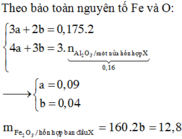cho 24.8 gam n2o tác dụng với dung dịch chứa 50.4 gam hno3.tính khối lượng các chất thu được sau phản ứng

Những câu hỏi liên quan
. Cho 24,8 gam Na2O tác dụng với dung dịch chứa 50,4 gam HNO3. Tính khối lượng các
chất thu được sau phản ứng.
Ta có: \(n_{Na_2O}=\dfrac{24,8}{62}=0,4\left(mol\right)\)
\(n_{HNO_3}=\dfrac{50,4}{63}=0,8\left(mol\right)\)
PT: \(Na_2O+2HNO_3\rightarrow2NaNO_3+H_2O\)
____0,4_____0,8_________0,8 (mol)
→ Pư vừa đủ.
\(\Rightarrow m_{NaNO_3}=0,8.85=68\left(g\right)\)
Bạn tham khảo nhé!
Đúng 0
Bình luận (0)
Cho 13,4 gam hỗn hợp Fe, Al, Mg tác dụng hết với một lượng dung dịch HNO3 2M (lấy dư 10%) thu được 4,48 lít hỗn hợp NO, N2O có tỉ khối đối với hiđro là 18,5 và dung dịch không chứa muối amoni. Thể tích dung dịch HNO3 đã dùng và khối lượng muối có trong dung dịch sau phản ứng là:
PTK trung bình của hỗn hợp NO và N2O = 18,5 x 2 = 37
--> n NO = n N2O = 4,48/44,8 = 0,1 mol
--> n HNO3 = 1,1(0,1 x 4 + 0,1 x 10) = 1,54 mol
--> Cm HNO3 = 1,54/2 = 0,77 lít = 770 ml.
m muối = 13,4 + 0,1 x 3 x 62 + 0,1 x 8 x 62 = 81,6 gam.
Đúng 0
Bình luận (0)
Cho 23,616 gam hỗn hợp X gồm Mg, Al, MgCO3 và Al(NO3)3 vào dung dịch chứa 0,72 mol H2SO4 và 0,08 mol HNO3, sau phản ứng thu được dung dịch Y chỉ chứa các muối sunfat trung hòa và hỗn hợp khí Z gồm CO2, NO, N2O và H2 (với số mol H2 là 0,128 mol). Dung dịch Y có thể phản ứng tối đa với 64 gam NaOH, sau phản ứng lọc lấy kết tủa đem nung đến khối lượng không đổi thu được 18,24 gam chất rắn khan. Phần trăm khối lượng của H2 trong Y gần nhất với A. 4 B. 5 C. 6 D. 7
Đọc tiếp
Cho 23,616 gam hỗn hợp X gồm Mg, Al, MgCO3 và Al(NO3)3 vào dung dịch chứa 0,72 mol H2SO4 và 0,08 mol HNO3, sau phản ứng thu được dung dịch Y chỉ chứa các muối sunfat trung hòa và hỗn hợp khí Z gồm CO2, NO, N2O và H2 (với số mol H2 là 0,128 mol). Dung dịch Y có thể phản ứng tối đa với 64 gam NaOH, sau phản ứng lọc lấy kết tủa đem nung đến khối lượng không đổi thu được 18,24 gam chất rắn khan. Phần trăm khối lượng của H2 trong Y gần nhất với
A. 4
B. 5
C. 6
D. 7
Chọn đáp án C
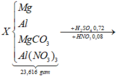
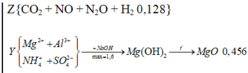
nMgO = 18,24/40 = 0,456 và n S O 4 2 - trong Y = 0,72 => nAl3+ trong Y =1,6 − 0,72×2 = 0,16
BTÐT => n N H 4 + = 0,72x2 − 0,16×3 − 0,456×2 = 0,048
Dễ thấy đề không cho quá nhiều dữ kiện về hỗn hợp khí Z, nhưng lại cho nH2 và bắt tìm phần trăm khối lượng H2 => Chỉ cần tìm khối lượng của Z, không cần tìm cụ thể số mol
Nhận thấy có đủ số mol ở tất cả các chất chứa hiđro trong quá trình
nH2O sau khi X tác dụng với axit = 0,72 + 0,08/2 – 0,128 – 0,048x2= 0,536
BTKL=>23,616+0,72×98+0,08×63 = mZ+0,456×24+0,16×27+0,048×18+0,72×96+0,536×18
=> mZ = 4,32 gam
Đúng 0
Bình luận (0)
Hòa tan hết m gam hỗn hợp X gồm Mg, FeSO4, Zn vào dung dịch chứa đồng thời HNO3 và 1,726 mol HCl, sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch Ychỉ chứa 95,105 gam các muối clorua và 0,062 mol hỗn hợp 2 khí N2O, NO ( tổng khối lượng hỗn hợp khí là 2,308 gam). Nếu đem dung dịch Y tác dụng với dung dịch AgNO3 dư thì thu được 254,161 gam kết tủa. Còn nếu đem dung dịch Y tác dụng với dung dịch NaOH dư thì thu được 54,554 gam kết tủa. Giá trị của m gần nhất với giá trị nào sau đây? A. 56,...
Đọc tiếp
Hòa tan hết m gam hỗn hợp X gồm Mg, FeSO4, Zn vào dung dịch chứa đồng thời HNO3 và 1,726 mol HCl, sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch Ychỉ chứa 95,105 gam các muối clorua và 0,062 mol hỗn hợp 2 khí N2O, NO ( tổng khối lượng hỗn hợp khí là 2,308 gam). Nếu đem dung dịch Y tác dụng với dung dịch AgNO3 dư thì thu được 254,161 gam kết tủa. Còn nếu đem dung dịch Y tác dụng với dung dịch NaOH dư thì thu được 54,554 gam kết tủa. Giá trị của m gần nhất với giá trị nào sau đây?
A. 56,7.
B. 43,0.
C. 38,0.
D. 46,0.
Đáp án B

BTNT: N => nHNO3 = nNH4+ + 2nN2O + nNO = t + 0,094 (mol)
BTNT: H => nHNO3 + nHCl = 4nNH4+ + 2nH2O
=> nH2O = [(t + 0,094) + 1,726 – 4t]/2 = 0,91 – 1,5t
BTNT: O => 4z + 3( t + 0,094) = 0,062 + ( 0,91 – 1,5t) (1)
BTĐT đối với các chất trong dd Y
=> 2x+ 2y + 0,06.2 + 3. (3z- 0,06) + t = 1,726 (2)
mmuối = 24x + 65y + 56.3z + 18t + 1,726.35,5 = 95,105 (3)
m↓ = 58y + 0,06.90 + 107( 3z- 0,06) = 54,554
=> 58y +321z = 55, 574 (4)
Giải hệ (1), (2), (3) và (4) => x = 0,128 ; y = 0,08 ; z = 0,15 ; t = 0,02 (mol)
=> m = 0,128. 24 + 0,08.65 + 0,15. 232 = 43,072 (g)
Gần nhất với 43 gam
Đúng 0
Bình luận (0)
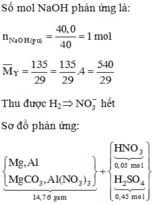
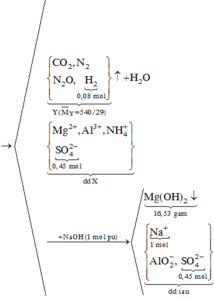
Hòa tan hết 14,76 gam hỗn hợp gồm Mg, Al, MgCO3, Al(NO3)3 trong dung dịch chứa 0,05 mol HNO3 và 0,45 mol H2SO4, sau phản ứng kết thúc thu được dung dịch X chỉ chứa các muối trung hòa và hỗn hợp khí Y gồm CO2, N2, N2O và H2 (trong đó H2 có số mol là 0,08 mol). Tỉ khối của Y so với He bằng 135/29. Cho dung dịch X tác dụng với dung dịch NaOH dư, thấy lượng NaOH phản ứng 40,0 gam, thu được 16,53 gam kết tủa. Phần trăm về khối lượng của N2 trong hỗn hợp Y là: A. 20,74%. B. 25,93%. C. 15,56%. D. 31...
Đọc tiếp
Hòa tan hết 14,76 gam hỗn hợp gồm Mg, Al, MgCO3, Al(NO3)3 trong dung dịch chứa 0,05 mol HNO3 và 0,45 mol H2SO4, sau phản ứng kết thúc thu được dung dịch X chỉ chứa các muối trung hòa và hỗn hợp khí Y gồm CO2, N2, N2O và H2 (trong đó H2 có số mol là 0,08 mol). Tỉ khối của Y so với He bằng 135/29. Cho dung dịch X tác dụng với dung dịch NaOH dư, thấy lượng NaOH phản ứng 40,0 gam, thu được 16,53 gam kết tủa. Phần trăm về khối lượng của N2 trong hỗn hợp Y là:
A. 20,74%.
B. 25,93%.
C. 15,56%.
D. 31,11%.
Đun nóng hỗn hợp Fe3O4, Fe2O3 và 19,44 gam Al trong khí trơ đến khi phản ứng xảy ra hoàn toàn thu được chất rắn X. Chia X làm hai phần bằng nhau. Phần 1 cho vào dung dịch NaOH dư thoát ra 0,06 mol H2. Phần 2 tác dụng vừa đủ với 420 gam dung dịch HNO3 34,2% thu được dung dịch Y chỉ chứa các muối kim loại và 5,376 lít (đktc) hỗn hợp khí Z gồm N2O và NO. Cô cạn dung dịch Y, sau đó lấy chất rắn nung trong chân không tới khối lượng không đổi thấy khối lượng chất rắn giảm 105,72 gam. Khối lượng Fe2O3...
Đọc tiếp
Đun nóng hỗn hợp Fe3O4, Fe2O3 và 19,44 gam Al trong khí trơ đến khi phản ứng xảy ra hoàn toàn thu được chất rắn X. Chia X làm hai phần bằng nhau. Phần 1 cho vào dung dịch NaOH dư thoát ra 0,06 mol H2. Phần 2 tác dụng vừa đủ với 420 gam dung dịch HNO3 34,2% thu được dung dịch Y chỉ chứa các muối kim loại và 5,376 lít (đktc) hỗn hợp khí Z gồm N2O và NO. Cô cạn dung dịch Y, sau đó lấy chất rắn nung trong chân không tới khối lượng không đổi thấy khối lượng chất rắn giảm 105,72 gam. Khối lượng Fe2O3 trong hỗn hợp ban đầu là:
A. 12,8 gam
B. 14,4 gam
C. 11,2 gam
D. 16,0 gam
Tính lượng muối nhôm sunfat tạo thành khí cho dung dịch chứa 490 gam axit H2SO4 10% tác dụng với 10,2 gam Al2O3. Tính khối lượng Al2(SO4)3 và nồng độ phần trăm các chất thu được trong dung dịch sau phản ứng?
n H2SO4=\(\dfrac{10\%.490}{2+32+16.4}=0,5mol\)
n Al2O3 =\(\dfrac{10,2}{27.2+16.3}=0,1mol\)
\(Al_2O_3+3H_2SO_4->Al_2\left(SO_4\right)_3+3H_2O\)
bđ 0,1............0,5
pư 0,1............0,3..................0,1
spu 0 ................0,2................0,1
=> sau pư gồm H2SO4 dư , Al2(S04)3 và H2O
m H2SO4 dư = \(0,2.\left(2+32+16.3\right)=19,6g\)
m Al2(SO4)3 = \(0,1\left(27.2+32.3+16.4.3\right)=34,2g\)
m dd = \(490+10,2=500,2g\)
% Al2(SO4)3 = \(\dfrac{34,2}{500,2}.100\sim6,84\%\)
% H2SO4 dư = \(\dfrac{19,6}{500,2}.100\sim3,92\%\)
Đúng 1
Bình luận (0)
Cho 3,2 gam Fe2O3 tác dụng với dung dịch có chứa 2,19 gam HCl thu được sản phẩm là FeCl3 và H2O
a) Chất nào còn dư sau phản ứng ? Dư bao nhiêu gam ?
b) Tính khối lượng các sản phẩm thu được ?
\(n_{Fe_2O_3}=\dfrac{3.2}{160}=0.02\left(mol\right)\)
\(n_{HCl}=\dfrac{2.19}{36.5}=0.06\left(mol\right)\)
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
\(1...........6\)
\(0.02...........0.06\)
Lập tỉ lệ : \(\dfrac{0.02}{1}>\dfrac{0.06}{6}\Rightarrow Fe_2O_3dư\)
\(n_{Fe_2O_3\left(dư\right)}=0.02-\dfrac{0.06}{6}=0.01\left(mol\right)\)
\(m_{Fe_2O_3\left(dư\right)}=0.01\cdot160=1.6\left(g\right)\)
\(m_{FeCl_3}=0.02\cdot162.5=3.25\left(g\right)\)
\(m_{H_2O}=0.03\cdot18=0.54\left(g\right)\)
Đúng 2
Bình luận (2)
Hòa tan hỗn hợp X gồm m gam Al và Al2O3 trong 1,4 lít dung dịch HNO3 1M thu được dung dịch Y và 1,568 lít (đktc) hỗn hợp khí Z có khối lượng 2,52 gam khí N2O và NO. Cô cạn dung dịch Y được chất T. Nung T đến khối lượng không đổi thu được (m+4,8) gam chất rắn. Mặt khác để tác dụng với các chất trong dung dịch Y thì cần tối đa 1,67 lít dung dịch KOH 1M. Giả sử các phản ứng xảy ra hoàn toàn. Phần trăm khối lượng của Al có trong X? A. 25,78% B. 34,61% C. 38,14% D. 40,94%
Đọc tiếp
Hòa tan hỗn hợp X gồm m gam Al và Al2O3 trong 1,4 lít dung dịch HNO3 1M thu được dung dịch Y và 1,568 lít (đktc) hỗn hợp khí Z có khối lượng 2,52 gam khí N2O và NO. Cô cạn dung dịch Y được chất T. Nung T đến khối lượng không đổi thu được (m+4,8) gam chất rắn. Mặt khác để tác dụng với các chất trong dung dịch Y thì cần tối đa 1,67 lít dung dịch KOH 1M. Giả sử các phản ứng xảy ra hoàn toàn. Phần trăm khối lượng của Al có trong X?
A. 25,78%
B. 34,61%
C. 38,14%
D. 40,94%