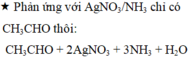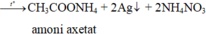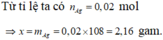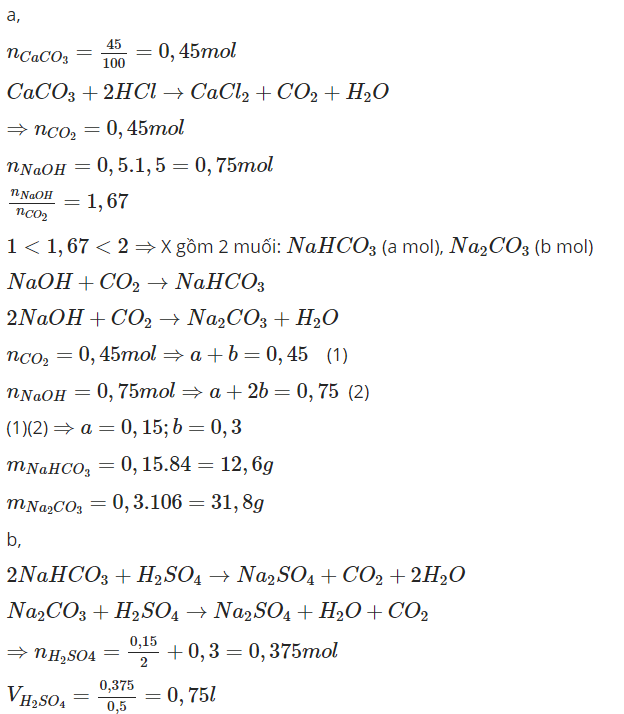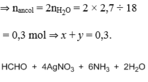Cần thêm bao nhiêu gam H2O để khi tác dụng với 500 (g) dug dịch C2H5OH 45% tạo ra dung dịch C2H5OH 30%

Những câu hỏi liên quan
Hỗn hợp X gồm C2H5OH, CH3COOCH3, CH3CHO, trong đó C2H5OH chiếm 50% về số mol. Khi đốt cháy hoàn toàn m gam hỗn hợp X thu được 3,06 gam H2O và 3,136 lít CO2 (đktc). Mặt khác, khi cho hỗn hợp X tác dụng với lượng dư dung dịch AgNO3 trong NH3 thu được x gam Ag. Giá trị của x là A. 2,16 B. 8,68 C. 4,32 D. 1,08
Đọc tiếp
Hỗn hợp X gồm C2H5OH, CH3COOCH3, CH3CHO, trong đó C2H5OH chiếm 50% về số mol. Khi đốt cháy hoàn toàn m gam hỗn hợp X thu được 3,06 gam H2O và 3,136 lít CO2 (đktc). Mặt khác, khi cho hỗn hợp X tác dụng với lượng dư dung dịch AgNO3 trong NH3 thu được x gam Ag. Giá trị của x là
A. 2,16
B. 8,68
C. 4,32
D. 1,08
Hỗn hợp X gồm CH3COOH và C2H5OH có khối lượng 16,6 gam tác dụng vừa đủ với 200 ml dung dịch NaOH 1M. Mặt khác, cho thêm dung dịch H2SO4 đặc và 9,2 gam C2H5OH vào 0,9 mol X được dung dịch Y. Đun nóng Y, thực hiện phản ứng este hóa với hiệu suất 80% thu được m gam este. Tính giá trị của m.
Gọi x, y lần lượt là số mol của CH3COOH và C2H5OH
X tác dụng vừa đủ với 200 ml dung dịch NaOH 1M => x = 0,2
mX = 60x + 46y = 16,6
=> y = 0,1
=> x : y = 2 : 1
=> 0,9 mol X có chứa 0,6 mol CH3COOH và 0,3 mol C2H5OH
=> Tổng C2H5OH = 0,5
Vậy giá trị của m = 35,2 (gam)
Đúng 0
Bình luận (0)
Chia 20,1 gam hỗn hợp X gồm CH3COOH, C2H5OH, aCH3COOC2H5 làm 3 phần. Cho phần 1 tác dụng với Na dư thu được 0,448 lít H2(đktc). Cho phần 2 tác dụng vừa đủ 500 ml dung dịch NaOH 0,2M đun nóng. Cho phần 3( có khối lượng bằng khối lượng phần 2) tác dụng với NaHCO3 dư thì có 1,344 lít ( đktc) khí bay ra. Khối lượng C2H5OH trong phần 1 là A. 2,3 gam B. 0,46 gam C. 1,38 gam D. 0,92 gam
Đọc tiếp
Chia 20,1 gam hỗn hợp X gồm CH3COOH, C2H5OH, aCH3COOC2H5 làm 3 phần. Cho phần 1 tác dụng với Na dư thu được 0,448 lít H2(đktc). Cho phần 2 tác dụng vừa đủ 500 ml dung dịch NaOH 0,2M đun nóng. Cho phần 3( có khối lượng bằng khối lượng phần 2) tác dụng với NaHCO3 dư thì có 1,344 lít ( đktc) khí bay ra. Khối lượng C2H5OH trong phần 1 là
A. 2,3 gam
B. 0,46 gam
C. 1,38 gam
D. 0,92 gam
Phần 2: n NaOH = n axit + n este = 0,1 mol Phần 3: n CO2 = n axit = 0,06 mol
Do 2 phần này có khối lượng như nhau nên => mỗi phần có neste = 0,04 mol
=> tổng cả 2 phần này có 0,12 mol axit và 0,08 mol este
Phần 1 giả sử có x mol ancol ; y mol este và 1,5y mol axit
( do tỉ lệ mol các chất trong hỗn hợp như nhau giữa các phần)
=> n ancol trong 2 phần còn lại là 0,08x/y mol => ta có:
Ở phần 1: 0,08x/y + 1,5y = 2nH2 = 0,04 mol
mX = 46(x+ 0,08x/y) + 60(0,12 + 1,5y ) + 88(y + 0,08)
Giải hệ ta được y = 0,02 mol ; x = 0,1 mol
=> m ancol (P1)= 0,46g =>B
Đúng 0
Bình luận (0)
cho 7(g) CaCO3 tác dụng với 5,475(g) HCl tạo thành CaCl2, khí CO2 và H2O. cần lấy thêm bao nhiêu Gam CaCO3 hay bao nhiêu Gam HCl để PƯ sảy ra hoàn toàn
\(n_{CaCO_3}=\dfrac{7}{100}=0,07\left(mol\right)\)
\(n_{HCl}=\dfrac{5,475}{36,5}=0,15\left(mol\right)\)
PTHH: CaCO3 + 2HCl --> CaCl2 + CO2 + H2O
Xét \(\dfrac{n_{CaCO_3}}{1}=0,07< \dfrac{n_{HCl}}{2}=0,075\)
=> HCl dư
Do đó, ta có:
PTHH: CaCO3 + 2HCl --> CaCl2 + CO2 + H2O
_______0,075<---0,15__________________________(mol)
=> \(m_{CaCO_3\left(cầnthêm\right)}=\left(0,075-0,07\right).100=0,5\left(g\right)\)
Đúng 1
Bình luận (0)
: Cho 4 gam một kim loại M hóa trị II tác dụng hết với H2O thu được 2,24 lít khí (đktc) và 500 gam dung dịch A.
a) Xác định tên của kim loại M và tính C% của dung dịch A
b) Để trung hòa hết 200 gam dung dịch A cần phải dùng bao nhiêu ml dung dịch HCl 2M
a, \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: M + 2H2O → M(OH)2 + H2
Mol: 0,1 0,1 0,1
\(\Rightarrow M_M=\dfrac{4}{0,1}=40\left(g/mol\right)\)
⇒ M là canxi (Ca)
\(C\%_{ddCa\left(OH\right)_2}=\dfrac{0,1.74.100\%}{500}=1,48\%\)
b) \(m_{Ca\left(OH\right)_2}=200.1,48=2,96\left(g\right)\Rightarrow n_{Ca\left(OH\right)_2}=\dfrac{2,96}{74}=0,04\left(mol\right)\)
PTHH: Ca(OH)2 + 2HCl → CaCl2 + 2H2O
Mol: 0,04 0,08
\(V_{ddHCl}=\dfrac{0,08}{2}=0,04\left(l\right)=40\left(ml\right)\)
Đúng 1
Bình luận (0)
Cho 45 gam CaCO3 tác dụng với dung dịch HCl dư, toàn bộ lượng khí sinh ra được hấp thụ trong một cốc có chứa 500 ml dung dịch NaOH 1,5M tạo thành dung dịch X.1- Tính khối lượng từng muối có trong X. 2- Tính thể tích dung dịch H2SO4 cần thiết để tác dụng với các chất có trong X tạo ra muối trung hoà.
Đọc tiếp
Cho 45 gam CaCO3 tác dụng với dung dịch HCl dư, toàn bộ lượng khí sinh ra được hấp thụ trong một cốc có chứa 500 ml dung dịch NaOH 1,5M tạo thành dung dịch X.
1- Tính khối lượng từng muối có trong X.
2- Tính thể tích dung dịch H2SO4 cần thiết để tác dụng với các chất có trong X tạo ra muối trung hoà.
Hỗn hợp X gồm C2H5OH, CH3COOCH3, CH3CHO, trong đó C2H5OH chiếm 50% về số mol. Khi đốt cháy hoàn toàn m gam hỗn hợp X thu được 3,06 gam H2O và 3,136 lít CO2 (đktc). Mặt khác, khi cho hỗn hợp X tác dung với lượng dư dung dịch AgNO3 trong NH3 thu được x gam Ag. Giá trị của x là A. 2,16 B. 8,68 C. 4,32 D. 1,08
Đọc tiếp
Hỗn hợp X gồm C2H5OH, CH3COOCH3, CH3CHO, trong đó C2H5OH chiếm 50% về số mol. Khi đốt cháy hoàn toàn m gam hỗn hợp X thu được 3,06 gam H2O và 3,136 lít CO2 (đktc). Mặt khác, khi cho hỗn hợp X tác dung với lượng dư dung dịch AgNO3 trong NH3 thu được x gam Ag. Giá trị của x là
A. 2,16
B. 8,68
C. 4,32
D. 1,08
Chọn đáp án A
Gọi số mol của C2H5OH, CH3COOCH3, CH3CHO lần lượt là a, b và c.
Theo đề bài ta có hệ pt: a a + b + c = 0 , 5
3a + 3b + 2c = 0,17
2a + 3b + 2c = 0,14
Giải hệ ta có a = 0,03, b = 0,02, c = 0,01
⇒ nAg = 2c = 0,02 mol
⇔ mAg = 2,16 gam
Đúng 0
Bình luận (0)
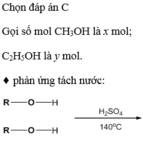
Đun nóng m gam hỗn hợp X gồm CH3OH và C2H5OH với H2SO4 đặc ở 140°C thu được 2,7 gam nước. Oxi hóa m gam X thành anđehit, rồi lấy toàn bộ lượng anđehit thu được cho tác dụng với dung dịch AgNO3 trong NH3 (dư) thấy tạo thành 86,4 gam Ag. Các phản ứng xảy ra với hiệu suất 100%. Phần trăm khối lượng của C2H5OH trong X là A. 37,1% B. 62,9% C. 74,2% D. 25,8%
Đọc tiếp
Đun nóng m gam hỗn hợp X gồm CH3OH và C2H5OH với H2SO4 đặc ở 140°C thu được 2,7 gam nước. Oxi hóa m gam X thành anđehit, rồi lấy toàn bộ lượng anđehit thu được cho tác dụng với dung dịch AgNO3 trong NH3 (dư) thấy tạo thành 86,4 gam Ag. Các phản ứng xảy ra với hiệu suất 100%. Phần trăm khối lượng của C2H5OH trong X là
A. 37,1%
B. 62,9%
C. 74,2%
D. 25,8%
Chọn đáp án C
Gọi số mol CH3OH là x mol; C2H5OH là y mol.
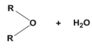
♦ phản ứng tách nước:
⇒ nancol = 2nH2O = 2 × 2,7 ÷ 18 = 0,3 mol
⇒ x + y = 0,3.
⇒ ∑nAg↓ = 4nHCHO + 2nCH3CHO = 0,8 mol
⇒ 4x + 2y = 0,8.
Giải hệ được x = 0,1 mol và y = 0,2 mol
⇒ mCH3OH = 3,2 gam; mC2H5OH = 9,2 gam.
⇒ %mC2H5OH trong X = 9,2 ÷ (9,2 + 3,2) × 100% ≈ 74,2%.
Đúng 0
Bình luận (0)
Đun nóng m gam hỗn hợp X gồm CH3OH và C2H5OH với H2SO4 đặc ở 140°C thu được 2,7 gam nước. Oxi hóa m gam X thành anđehit, rồi lấy toàn bộ lượng anđehit thu được cho tác dụng với dung dịch AgNO3 trong NH3 (dư) thấy tạo thành 86,4 gam Ag. Các phản ứng xảy ra với hiệu suất 100%. Phần trăm khối lượng của C2H5OH trong X là A. 37,1% B. 62,9% C. 74,2% D. 25,8%
Đọc tiếp
Đun nóng m gam hỗn hợp X gồm CH3OH và C2H5OH với H2SO4 đặc ở 140°C thu được 2,7 gam nước. Oxi hóa m gam X thành anđehit, rồi lấy toàn bộ lượng anđehit thu được cho tác dụng với dung dịch AgNO3 trong NH3 (dư) thấy tạo thành 86,4 gam Ag. Các phản ứng xảy ra với hiệu suất 100%. Phần trăm khối lượng của C2H5OH trong X là
A. 37,1%
B. 62,9%
C. 74,2%
D. 25,8%