
Những câu hỏi liên quan
Hòa tan hỗn hợp gồm FeO, Fe2O3 và F3O4 (có số mol bằng nhau) bằng dd H2SO4 20% (lượng axit lấy dư 50% so với lượng phản ứng vừa đủ), thu được dd A. Chia A thành bốn phần bằng nhau, mỗi phần có khối lượng 79,3 gam. Phần I tác dụng vừa đủ với V1 ml dung dịch KMnO4 0,05M. Phần II tác dụng vừa đủ với V2 ml dd brom 0,05M. Phần III tác dụng vừa đủ với V3 ml dd HI 0,05M. Cho Na2CO3 từ từ đến dư vào phần IV được V4 lít khí và m gam kết tủa. Giả thiết các phản ứng xảy ra hoàn toàn. Các thể tích khí đo ở...
Đọc tiếp
Hòa tan hỗn hợp gồm FeO, Fe2O3 và F3O4 (có số mol bằng nhau) bằng dd H2SO4 20% (lượng axit lấy dư 50% so với lượng phản ứng vừa đủ), thu được dd A. Chia A thành bốn phần bằng nhau, mỗi phần có khối lượng 79,3 gam. Phần I tác dụng vừa đủ với V1 ml dung dịch KMnO4 0,05M. Phần II tác dụng vừa đủ với V2 ml dd brom 0,05M. Phần III tác dụng vừa đủ với V3 ml dd HI 0,05M. Cho Na2CO3 từ từ đến dư vào phần IV được V4 lít khí và m gam kết tủa. Giả thiết các phản ứng xảy ra hoàn toàn. Các thể tích khí đo ở đktc. Xác định các giá trị V1, V2, V3, V4.
m dd A = 4 . 79,3 = 317,2g
Qui đổi hỗn hợp FeO, Fe2O3, Fe3O4về Fe3O4 có số mol là a
Ta có 232a + (a . 4 . 1,5 . 98) : 0,2 = 317,2
=> a = 0,1 mol
Dd ban đầu
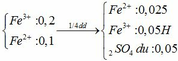
Phần 1:
8H2SO4 + 2KMnO4 + 10FeSO4 → 5Fe2(SO4)3 + 8H2O + 2MnSO4 + K2SO4
0,05 0,025
=> FeSO4 phản ứng hết
=> nKMnO4 = 0,005mol
=> V1= 0,1 lít = 100ml
Phần 2:
2Fe2+ + Br2 → 2Fe3+ + 2Br-
0,025 0,0125
=> V2 = 0,25 lít = 250ml
Phần 3:
2Fe3+ + 2I- → 2Fe2+ + I2
0,05 0,05
=> V3 = 1 lít = 1000ml
Phần 4:
Fe2+ + CO32- → FeCO3↓
0,025 0,025 0,025
2Fe3+ + 3CO32- + 3H2O → 2Fe(OH)3 + 3CO2
0,05 0,075 0,05 0,075
2H+ + CO32- →CO2 + H2O
0,1 0,05 0,05
=> nCO2 = 0,125
=> V4 = 2,8 lít
m kết tủa = mFeCO3 + mFe(OH)3 = 8,25g
Đúng 0
Bình luận (0)
Cho 5,56g hỗn hợp A gồm Fe và kim loại M ( hóa trị không đổi) . Chia A thành 2 phần bằng nhau
Phần 1 : Hòa tan hết trong dd HCl được 1,568 lít khí H2(đktc)
Phần 2 : Tác dụng vừa đủ với 2,016 lít khí Cl2 ( đktc) . Xác định kim loại M? Giúp mình vớii
Gọi: \(\left\{{}\begin{matrix}n_{Fe}=x\left(mol\right)\\n_M=y\left(mol\right)\end{matrix}\right.\) (trong 1 phần) ⇒ 56x + MM.y = 5,56:2 (1)
Giả sử M có hóa trị n không đổi.
- Phần 2: \(n_{Cl_2}=\dfrac{2,016}{22,4}=0,09\left(mol\right)\)
PT: \(2Fe+3Cl_2\underrightarrow{t^o}2FeCl_3\)
\(2M+nCl_2\underrightarrow{t^o}2MCl_n\)
Theo PT: \(n_{Cl_2}=\dfrac{3}{2}n_{Fe}+\dfrac{n}{2}n_M=\dfrac{3}{2}x+\dfrac{n}{2}y=0,09\left(2\right)\)
- Phần 1: \(n_{H_2}=\dfrac{1,568}{22,4}=0,07\left(mol\right)\)
+ TH1: M có pư với HCl.
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(2M+2nHCl\rightarrow2MCl_n+nH_2\)
Theo PT: \(n_{H_2}=n_{Fe}+\dfrac{n}{2}n_M=x+\dfrac{n}{2}y=0,07\left(3\right)\)
Từ (2) và (3) \(\Rightarrow\left\{{}\begin{matrix}x=0,04\left(mol\right)\\ny=0,06\end{matrix}\right.\)
Thay vào (1), ta được: \(M_M.y=0,54\) \(\Rightarrow\dfrac{M_M.y}{n.y}=\dfrac{0,54}{0,06}\Rightarrow M_M=9n\)
Với n = 3 thì MM = 27 (g/mol) là thỏa mãn.
→ M là Al.
+ TH2: M không pư với HCl.
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo PT: \(x=n_{Fe}=n_{H_2}=0,07\left(mol\right)\)
Thay vào (1) ta được \(M_M.y=-1,14\) (vô lý vì MM và y đều là số dương)
Vậy: M là Al.
Đúng 2
Bình luận (0)
Câu 1:cho a gam hỗn hợp X gồm hai kim loại Al và Fe, được chia làm hai phần,phần 1 gấp đôi phần 2. Phần 1 cho tác dụng hoàn toàn với b gam dung dịch Hcl 15% vừa đủ, ta thu được 9 15 gam muối. Phần 2 đem đốt cháy trong khí oxi đến khi phản ứng xảy ra hoàn toàn ta thu được 2 18gam oxi.tính giá trị của a và bCâu 2:cho 21,4 gam hỗn hợp A gồm Fe và kim loại X(có hóa trị II), tác dụng hoàn toàn với dung dịch axit clohidric ta thu được 7,84 lít khí ở đktc. Đốt cùng lượng hỗn hợp A ở trên trong khí oxi...
Đọc tiếp
Câu 1:cho a gam hỗn hợp X gồm hai kim loại Al và Fe, được chia làm hai phần,phần 1 gấp đôi phần 2. Phần 1 cho tác dụng hoàn toàn với b gam dung dịch Hcl 15% vừa đủ, ta thu được 9 15 gam muối. Phần 2 đem đốt cháy trong khí oxi đến khi phản ứng xảy ra hoàn toàn ta thu được 2 18gam oxi.tính giá trị của a và b
Câu 2:cho 21,4 gam hỗn hợp A gồm Fe và kim loại X(có hóa trị II), tác dụng hoàn toàn với dung dịch axit clohidric ta thu được 7,84 lít khí ở đktc. Đốt cùng lượng hỗn hợp A ở trên trong khí oxi phải dùng hết 4,48 lít khí oxi ở đktc
a) Xác định kim loại X
b) tính thành phần phần trăm về khối lượng các chất trong hỗn hợp A?
GIẢI CHI TIẾT DÙM EM VỚI !!!
Một loại khí clo có chứa 2 đồng vị
C
17
35
l
;
C
17
37
l
. Cho
C
l
2
tác dụng với
H
2
rồi lấy sản phẩm hoà tan vào nước thu được dung dịch X. Chia dung dịch X thành hai phần bằng nhau:- Phần thứ nhất cho tác dụng vừa đủ với 125 ml dung dịch
B...
Đọc tiếp
Một loại khí clo có chứa 2 đồng vị C 17 35 l ; C 17 37 l . Cho C l 2 tác dụng với H 2 rồi lấy sản phẩm hoà tan vào nước thu được dung dịch X. Chia dung dịch X thành hai phần bằng nhau:
- Phần thứ nhất cho tác dụng vừa đủ với 125 ml dung dịch B a ( O H ) 2 0,88M.
- Phần thứ hai cho tác dụng với A g N O 3 vừa đủ ta thu được 31,57 gam kết tủa.
Thành phần % số nguyên tử của đồng vị C 17 35 l ; C 17 37 l lần lượt là
A. 75% và 25%
B. 25% và 75%
C. 30% và 70%
D. 70% và 30%
Gọi phần trăm số nguyên tử của C 17 35 l là x, C 17 37 l là (100 – x).
Cl2 + H2 ® 2HCl (1)

M ¯ C l = 35 x + 37 ( 100 − x ) 100 ⇒ x = 75
Vậy thành phần phần trăm mỗi loại đồng vị của clo là : C 17 35 l (75% ) ; C 17 37 l (25%).
ĐÁP ÁN A
Đúng 0
Bình luận (0)
Cho m gam hỗn hợp kim loại có hóa trị không đổi thành hai phần bằng nhau. Phần I cho tác dụng hoàn toàn với dung dịch H2SO4 vừa đủ thu đượ 4,48l khí H2 (đktc) và m1 gam muối sunfat khan. Phần II cho tác dụng hoàn toàn với oxi thu được m2 gam oxit. Giá trị m1 - m2 có giá trị là
PTHH:
\(M+H_2SO_4\rightarrow M_2\left(SO_4\right)_x+H_2\left(1\right)\)
\(M+O_2\rightarrow M_2O_x\left(2\right)\)
Phần 1:
\(n_{SO_4}=n_{H_2SO_4}=n_{H_2}=0,2\left(mol\right)\)
Ta có: \(m_{M_2\left(SO_4\right)_x}=m_M+m_{SO_4}\Leftrightarrow m_1=\dfrac{m}{2}+0,2.96=\dfrac{m}{2}+19,2\left(3\right)\)
Phần 2:
Ta có: \(m_O=m_{M_2O_x}-m_M=m_2-\dfrac{m}{2}\Rightarrow n_O=\dfrac{m_2}{16}-\dfrac{m}{32}\left(mol\right)\)
Lại có: \(n_{SO_4\left(1\right)}=x.n_{M_2\left(SO_4\right)_n}=\dfrac{x}{2}.n_M=x.n_{M_2O_x}=n_{O\left(2\right)}\)
\(\Leftrightarrow0,2=\dfrac{m_2}{16}-\dfrac{m}{32}\)
\(\Leftrightarrow3,2=m_2-\dfrac{m}{2}\)
\(\Leftrightarrow m_2=\dfrac{m}{2}+3,2\left(4\right)\)
Từ \(\left(3\right)\) và \(\left(4\right)\Rightarrow m_1-m_2=16\)
Đúng 1
Bình luận (0)
Chia 43,4 gam hỗn hợp X gồm fe, zn, cu thành hai phần bằng nhau. Phần 1 tác dụng hoàn toàn với dd hcl dư thu được 4,48 lít khí h2 ( đktc ). Mặt khác, cho phần 2 phản ứng vừa đủ với 8,96 lít khí Cl2 ( đktc ). Tính khối lượng mỗi kim loại trong hỗn hợp X
Cho 16,5 gam một kim loại M hóa trị II tác dụng vừa đủ với 250ml dung dịch HCl 2M. Nguyên tử khối của kim loại M là
A. 64.
B. 65.
C. 27.
D. 24.
Giúp em với ạ:
Lọ thứ nhất đựng 150ml dd HCl 10%(D= 1,047g/ml), lọ thứ 2 đựng 250ml dd HCl 2M. Trộn 2 dd này với nhau được dd HCl mới (dd A). Nếu 40ml dd A tác dụng vừa đủ với 2,7g hỗn hợp kim loại Zn và Fe. Hãy tính CM của dd A và % về khối lượng mỗi kim loại trong hỗn hợp A
Ta có: m dd HCl (1) = 1,047.150 = 157,05 (g)
\(\Rightarrow m_{HCl\left(1\right)}=157,05.10\%=15,705\left(g\right)\Rightarrow n_{HCl\left(2\right)}=\dfrac{15,705}{36,5}=0,43\left(mol\right)\)
\(n_{HCl\left(2\right)}=0,25.2=0,5\left(mol\right)\)
\(\Rightarrow C_{M_A}=\dfrac{0,43+0,5}{0,15+0,25}=2,325M\)
Giả sử: \(\left\{{}\begin{matrix}n_{Zn}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\)
⇒ 65x + 56y = 2,7 (1)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Có: \(n_{HCl}=0,04.2,325=0,093\left(mol\right)\)
Theo PT: \(n_{HCl}=2n_{Zn}+2n_{Fe}=2x+2y\left(mol\right)\)
\(\Rightarrow2x+2y=0,093\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=\dfrac{4}{375}\left(mol\right)\\y=\dfrac{43}{1200}\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{\dfrac{4}{375}.65}{2,7}.100\%\approx25,68\%\\\%m_{Fe}\approx74,32\%\end{matrix}\right.\)
Bạn tham khảo nhé!
Đúng 1
Bình luận (0)
Một loại khí X có chứa 2 đồng vị 3517X, 3717X. Cho X2 tác dụng với H2 rồi lấy sản phẩm hoà tan vào nước thu được dung dịch Y. Chia dung dịch Y thành hai phần bằng nhau: - Phần thứ nhất cho tác dụng vừa đủ với 125 ml dung dịch Ba(OH)2 0,88M. - Phần thứ hai cho tác dụng với AgNO3 vừa đủ ta thu được 31,57 gam kết tủa. Thành phần % số nguyên tử của mỗi đồng vị là bao nhiêu? A. 35 và 65 B. 40 và 60 C. 85 và 15 D. 75 và 25
Đọc tiếp
Một loại khí X có chứa 2 đồng vị 3517X, 3717X. Cho X2 tác dụng với H2 rồi lấy sản phẩm hoà tan vào nước thu được dung dịch Y. Chia dung dịch Y thành hai phần bằng nhau:
- Phần thứ nhất cho tác dụng vừa đủ với 125 ml dung dịch Ba(OH)2 0,88M.
- Phần thứ hai cho tác dụng với AgNO3 vừa đủ ta thu được 31,57 gam kết tủa.
Thành phần % số nguyên tử của mỗi đồng vị là bao nhiêu?
A. 35 và 65
B. 40 và 60
C. 85 và 15
D. 75 và 25
Đáp án D
Gọi phần trăm số nguyên tử của X 17 35 là x, X 17 37 là (100 – x).
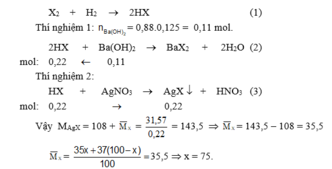
Vậy thành phần phần trăm mỗi loại đồng vị của clo là : C 17 35 l (75% ) ; C 17 37 l (25%).
Đúng 0
Bình luận (0)
















