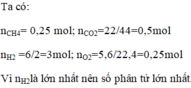Những câu hỏi liên quan
a) Tính khối lượng của : 0,5mol nguyên tử Al ; 6,72 lít khí CO2(đktc); 5,6 lít khí N2 ( ở đktc); 0,25 mol phân tử CaCO3.
b) Tính khối lượng của hỗn hợp gồm: 3,36 lít khí H2( đktc) và 5,6 lít khí N2(đktc); 0,2 mol CO2.
a.
\(m_{Al}=0.5\cdot27=13.5\left(g\right)\)
\(m_{CO_2}=\dfrac{6.72}{22.4}\cdot44=13.2\left(g\right)\)
\(m_{N_2}=\dfrac{5.6}{22.4}\cdot28=7\left(g\right)\)
\(m_{CaCO_3}=0.25\cdot100=25\left(g\right)\)
b.
\(m_{hh}=\dfrac{3.36}{22.4}\cdot2+\dfrac{5.6}{22.4}\cdot28+0.2\cdot44=16.1\left(g\right)\)
Đúng 3
Bình luận (1)
Câu 5: Thể tích của hỗn hợp khí X gồm: 0,1 mol CO2; 0,2 mol H2 và 0,7 mol O2 ở điều kiện tiêu chuẩn là:A. 15,68 lít. B. 3,36 lít. C. 22,4 lít. D. 6,72 lít.Câu 6: Lượng chất có chứa N (6.1023) nguyên tử hoặc phân tử chất đó được gọi là:A. mol. B. khối lượng mol. C. thể tích mol D. tỉ khối.Câu 7: Cho sơ đồ phản ưng: Fe2O3 + HCl 4 FeCl3 + H2O. Để hòa tan hoàn toàn 8 gam sắt (III) oxit Fe2O3 cần dùng bao nhiêu gam axit clohiđric.A. 3,65 g. B. 4,475. C. 10,65. D. 10,95.Câu 8: Nguyên tử khối của cacbo...
Đọc tiếp
Câu 5: Thể tích của hỗn hợp khí X gồm: 0,1 mol CO2; 0,2 mol H2 và 0,7 mol O2 ở điều kiện tiêu chuẩn là:
A. 15,68 lít. B. 3,36 lít. C. 22,4 lít. D. 6,72 lít.
Câu 6: Lượng chất có chứa N (6.1023) nguyên tử hoặc phân tử chất đó được gọi là:
A. mol. B. khối lượng mol. C. thể tích mol D. tỉ khối.
Câu 7: Cho sơ đồ phản ưng: Fe2O3 + HCl 4 FeCl3 + H2O. Để hòa tan hoàn toàn 8 gam sắt (III) oxit Fe2O3 cần dùng bao nhiêu gam axit clohiđric.
A. 3,65 g. B. 4,475. C. 10,65. D. 10,95.
Câu 8: Nguyên tử khối của cacbon bằng 3/4 nguyên tử khối của oxi. Biết nguyên tử khối của cacbon là 12 đvC, suy ra nguyên tử khối của oxi là
A. 12 đvC. B. 14 đvC. C. 16 đvC. D. 32 đvC.
Câu 9: Trong 1 mol nước chứa số nguyên tử H là
A. 6.1023. B. 12.1023. C. 18.1023. D. 24.1023.
Câu 10: Trong 1,8 mol CH4 có tất cả bao nhiêu phân tử CH4?
A. 6.1023 . B. 1,08.10-23 . C. 1,08.1023 D. 1,08.1024.
Câu 11: Khối lượng mol của hợp chất Ca(H2PO4)2 là:
A. 234 g/mol. B. 170 g.mol. C. 137 g.mol. D. 88 g/mol
Câu 12: Một hợp chất có chứa 50% S còn lại là O. Tỉ lệ số mol nguyên tử tối giản nhất của S và O là:
A. 1:1 B. 2:1. C. 1:2. D. 2:
Câu `5`:
`V_(CO2) = n . 22,4 = 0,1 . 22,4 =2,24 ` (l)
`V_(H_2) = n.22,4 = 0,2 . 22,4=4,48 `( l)
`V_(O_2) = n . 22,4 = 0,7 . 22,4 =15,68` (l)
`=> V_X= 2,24 + 4,48 + 15,68 = 22,4`(l)
`->`Chọn `C`
Câu `6: A `
Câu `7`:
Cân bằng PT: `Fe_2O_3 + 6HCl -> 2FeCl_3 + 3H_2O`
`n_(Fe_2O_3)= 8/(2.56 + 3.16) = 0,05` (mol)
`n_(HCl) = ( 0,05 .6)/1 = 0,3 ` (mol)
`m_(HCl) = 0,3 . (1 + 35,5) = 10,95` (g)
`->` Chọn `D`
Câu `8`:
Nguyên tử khối của oxi `= 12 : 3/4 =16` ( đvC)
`->` Chọn `C`
Câu `9`: `A`
Câu `11`: `=40+ 2( 2.1 + 31 + 4.16) =234` (g)
`->` Chọn `A`
Câu `12`:`C`
Đúng 0
Bình luận (0)
Tính khối lượng của hỗn hợp gồm:
a) N phân tử oxi; 2N phân tử nitơ và 1,5N phân tử CO2.
b) 0,1 mol Fe; 0,2 mol Cu; 0,3 mol Zn; 0,25 mol Al.
Hóa 8 :<
Help
khối lượng của N phân tử oxi chính là khối lượng của 1 mol oxi, ta có:
\(m_{O_2}=16.1=16\left(g\right)\)
tương tự với \(N_2\) và \(CO_2\)ta có:
\(m_{N_2}=28.2=56\left(g\right)\)
\(m_{CO_2}=44.1,5=66\left(g\right)\)
khối lượng của hỗn hợp là:
\(m_{hh}=m_{O_2}+m_{N_2}+m_{CO_2}=16+56+66=138\left(g\right)\)
Tính Khối Lượng Của: a. 0,25 mol CaSO4 b. 3.1023 phân tử Cu2O c. 6,72 lít khí NH3d. 0,17 mol C4H10 e. 4,5.1025 phân tử Cu(OH)2g. 0,48 mol MgO h. 3,36 lít khí CO2 ( đktc ) i. 0,25 mol Al(OH)3k. 16,8 lít khí C4H8 (đktc)l. 0,9.1024 phân tử O2 m. 2,8 lít khí H2 ( đktc )
Đọc tiếp
Tính Khối Lượng Của:
a. 0,25 mol CaSO4
b. 3.1023 phân tử Cu2O
c. 6,72 lít khí NH3
d. 0,17 mol C4H10
e. 4,5.1025 phân tử Cu(OH)2
g. 0,48 mol MgO
h. 3,36 lít khí CO2 ( đktc )
i. 0,25 mol Al(OH)3
k. 16,8 lít khí C4H8 (đktc)
l. 0,9.1024 phân tử O2
m. 2,8 lít khí H2 ( đktc )
Tính Khối Lượng Của: a. 0,25 mol CaSO4 b. 3.1023 phân tử Cu2O c. 6,72 lít khí NH3d. 0,17 mol C4H10 e. 4,5.1025 phân tử Cu(OH)2g. 0,48 mol MgO h. 3,36 lít khí CO2 ( đktc ) i. 0,25 mol Al(OH)3k. 16,8 lít khí C4H8 (đktc)l. 0,9.1024 phân tử O2 m. 2,8 lít khí H2 ( đktc )
Đọc tiếp
Tính Khối Lượng Của:
a. 0,25 mol CaSO4
b. 3.1023 phân tử Cu2O
c. 6,72 lít khí NH3
d. 0,17 mol C4H10
e. 4,5.1025 phân tử Cu(OH)2
g. 0,48 mol MgO
h. 3,36 lít khí CO2 ( đktc )
i. 0,25 mol Al(OH)3
k. 16,8 lít khí C4H8 (đktc)
l. 0,9.1024 phân tử O2
m. 2,8 lít khí H2 ( đktc )
\(a,m_{CaSO_4}=136.0,25=34\left(g\right)\\ b,n_{Cu_2O}=\dfrac{3.10^{23}}{6.10^{23}}=0,5\left(mol\right)\\ m_{Cu_2O}=0,5.144=72\left(g\right)\\ c,n_{NH_3}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ m_{NH_3}=17.0,3=5,1\left(g\right)\\ d,m_{C_4H_{10}}=0,17.58=9,86\left(g\right)\\ e,n_{Cu\left(OH\right)_2}=\dfrac{4,5.10^{25}}{6.10^{23}}=75\left(mol\right)\\ m_{Cu\left(OH\right)_2}=98.75=7350\left(g\right)\\ g,m_{MgO}=0,48.40=19,2\left(g\right)\\ h,n_{CO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ m_{CO_2}=44.0,15=6,6\left(g\right)\\ i,m_{Al\left(OH\right)_3}=78.0,25=19,5\left(g\right)\\\)
Các câu còn lại em làm tương tự nha!
Đúng 1
Bình luận (1)
Cho hỗn hợp gồm 1,5 mol
O
2
; 2,5 mol
N
2
; 0,5 mol
C
O
2
và 0,5 mol
S
O
2
. Cho các khí sau:
C
H
4
(0,25 mol),
H
2
(6 gam),
C
O
2
(22 gam) và
O
2
(5,6 lít ở đktc). Hãy...
Đọc tiếp
Cho hỗn hợp gồm 1,5 mol O 2 ; 2,5 mol N 2 ; 0,5 mol C O 2 và 0,5 mol S O 2 . Cho các khí sau: C H 4 (0,25 mol), H 2 (6 gam), C O 2 (22 gam) và O 2 (5,6 lít ở đktc). Hãy xác định chất có số phân tử lớn nhất.
Các bạn giúp mình với, mình cần gấp lắmBài 1: Tính khối lượng của:a, 0,25 mol FeSO4? b, 13,2.1023 phân tử FeSO4? c, 8, 96 lít khí NO2 (đktc) d, Hỗn hợp chất rắn A gồm : 0,22 mol AL và 0,25 mol Cu?e, Hỗn hợp khí B gồm : 11,2 lít O2 và 13,44 lít N2 (đktc)g, Hỗn hợp C : 0,25 mol Cu, 15.1023 nguyên tử Fe?h, Hỗn hợp D : 0,25 mol O2, 11,2 lita CO2 VÀ 2,7.1023 phân tử N2?
Đọc tiếp
Các bạn giúp mình với, mình cần gấp lắm
Bài 1: Tính khối lượng của:
a, 0,25 mol FeSO4? b, 13,2.1023 phân tử FeSO4? c, 8, 96 lít khí NO2 (đktc)
d, Hỗn hợp chất rắn A gồm : 0,22 mol AL và 0,25 mol Cu?
e, Hỗn hợp khí B gồm : 11,2 lít O2 và 13,44 lít N2 (đktc)
g, Hỗn hợp C : 0,25 mol Cu, 15.1023 nguyên tử Fe?
h, Hỗn hợp D : 0,25 mol O2, 11,2 lita CO2 VÀ 2,7.1023 phân tử N2?
a) mFeSO4= 0,25.152=38(g)
b) mFeSO4= \(\dfrac{13,2.10^{23}}{6.10^{23}}.152=334,4\left(g\right)\)
c) mNO2= \(\dfrac{8,96}{22,4}.46=18,4\left(g\right)\)
d) mA= 27.0,22+64.0,25=21,94(g)
e) mB= \(\dfrac{11,2}{22,4}.32+\dfrac{13,44}{22,4}.28=32,8\left(g\right)\)
g) mC= \(64.0,25+\dfrac{15.10^{23}}{6.10^{23}}.56=156\left(g\right)\)
h) mD= \(0,25.32+\dfrac{11,2}{22,4}.44+\dfrac{2,7.10^{23}}{6.10^{23}}.28=42,6\left(g\right)\)
hơi muộn nha<3![]()
Đúng 0
Bình luận (0)
GIÚP MINH ZF18: Tính số mol của: a. 75,24 gam Al2(SO4)3 b. 15,68 lít O2 (đkc) c. 13,2.1023 phân tử H2SO4d. hỗn hợp X ( 11,2 gam Fe và 3,24 gam Al) e. Hỗn hợp Y ( 8,94 lít O2 và 2,24 lít H2)
Đọc tiếp
GIÚP MINH Z![]()
F18: Tính số mol của:
a. 75,24 gam Al2(SO4)3
b. 15,68 lít O2 (đkc)
c. 13,2.1023 phân tử H2SO4
d. hỗn hợp X ( 11,2 gam Fe và 3,24 gam Al)
e. Hỗn hợp Y ( 8,94 lít O2 và 2,24 lít H2)
a)
$n_{Al_2(SO_4)_3} = \dfrac{75,24}{27.2 + 32.3 + 16.12} = 0,22(mol)$
b)
$n_{O_2} = \dfrac{15,68}{22,4} = 0,7(mol)$
c)
$n_{H_2SO_4} = \dfrac{13,2.10^{23}}{6.10^{23}} = 2,2(mol)$
d)
$n_{Fe} = \dfrac{11,2}{56} = 0,2(mol)$
$n_{Al} = \dfrac{3,24}{27} = 0,12(mol)$
$n_{X} = 0,2 + 0,12 = 0,32(mol)$
e)
$n_{O_2} = \dfrac{8,94}{22,4} = 0,4(mol)$
$n_{H_2} = \dfrac{2,24}{22,4} = 0,1(mol)$
$n_Y = 0,4 + 0,1 = 0,5(mol)$
Đúng 4
Bình luận (1)
a) nAl2(SO4)3= mAl2(SO4)3/M(Al2(SO4)3)= 75,24/342=0,22(mol)
b) nO2=V(O2,đktc)/22,4=15,68/22,4=0,7(mol)
c) nH2SO4=N/6.1023= (13,2.1023)/(6.1023)= 2,2(mol)
d) nX có:
Số mol Fe: nFe= mFe/M(Fe)=11,2/56=0,2(mol)
Số mol Al: nAl=mAl/M(Al)=3,24/27=0,12(mol)
e) nY có:
Số mol O2: nO2=V(O2,đktc)/22,4=8,94/22,4=447/1120(mol)
Số mol H2: nH2=V(H2,đktc)/22,4=2,24/22,4=0,1(mol
Đúng 1
Bình luận (0)
Bài 4. Tính thể tích (đo ở đktc) của: a) 0,5 mol SO2 b) 3,2 g CH4 c) 0,9.1023 phân tử khí N2
Bài 5. Tính khối lượng của: a) 0,1 mol Al b) 0,3 mol Cu(NO3)2 ; c) 1,2.1023 phân tử Na2CO3 d) 8,96 lít CO2 (đktc) ; e) Mỗi nguyên tố có trong 0,5 mol K2CO3
cứu mình cần gấp
4.
a) \(V_{SO_2}=0.5\cdot22.4=11.2\left(l\right)\)
b) \(V_{CH_4}=\dfrac{3.2}{16}\cdot22.4=4.48\left(l\right)\)
c) \(V_{N_2}=\dfrac{0.9\cdot10^{23}}{6\cdot10^{23}}\cdot22.4=3.36\left(l\right)\)
5.
a) \(m_{Al}=0.1\cdot27=2.7\left(g\right)\)
b) \(m_{Cu\left(NO_3\right)_2}=0.3\cdot188=56.4\left(g\right)\)
c) \(m_{Na_2CO_3}=\dfrac{1.2\cdot10^{23}}{6\cdot10^{23}}\cdot106=21.2\left(g\right)\)
d) \(m_{CO_2}=\dfrac{8.96}{22.4}\cdot44=17.6\left(g\right)\)
e) \(m_K=0.5\cdot2\cdot39=39\left(g\right)\\ m_C=0.5\cdot12=6\left(g\right)\\ m_O=0.5\cdot3\cdot16=24\left(g\right)\)
Đúng 2
Bình luận (1)