Số hidrocacbon ở thể khí (đktc) tác dụng được với dd AgNO3 trong NH3 là
A. 2
B. 4
C. 3
D. 5
Số hiđrocacbon ở thể khí (đktc) tác dụng được với dd AgNO3 trong NH3 là
A. 2
B. 4
C. 3
D. 5
Số hiđrocacbon ở thể khí (đktc) tác dụng được với dung dịch A g N O 3 trong N H 3 là:
A. 2.
B. 4.
C. 3.
D. 5.
Chọn đáp án D.
Các hiđrocacbon ở thể khí, phản ứng được với dung dịch A g N O 3 là những hiđrocacbon có số nguyên tử C nhỏ hơn hoặc bằng 4 và có liên kết ba ở đầu mạch. Có 5 hiđrocacbon thỏa mãn điều kiện là:
C H ≡ C H , C H ≡ C − C H 3 , C H ≡ C − C H 2 − C H 3 , C H ≡ C − C H = C H 2 , C H ≡ C − C ≡ C H
Số hiđrocacbon (thể khí ở đktc) tác dụng được với dung dịch AgNO3 trong NH3 là
A. 2
B. 4.
C. 3.
D. 5.
Số hiđrocacbon ở thể khí (đktc) tác dụng được với lượng dư dung dịch AgNO3 trong NH3 là
A. 2
B. 4
C. 3
D. 5
Cho 200g dd NaOH .10% tác dụng với 100g dd NH4Cl thu được khí NH3 và dd A. a,Tính thể tích khí NH3 ở đktc,
b,C% ddA
a)
$NH_4Cl+ NaOH \to NH_3 + H_2O$
$n_{NH_3} = n_{NaOH} = \dfrac{200.10\%}{40} = 0,5(mol)$
$V_{NH_3} = 0,5.22,4 = 11,2(lít)$
b)
Sau phản ứng :
$m_{dd} = 200 + 100 - 0,5.17 = 291,5(gam)$
$n_{NaCl} = n_{NaOH} = 0,5(mol)$
$C\%_{NaCl} = \dfrac{0,5.58,5}{291,5}.100\% = 10,03\%$
Đốt cháy hidrocacbon mạch hở X (ở thể khí trong điều kiện thường) thu được số mol CO2 gấp 2 lần số mol H2O. Mặt khác 0,1 mol X tác dụng với dung dịch AgNO3 trong NH3 (dư) thu được 15,9 gam kết tủa vàng. Công thức cấu tạo của X là:
![]()
![]()
![]()
![]()
Đáp án C
Gọi hidrocacbon là CxHy
Quá trình cháy:
![]()
![]() suy ra x = y
suy ra x = y
Mkết tủa = 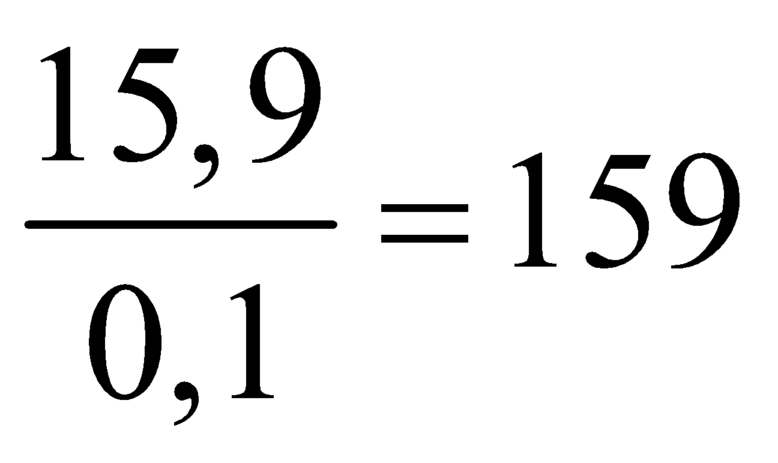 , Mhidrocacbon = 52
, Mhidrocacbon = 52
Suy ra hidrocacbon đó là C4H4
1. Dẫn 0,56l hh khí gồm axetilen và etilen qua dd AgNO3/NH3 dư thu dược 1,2g kết tủa vàng. Thể tích etilen trong hh
2. Cho 8,96l hh gồm etan,propin qua bình chứa dd AgNO3 trong NH3 dư thu được 22,05g kết tủa vàng. Tp % theo thể tích cua etan trong hh
3. Ch 8,4g but-1-en tác dụng hết với dd Br2 dư. Tính kl sp thu đựơc
4. Khi đốt cháy 1 hidrocacbon X thu được CO2 và H2O với tỉ lệ số mol là nNO2 : nH2O = 2:1 X là hidrocacbon nào
Cảm ơn
Do chỉ có axetilen tác dụng với AgNO3/NH3 tạo kết tủa C2Ag2 suy ra số mol axetilen trong hỗn hợp là: \(\dfrac{1,2}{108.2+12.2}\)= 0,005 (mol)
V etilen: 0,005.22,4 = 0,112 (l)
nhỗn hợp là: \(\dfrac{8,96}{22,4}\) = 0,4 (mol)
Do chỉ có propin tác dụng với AgNO3/NH3 tạo thành CAg(nối ba)C-CH3
npropin = 22,05 : (12.3 + 3 + 108) = 0,15 (mol)
Vpropin là : 0,15 : 0,4 = 37,5%
Vetan là: 100% - 37,5% = 62,5%
4. Do nCO2 > nH2O nên hidrocacbon đó là ankin
Đặt công thức CnH2n-2 → nCO2 + n-1H2O
Ta có \(\dfrac{n}{n-1}\) = \(\dfrac{2}{1}\) suy ra n là: 2
Ankin đó là C2H2
Cho m gam hỗn hợp X gồm CH3CH,COOH, HO-CH2-CHO. Nếu cho m gam X tác dụng với dd AgNO3/NH3 dư thì được 32,4 gam kết tủa. Còn nếu cho m gam X tác dụng với Na dư sẽ được 2,24 lít khí ở đktc. Giá trị của m là?
cho 16,8l khí h2 tác dụng với 14,56l khí cl2 ở điều kiện thích hợp. sản phẩm sinh ra hòa tan trong nước được dd D. lấy 1/10 dd D cho tác dụng với agno3 dư thì thu được 17,22g kết tủa trắng. tiinhs hiệu xuất phản ứng tổng hợp ban đầu, biết các chất khí đó ở đktc
H2 + Cl2 ---> 2HCl (khí) (1)
nH2 = \(\frac{16,8}{22,4}\) = 0,75 (mol)
nCl2 = \(\frac{14,56}{22,4}\) = 0,65 (mol)
So sánh: \(\frac{nH2}{1}\) > \(\frac{nCL2}{1}\)
=> H2 dư sau phản ứng, chọn nCl2 để tính
Theo PTHH: nHCl = 2.nCl2 = 2. 0,65 = 1,3 (mol)
Khi hòa tan hỗn hợp khí gồm khí HCl và H2 dư vào H2O, thu được dd D là dd HCl
Khi cho dd HCl vào AgNO3 dư thì:
HCl + AgNO3 ----> AgCl + HNO3 (2)
Vì HNO3 dư nên tính theo nHCl
nHCl = \(\frac{1}{10}\).1,3 = 0,13 (mol)
Theo PTHH (2) nAgCl (lí thuyết) = nHCl = 0,13 (mol)
=> mAgCl (lí thuyết) = 0,13 . 143,5 = 18,655 (g)
Hiệu suất phản ứng:
H = \(\frac{17,22.100}{18,655}\) = 92,31 %