Biết rằng tính phi kim giảm dần theo thứ tự F, O, Cl, N. Trong các phân tử sau, phân tử nào có liên kết phân cực mạnh nhất.
A. F2O
B. Cl2O
C. NCl3
D. NF3
Biết rằng tính phi kim giảm dần theo thứ tự : F, O, N, Cl. Phân tử có liên kết phân cực nhất là phân tử nào sau đây ?
A. F 2 O B. Cl 2 O
C. ClF D. N Cl 3
a) Dựa vào giá trị độ âm điện ( F: 3,98 ; O: 3,44 ; Cl: 3,16 ; N: 3,04) hãy xét xem tính phi kim thay đổi như thế nào của dãy nguyên tố sau: F, O, N, Cl.
b) Viết công thức cấu tạo của các phân tử sau đây:
N2, CH4, H2O, NH3
Xét xem phân tử nào có liên kết không phân cực, liên kết phân cực mạnh nhất.
F O Cl N
Độ âm điện: 3,98 3,44 3,16 3,14
Nhận xét: tính phi kim giảm dần.
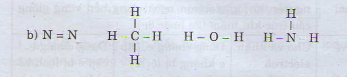
N2 CH4 H2O NH3
Hiệu độ âm điện: 0 0,35 1,24 0,84
Phân tử N2, CH4 có liên kết cộng hóa trị không phân cực. Phân tử H2O có liên kết cộng hóa trị phân cực mạnh nhất trong dãy.
a) Dựa vào giá trị độ âm điện ( F: 3,98 ; O: 3,44 ; Cl: 3,16 ; N: 3,04) hãy xét xem tính phi kim thay đổi như thế nào của dãy nguyên tố sau: F, O, N, Cl.
b) Viết công thức cấu tạo của các phân tử sau đây:
N2, CH4, H2O, NH3
Xét xem phân tử nào có liên kết không phân cực, liên kết phân cực mạnh nhất.
F O Cl N
Độ âm điện: 3,98 3,44 3,16 3,14
Nhận xét: tính phi kim giảm dần.
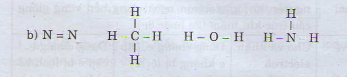
N2 CH4 H2O NH3
Hiệu độ âm điện: 0 0,35 1,24 0,84
Phân tử N2, CH4 có liên kết cộng hóa trị không phân cực. Phân tử H2O có liên kết cộng hóa trị phân cực mạnh nhất trong dãy.
a) Dựa vào giá trị độ âm điện ( F: 3,98 ; O: 3,44 ; Cl: 3,16 ; N: 3,04) hãy xét xem tính phi kim thay đổi như thế nào của dãy nguyên tố sau: F, O, N, Cl.
b) Viết công thức cấu tạo của các phân tử sau đây:
N2, CH4, H2O, NH3
Xét xem phân tử nào có liên kết không phân cực, liên kết phân cực mạnh nhất.
F O Cl N
Độ âm điện: 3,98 3,44 3,16 3,14
Nhận xét: tính phi kim giảm dần.
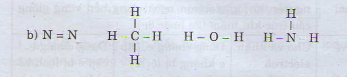
N2 CH4 H2O NH3
Hiệu độ âm điện: 0 0,35 1,24 0,84
Phân tử N2, CH4 có liên kết cộng hóa trị không phân cực. Phân tử H2O có liên kết cộng hóa trị phân cực mạnh nhất trong dãy.
a. Dựa vào giá trị độ âm điện (F : 3,98, O : 3,44, Cl : 3,16, N : 3,04) hãy xét xem tính phi kim thay đổi như thế nào trong dãy nguyên tố sau: F, O, Cl, N.
b. Viết công thức cấu tạo của các phân tử sau đây: N2, CH4, H2O, NH3.
Xét xem phân tử nào có liên kết cộng hóa trị không phân cực, liên kết cộng hóa trị phân cực mạnh nhất.
Tham khảo
a)
| F | O | Cl | N | |
| Độ âm điện | 3,98 | 3,44 | 3,16 | 3,04 |
Tính phi kim giảm dần
b)
| N2 | CH4 | H2O | NH3 | |
| Hiệu độ âm điện | 0 | 0,35 | 1,24 | 0,84 |
Phân tử N2, CH4 có liên kết cộng hóa trị không phân cực. Phân tử H2O có liên kết cộng hóa trị phân cực mạnh nhất trong dãy.
Mức độ phân cực của liên kết hóa học trong các phân tử được sắp xếp theo thứ tự giảm dần từ trái sang phải là:
A. HI, HBr, HCl
B. HI, HCl, HBr
C. HCl, HI, HBr
D. HCl, HBr, HI
Đáp án : A
Vì Từ Cl -> Br -> I thì bán kính tăng rất nhanh trong khi độ âm điện lại giảm chậm
=> Độ phân cực H-X nhìn chung là tăng
Mức độ phân cực của liên kết hoá học trong các phân tử được sắp xếp theo thứ tự giảm dần từ trái sang phải là:
A. HI, HBr, HCl
B. HI, HCl, HBr
C. HCl, HBr, HI
D. HBr, HI, HCl
Đáp án C
Vì từ Cl → Br → I thì bán kính tăng rất nhanh trong khi độ âm điện lại giảm chậm
⇒ Độ phân cực H-X nhìn chung là tăng
Mức độ phân cực của liên kết hoá học trong các phân tử được sắp xếp theo thứ tự giảm dần từ trái sang phải là
A. HCl, HBr, HI
B. HI, HBr, HCl
C. HI, HCl, HBr
D. HBr, HI, HCl
Đáp án A
HCl, HBr, HI.
Để đánh giá độ phân cực của liên kết giữa hai nguyên tử, người ta dựa vào hiệu độ âm điện của chúng. Hiệu độ âm điện càng lớn thì liên kết càng phân cực và ngược lại.
Trong nhóm VIIA, đi từ Cl đến I thì độ âm điện giảm dần. Suy ra độ phân cực của liên kết trong các hợp chất HCl, HBr, HI giảm dần.
Mức độ phân cực của liên kết hoá học trong các phân tử được sắp xếp theo thứ tự giảm dần từ trái sang phải là :
A. HCl, HBr, HI.
B. HI, HBr, HCl.
C. HI, HCl, HBr.
D. HBr, HI, HCl.