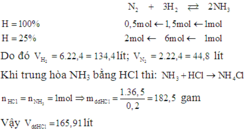Tính thể tích khí N2 và khí H2 (đktc) cần dùng để điều chế được 17 gam NH3. Biết hiệu suất phản ứng là 25%.

Những câu hỏi liên quan
Phải dùng bao nhiêu lít khí nitơ để điều chế 17 gam NH3 biết hiệu suất phản ứng là 25%, các thể tích đo ở đktc.
A. 44,8 lít
B. 22,4 lít
C. 1,12 lít
D. 4,48 lít
Đáp án A
N2+ 3H2![]() 2NH3
2NH3
nNH3= 1mol
Theo PTHH: nN2 (PT)= ½.nNH3= 0,5 mol;
nH2 (PT)= 3/2. nNH3=1,5 mol
Công thức tính hiệu suất:
H = n N 2 ( PT ) n N 2 ( thucte ) . 100 % , H = n H 2 ( PT ) n H 2 ( thucte ) . 100 % → n N 2 ( thucte ) = 2 mol ; n H 2 ( thucte ) = 6 mol → V N 2 ( thucte ) = 44 . 8
Đúng 0
Bình luận (0)
Phải dùng bao nhiêu lít khí nitơ và bao nhiêu lít khí hidro để điều chế 17 gam NH3, biết rằng hiệu suất chuyển hóa thành amoniac là 25%. Các thể tích khí đo được ở đktc.
A. 44,8 lít N2 và 13,44 lít H2.
B. 22,4 lít N2 và 134,4 lít H2.
C. 22,4 lít N2 và 67,2 lít H2.
D. 44,8 lít N2 và 67,2 lít H2.
$n_{NH_3} = \dfrac{17}{17} = 1(mol)$
$N_2 + 3H_2 \xrightarrow{t^o} 2NH_3$
Theo PTHH :
$n_{N_2\ pư} = \dfrac{1}{2}n_{NH_3} = 0,5(mol)$
$n_{H_2\ pư} = \dfrac{3}{2}n_{NH_3} = 1,5(mol)$
Suy ra :
$n_{N_2\ đã\ dùng} = \dfrac{0,5}{25\%} = 2(mol)$
$n_{H_2\ đã\ dùng} = \dfrac{1,5}{25\%} = 6(mol)$
Vậy :
$V_{N_2} = 2.22,4 = 44,8(lít)$
$V_{H_2} = 6.22,4 = 134,4(lít)$
Đúng 1
Bình luận (0)
Cần lấy bao nhiêu lít N2 và H2 để điều chế được 4,48 lít NH3, biết hiệu suất phản ứng là 20%. Các khí được đo ở đktc
PTHH:3H2+N2=2NH3
nNH3=0,2(mol) suy ra nH2=0,3(mol);nN2=0,1(mol)
suy ra V H2=6,72(l);V N2=2,24(l)
mà hiệu suất phản ứng chỉ có 20 phần trăm
suy ra V H2 cần dùng để điều chế 4,48 lít NH3 là:6,72x100:20=3,36(l)
V N2 cần dùng để điều chế 4,48 lít NH3 là:2,24x100:20=11,2(l)
Đúng 0
Bình luận (0)
Cần lấy bao nhiêu lít khí
N
2
và
H
2
để điều chế được 67,2 lít khí amoniac ? Biết rằng thể tích của các khí được đo trong cùng điều kiện nhiệt độ, áp suất và hiệu suất của phản ứng là 25%. A. 33,6 lít
N
2
và 100,8 lít
H
2
.
B. 8,4 lít
N...
Đọc tiếp
Cần lấy bao nhiêu lít khí N 2 và H 2 để điều chế được 67,2 lít khí amoniac ? Biết rằng thể tích của các khí được đo trong cùng điều kiện nhiệt độ, áp suất và hiệu suất của phản ứng là 25%.
A. 33,6 lít N 2 và 100,8 lít H 2 .
B. 8,4 lít N 2 và 25,2 lít H 2 .
C. 268,8 lít N 2 và 806,4 lít H 2 .
D. 134,4 lít N 2 và 403,2 lít H 2 .
Chọn D
Ở cùng điều kiện nhiệt độ và áp suất, tỉ lệ về thể tích cũng là tỉ lệ về số mol.
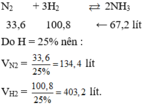
Đúng 0
Bình luận (0)
Phải dùng bao nhiêu lít khí nitơ và bao nhiêu lít khí hiđro để điều chế 17,00 gram NH3. Biết rằng hiệu suất chuyển hoá thành amoniac là 25%. Các thể tích khí được đo ở đktc. A. 44,8 lit N2 và 134,4 lit H2 B. 22,4 lit N2 và 134,4 lit H2 C. 22,4 lit N2 và 67,2 lit H2 D. 44,8 lit N2 và 67,2 lit H2
Đọc tiếp
Phải dùng bao nhiêu lít khí nitơ và bao nhiêu lít khí hiđro để điều chế 17,00 gram NH3. Biết rằng hiệu suất chuyển hoá thành amoniac là 25%. Các thể tích khí được đo ở đktc.
A. 44,8 lit N2 và 134,4 lit H2
B. 22,4 lit N2 và 134,4 lit H2
C. 22,4 lit N2 và 67,2 lit H2
D. 44,8 lit N2 và 67,2 lit H2
- Đáp án A
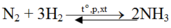
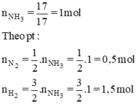
Do hiệu suất 25% nên
nN2cần dùng = 2( mol) và nH2cần dùng = 6(mol).
⇒VN2 = 2. 22,4 = 44,8 (lit) và VH2 = 22,4. 6= 134,4 (lit).
Đúng 1
Bình luận (0)
Cho 17,5 lít H2 và 5 lít N2 vào 1 bình phản ứng. Sau phản ứng thu được hỗn hợp khí A gồm N2 H2 NH3( các thể tích khí đo trong cùng điều kiện nhiệt dộ và áp suất ) biết dA/h2=5 . Tính hiệu suất tổng hợp NH3 và thể tích NH3 thu được sau phản ứng.
Xem chi tiết
Cho 17,5 lít H2 và 5 lít N2 vào một bình phản ứng. Sau phản ứng thu được hỗn hợp khí A gồm NH3, N2 và H2 (các thể tích khí đo trong cùng điều kiện nhiệt độ và áp suất). Biết dA/H2 = 5. Tính hiệu suất tổng hợp NH3 và thể tích khí NH3 thu được sau phản ứng.
\(M_A=5.2=10\left(g/mol\right)\)
Do các khí đo ở cùng điều kiện nhiệt độ và áp suất nên tỉ lệ thể tích cũng là tỉ lệ mol
Chọn \(\left\{{}\begin{matrix}n_{H_2}=17,5\left(mol\right)\\n_{N_2}=5\left(mol\right)\end{matrix}\right.\)
Gọi \(n_{N_2\left(p\text{ư}\right)}=a\left(mol\right)\left(0< a< 5\right)\)
PTHH: \(N_2+3H_2\xrightarrow[]{t^o,p,xt}2NH_3\)
a---->3a---------->2a
Xét tỉ lệ: \(5< \dfrac{17,5}{3}\Rightarrow\) Hiệu suất phản ứng tính theo N2
Ta có: \(n_A=5+17,5+2a-a-3a=22,5-2a\left(mol\right)\)
Theo ĐLBTKL: \(m_A=5.28+17,5.2=175\left(g\right)\)
\(\Rightarrow M_A=\dfrac{175}{22,5-2a}=10\Leftrightarrow a=2,5\left(TM\right)\)
\(\Rightarrow H=\dfrac{2,5}{5}.100\%=50\%\)
Đúng 1
Bình luận (0)
Phải dùng bao nhiêu lít N2 và H2 (đktc) để điều chế 17 gam NH3. Biết hiệu suất chuyển hoán thành NH3 là 25%. Nếu dùng dung dịch HCl 20% (d 1,1g/ml) để trung hòa lượng NH3 trên thì cần bao nhiêu ml? A. 165,91 lít B. 163 lít C. 175,91 lít D. 153 lít
Đọc tiếp
Phải dùng bao nhiêu lít N2 và H2 (đktc) để điều chế 17 gam NH3. Biết hiệu suất chuyển hoán thành NH3 là 25%. Nếu dùng dung dịch HCl 20% (d = 1,1g/ml) để trung hòa lượng NH3 trên thì cần bao nhiêu ml?
A. 165,91 lít
B. 163 lít
C. 175,91 lít
D. 153 lít
1. Cho 17,5 lít H2 và 5 lít N2 vào một bình phản ứng. Sau phản ứng thu được hỗn hợp khí A gồm NH3, N2 và H2 ( các thể tích khí đo trong cùng điều kiện nhiệt độ và áp suất). Biết dA/H2 5 Tính hiệu suất tổng hợp NH3 và thể tích khí NH3 thu được sau phản ứng.2. Cho m gam hỗn hợp 2 kim loại Mg và Al có số mol bằng nhau phản ứng hoàn toàn với lượng oxi dư. Kết thúc phản ứng thu được hỗn hợp chất rắn có khối lượng tăng so với hỗn hợp ban đầu là 2 g. Tín
Đọc tiếp
1. Cho 17,5 lít H2 và 5 lít N2 vào một bình phản ứng. Sau phản ứng thu được hỗn hợp khí A gồm NH3, N2 và H2 ( các thể tích khí đo trong cùng điều kiện nhiệt độ và áp suất). Biết dA/H2 = 5 Tính hiệu suất tổng hợp NH3 và thể tích khí NH3 thu được sau phản ứng.
2. Cho m gam hỗn hợp 2 kim loại Mg và Al có số mol bằng nhau phản ứng hoàn toàn với lượng oxi dư. Kết thúc phản ứng thu được hỗn hợp chất rắn có khối lượng tăng so với hỗn hợp ban đầu là 2 g. Tín