Trình bày phương pháp hoá học để phân biệt các dung dịch: NH3, Na2SO4, NH4Cl, (NH4)2SO4. Viết phương trình hoá học của các phản ứng đã dùng.

Những câu hỏi liên quan
Trình bày phương pháp hóa học để phân biệt các dung dịch : NH3, Na2SO4, NH4Cl, (NH4)2SO4. Viết phương trình hóa học của các phản ứng đã dùng.
Trích mẫu thử
Cho dung dịch $Ba(OH)_2$ vào :
- mẫu thử tạo khí mùi khai là $NH_4Cl$
$2NH_4Cl + Ba(OH)_2 \to 2NH_3 + BaCl_2 + 2H_2O$
- mẫu thử tạo khí mùi khai và kết tủa trắng là $(NH_4)_2SO_4$
$(NH_4)_2SO_4 + Ba(OH)_2 \to BaSO_4 + 2NH_3 + 2H_2O$
- mẫu thử tạo kết tủa trắng là $Na_2SO_4$
$Ba(OH)_2 + Na_2SO_4 \to BaSO_4 + 2NaOH$
- mẫu thử không hiện tượng là $NH_3$
Đúng 1
Bình luận (0)
Trình bày phương pháp hoá học phân biệt 3 chất lỏng sau: toluen, benzen, stiren. Viết phương trình hoá học của các phản ứng hoá học đã dùng.
- Cho 3 chất lỏng tác dụng với dung dịch KMnO4 ở nhiệt độ thường, chất nào làm mất màu dung dịch KMnO4 ở nhiệt độ thường là stiren.
- Với 2 hỗn hợp phản ứng còn lại ta đem đun nóng, chất nào làm mất màu dung dịch KMnO4 (nóng) thì là toluen, còn lại là benzen.
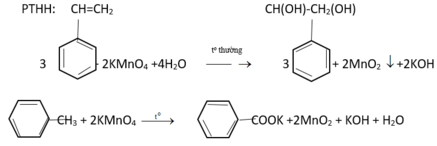
Đúng 0
Bình luận (0)
Trình bày phương pháp hoá học phân biệt các chất: benzen, hex-1-en và toluen. Viết phương trình hoá học của các phản ứng đã dùng
– Cho các chất lần lượt tác dụng với dung dịch Br2, chất nào làm nhạt màu dung dịch Br2 thì đó là hex-1-en.
- Cho 2 chất còn lại qua dung dịch KMnO4, chất nào làm mất màu dung dịch KMnO4 thì đó là toluen.
PTHH:
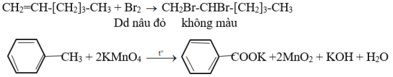
Đúng 1
Bình luận (0)
Cho 4 dung dịch đựng trong 4 ống nghiệm riêng biệt không nhãn,gồm:NaCl,NaOH,HCl,Na2SO4 loãng. hãy trình bày phương pháp hóa học để nhận biết từng dung dịch trong mỗi ống nghiệm nói trên và Viết các phương trình hoá học của các phản ứng xảy ra(nếu có)
- Trích mẫu thử.
- Nhỏ vài giọt từng mẫu thử vào giấy quỳ tím.
+ Quỳ hóa xanh: NaOH
+ Quỳ hóa đỏ: HCl
+ Quỳ không đổi màu: NaCl, Na2SO4 (1)
- Cho mẫu thử nhóm (1) pư với dd BaCl2
+ Có tủa trắng: Na2SO4
PT: \(BaCl_2+Na_2SO_4\rightarrow2NaCl+BaSO_4\)
+ Không hiện tượng: NaCl
- Dán nhãn.
Đúng 2
Bình luận (0)
Nêu phương pháp hoá học để phân biệt các dung dịch sáu với điều kiện được dùng quỳ tím và chọn thêm một hoá chất làm thuốc thử :
Na
2
SO
4
, NaCl,
H
2
SO
4
, HClViết PTHH của những phản ứng đã dùng.
Đọc tiếp
Nêu phương pháp hoá học để phân biệt các dung dịch sáu với điều kiện được dùng quỳ tím và chọn thêm một hoá chất làm thuốc thử :
Na 2 SO 4 , NaCl, H 2 SO 4 , HCl
Viết PTHH của những phản ứng đã dùng.
- Dùng quỳ tím để phân thành hai nhóm chất :
Nhóm 1 : HCl, H 2 SO 4
Nhóm 2 : Na 2 SO 4 , NaCl
Thuốc thử được chọn thêm có thể là dung dịch BaCl 2 để phân biệt từng chất có trong mỗi nhóm chất:
Chất nào ở nhóm 1 tạo kết tủa trắng với dung dịch BaCl 2 ; chất đó là H 2 SO 4 ; Chất còn lại là HCl.
Chất nào ở nhóm 2 tạo kết tủa trắng với dung dịch BaCl 2 chất đó là Na 2 SO 4 ; Chất còn lại là NaCl.
PTHH:
H 2 SO 4 + BaCl 2 → Ba SO 4 + 2HCl
Na 2 SO 4 + BaCl 2 → 2NaCl + Ba SO 4
Đúng 0
Bình luận (0)
Bằng phương pháp hoá học, hãy nhận biết các chất sau: a/ Dung dịch: NH4Cl, (NH4)2SO4, Nacl, Na2SO4 b/ Dung dịch: CuSO4, K2SO4, KNO3, Ba(NO3)2
a, - Trích mẫu thử.
- Cho từng mẫu thử pư với dd Ba(OH)2
+ Có khí mùi khai: NH4Cl
PT: \(Ba\left(OH\right)_2+2NH_4Cl\rightarrow BaCl_2+2NH_3+2H_2O\)
+ Có tủa trắng và khí mùi khai: (NH4)2SO4
PT: \(\left(NH_4\right)_2SO_4+Ba\left(OH\right)_2\rightarrow BaSO_4+2NH_3+2H_2O\)
+ Có tủa trắng: Na2SO4
PT: \(Na_2SO_4+Ba\left(OH\right)_2\rightarrow2NaOH+BaSO_4\)
+ Không hiện tượng: NaCl.
- Dán nhãn.
b, - Trích mẫu thử.
- Cho từng mẫu thử pư với dd NaOH
+ Có tủa xanh: CuSO4
PT: \(CuSO_4+2NaOH\rightarrow Na_2SO_4+Cu\left(OH\right)_2\)
+ Không hiện tượng: K2SO4, KNO3, Ba(NO3)2 (1)
- Cho mẫu thử nhóm (1) pư với dd BaCl2
+ Có tủa trắng: K2SO4
PT: \(BaCl_2+K_2SO_4\rightarrow2KCl+BaSO_4\)
+ Không hiện tượng: KNO3, Ba(NO3)2 (2)
- Cho mẫu thử nhóm (2) pư với dd K2SO4
+ Có tủa trắng: Ba(NO3)2
PT: \(K_2SO_4+Ba\left(NO_3\right)_2\rightarrow2KNO_3+BaSO_4\)
+ Không hiện tượng: KNO3
- Dán nhãn.
Đúng 3
Bình luận (1)
Chỉ dùng một thuốc thử, trình bày phương pháp phân biệt các dung dịch riêng biệt: NH4Cl, (NH4)2SO4, NaNO3, Al(NO3)3, MgCl2, FeCl2, FeCl3
Phương pháp: thử 5 hóa chất hữu dụng: Ba(OH)2, H2SO4, AgNO3, Quì, HCl
|
|
NH4Cl |
(NH4)2SO4 |
NaNO3 |
| Ba(OH)2 |
↑NH3 Mùi khai |
↑NH3 Mùi khai BaSO4 ↓trắng |
x |
|
|
MgCl2 |
FeCl2 |
FeCl3 |
|
|
Mg(OH)2 Trắng |
Fe(OH)2 xanh |
Fe(OH)3 Nâu đỏ |
|
|
Al(NO3)3 |
|
|
|
|
Al(OH)3 Trắng sau đó tan dần |
|
|
Đúng 0
Bình luận (0)
Bằng phương pháp hoá học phân biệt các muối :
N
a
3
P
O
4
, NaCl, NaBr,
N
a
2
S
,
N
a
N
O
3
. Nêu rõ hiện tượng dùng để phân biệt và viết phương trình hoá học của các phản ứng.
Đọc tiếp
Bằng phương pháp hoá học phân biệt các muối : N a 3 P O 4 , NaCl, NaBr, N a 2 S , N a N O 3 . Nêu rõ hiện tượng dùng để phân biệt và viết phương trình hoá học của các phản ứng.
Dùng dung dịch A g N O 3 để phân biệt các muối: N a 3 P O 4 , NaCl, NaBr, N a 2 S , N a N O 3 .
Lấy mỗi muối một ít vào từng ống nghiệm, thêm nước vào mỗi ống và lắc cẩn thận để hoà tan hết muối. Nhỏ dung dịch A g N O 3 vào từng ống nghiệm.
- Ở dung dịch nào có kết tủa màu trắng không tan trong axit mạnh, thì đó là dung dịch NaCl :
NaCl + A g N O 3 → AgCl↓ + N a N O 3 (màu trắng)
- Ở dung dịch nào có kết tủa màu vàng nhạt không tan trong axit mạnh, thì đó là dung dịch NaBr :
NaBr + A g N O 3 → AgBr↓ + N a N O 3 (màu vàng nhạt)
- Ở dung dịch nào có kết tủa màu đen, thì đó là dung dịch Na2S :
N a 2 S + 2 A g N O 3 → A g 2 S ↓ + 2 N a N O 3 (màu đen)
- Ở dung dịch nào có kết tủa màu vàng tan trong axit mạnh, thì đó là dung dịch Na3PO4 :
N a 3 P O 4 + 3 A g N O 3 → N a 3 P O 4 + 3 N a N O 3 (màu vàng)
- Ở dung dịch không có hiện tượng gì là dung dịch N a N O 3 .
Đúng 0
Bình luận (0)
Có bốn dung dịch: (NH4)2CO3, AgNO3, K3PO4, NaNO3, HCl đựng trong 4 lọ riêng biệt. Chỉ dùng quỳ tím, hãy trình bày phương pháp hóa học để phân biệt từng dung dịch. Viết các phương trình phản ứng xảy ra (nếu có)?
- Dùng quỳ tím
+) Hóa đỏ: HCl và AgNO3 (Nhóm 1)
+) Hóa xanh: K3PO4
+) Không đổi màu: NaNO3 và (NH4)2CO3
- Đổ dd BaCl2 vào từng nhóm
+) Xuất hiện kết tủa: AgNO3 (Nhóm 1) và (NH4)2CO3 (Nhóm 2)
PT: \(Ag^++Cl^-\rightarrow AgCl\downarrow\)
\(Ba^{2+}+CO_3^{2-}\rightarrow BaCO_3\downarrow\)
+) Không hiện tượng: HCl (Nhóm 1) và NaNO3 (Nhóm 2)
Đúng 1
Bình luận (1)












