Đốt cháy hoàn toàn 100ml hơi chất A, cần dùng 250ml O 2 , chỉ tạo ra 200ml CO 2 và 200ml hơi nước( các thể tích đo cùng điều kiện). Công thức phân tử của A là:
A. C 2 H 4
B. C 2 H 6 O
C. C 2 H 4 O
D. C 3 H 6 O
Đốt cháy hoàn toàn 100ml hơi chất hữu cơ A chứa 3 nguyên tố C,H,O cần 250ml oxi thu được 200ml CO2 và 200ml H2O. . Xác định công thức phân tử của hợp chất hữu cơ
Bảo toàn \(oxi\) :
\(n_{O/A}=2n_{CO_2}+n_{H_2O}-2n_{O_2}=1\left(mol\right)\)
\(SốC=\dfrac{n_{CO_2}}{n_A}=2\)
\(SốH=\dfrac{2n_{H_2O}}{n_A}=4\)
\(SốO=\dfrac{n_{O/A}}{n_A}=1\)
\(CTPT:C_2H_4O\)
a/ Đốt cháy hoàn toàn 1 lít khí (Y) cần 6,5 lít khí oxi. Sau phản ứng thu được 4 lít khí cacbonic và 5 lít hơi nước. Xác định công thức phân tử của (Y) và viết công thức cấu tạo. b/ Đốt cháy 100ml hơi khí (Z) cần 300ml oxi. Sản phẩm thu được 200ml khí CO, và 200ml hơi nước. Tìm công thức phân tử của (Z). Phân tử khối của (Z) bằng bao nhiêu? Biết rằng các khí và hơi nước đo ở cùng điều kiện nhiệt độ và áp suất.
Giải thích các bước giải:
⋅⋅ 2Cu+O2→to2CuO2
Do đun trong không khí 1 thời gian
⇒ A: CuO,Cudư
⋅⋅ Hòa tan A trong H2SO4 đặc nóng
CuO+H2SO4→CuSO4+H2O
Cu+2H2SO4→toCuSO4+SO2+2H2O
ddB:CuSO4
khíD:SO2
⋅⋅cho Na vào dd CuSO44 thì Na sẽ tác dụng với H2O2 ở trong muối trước sau đó sẽ tác dụng với CuSO4
2Na+2H2O→2NaOH+H22
2NaOH+CuSO4→Cu(OH)2⏐↓+Na2SO42
Khí G:H2
Kết tủa M:Cu(OH)2
⋅⋅Cho SO2 vào KOH
SO2+2KOH→K2SO3
K2SO3+SO2+H2O→2KHSO
K2SO3+BaCl2→BaSO3↓+2KCl
2KHSO3+2NaOH→K2SO3+Na2SO3+2H2O
đốt cháy hoàn toàn 2 thể tích hợp chất A cần 9 thể thích khí O2 và tạo ra 6 thể tích khí cacbonic và 8 thể tích hơi nước. Các chấy khí và hơi đo ở cùng điều kiện về nhiệt độ, áp suất. Xác định CTPT của A
Giả sử khí được đo ở điều kiện sao cho 1 mol khí chiếm thể tích 1 lít
\(n_A=\dfrac{2}{1}=2\left(mol\right)\)
\(n_{O_2}=\dfrac{9}{1}=9\left(mol\right)\)
\(n_{CO_2}=\dfrac{6}{1}=6\left(mol\right)\)
\(n_{H_2O}=\dfrac{8}{1}=8\left(mol\right)\)
Bảo toàn C: nC(A) = 6 (mol)
Bảo toàn H: nH(A) = 16 (mol)
Bảo toàn O: \(n_{O\left(A\right)}=6.2+8.1-9.2=2\left(mol\right)\)
Số nguyên tử C là \(\dfrac{6}{2}=3\) (nguyên tử)
Số nguyên tử H là \(\dfrac{16}{2}=8\) (nguyên tử)
Số nguyên tử O là \(\dfrac{2}{2}=1\) (nguyên tử)
=> CTPT: C3H8O
Đốt cháy hoàn toàn 4,6 gam rượu etylic trong oxi thu được khí cacbonđioxit và hơi nước. a. Viết phương trình hóa học xảy ra? b. Tính thể tích khí oxi (ở đktc) cần dùng ? c. Tính khối lượng khí cacbonic và khối lượng hơi nước tạo thành?
a) $C_2H_5OH + 3O_2 \xrightarrow{t^o} 2CO_2 + 3H_2O$
b) $n_{C_2H_5OH} = \dfrac{4,6}{46} = 0,1(mol)$
$n_{O_2} = 3n_{C_2H_5OH} = 0,3(mol)$
$V_{O_2} = 0,3.22,4 = 6,72(lít)$
c)
Theo PTHH :
$n_{CO_2} = 2n_{C_2H_5OH} = 0,2(mol) \Rightarrow V_{CO_2} = 0,2.22,4 = 4,48(lít)$
$n_{H_2O} = 3n_{C_2H_5OH} = 0,3(mol) \Rightarrow m_{H_2O} = 0,3.18 = 5,4(gam)$
Anh chị làm ơn giúp e mấy bài này ạ.E cảm ơn!
Bài 1:
Khi đốt cháy hoàn toàn một lượng hợp chất hữu cơ X cần 0,8 gam O2 người ta thu được 1,1 gam CO2,0,45 gam H2O và không có sản phẩm nào khác. Xác định công thức phân tử của X. Biết rằng khi cho bay hơi hoàn toàn 0,6gam X ở điều kiện nhiệt độ và áp suất thích hợp đã thu được một thể tích hơi đúng bằng thể tích hơi của 0,32 gam O2 trong cùng điều kiện.
Bài 2:
Đốt cháy hoàn toàn một hợp chất hữu cơ A có thành phần C,H,O thu được CO2 có thể tích bằng 3/4 thể tích hơi nước và bằng 6/7 thể tích O2 dùng để đốt cháy. Mặt khác, 1l hơi A có khối lượng bằng 46 lần khối lượng 1 lít H2 ở cùng điều kiện.Tìm công thức phân tử của A.
Bài 3: Đốt cháy hoàn toàn 4,3 gam hợp chất hữu cơ thu được 6,72 lít CO2 và 0,35 mol H2O. Khi đốt cháy hoàn toàn 1 mol chất A cần 212,8l O2.Xác định CTPT của A.
Đốt cháy 400ml hơi 1 chất hữu cơ A chứa C, H, O trong 1800ml O2, thể tích hỗn hợp khí thu được là 2,6 lít. Sau khi cho hơi nước ngưng tụ, chỉ còn 1400ml. Tiếp theo cho qua dung dịch NaOH đậm đặc thì chỉ còn lại 200ml (các thể tích khí đo được ở cùng điều kiện). Công thức phân tử của chất hữu cơ A là:
A. C3H6O2
B. C3H6
C. C3H8O
D. C3H8
Đáp án A
Gọi công thức phân tử của A là CxHyOz.
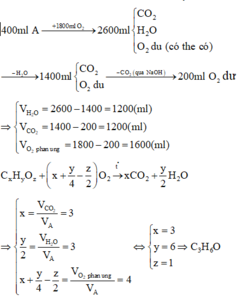
Hỗn hợp X g'ôm(CH3)2NH và 2 hidrocacbon đồng đẳng kế tiếp. Đốt cháy hoàn toàn 100ml hỗn hợp X bằng lượng oxi vừa đủ, thu được 550ml hỗn hợp khí và hơi nước. Nếu cho Y đi qua dung dịch H2SO4 đặc, dư thì còn lại 250ml khí (các thể tích khí và hơi đo ở cùng điều kiện). Công thức phân tử của 2 hidrocacbon là:
A. CH4 và C2H6.
B. C2H4 và C3H6.
C. C2H6 và C3H8.
D. C3H6 và C4H8.
Gọi công thức phân tử trung bình của 2 hidrocacbon là C n H 2 n + 2 - 2 k (vì 2 hidrocacbon thuộc cùng dãy đồng đẳng nên k ∈ N ). Giả sử có X mol C2H7N và y mol CnH2n+2-2k

Vì 2 hidrocacbon là đồng đẳng kế tiếp nên 2 hidrocacbon có số nguyên tử C trong phân tử là 2 và 3.
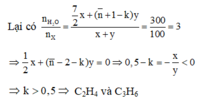
Đáp án B
Đốt cháy hoàn toàn một chất X thu được CO 2 và H 2 O . Biết thể tích CO 2 sinh ra bằng thể tích oxi cần dùng và gấp 1,5 lần thể tích hơi nước ở cùng điều kiện nhiệt độ, áp suất. X là hợp chất đơn chức tác dụng được với dd Ag 2 O / NH 3 . Công thức cấu tạo của X là:
A. HCHO
B. CH 3 CHO
C. HCOOCH 3
D. HCOOCH = CH 2
Đáp án D
Công thức cấu tạo của X là HCOOCH = CH 2
Đốt cháy một hỗn hợp 300ml hiđrocacbon và amoniac trong oxi có dư. Sau khi cháy hoàn toàn, thể tích khí thu được là 1250ml. Sau khi làm ngưng tụ hơi nước, thể tích giảm còn 550ml. Sau khi cho tác dụng với dung dịch kiềm còn 250ml trong đó có 100ml nitơ. Thể tích của tất cả các khí đo trong điều kiện như nhau. Lập công thức của hiđrocacbon
V nước = = 1250 - 550 = 700(ml)
V nio = 100(ml)
=> V CO2 = 550 - 250 = 300(ml)
Bảo toàn nguyên tố với N :
=> V NH3 = 2 V N2 = 200(ml)
=> V hidrocacbon = 300 -200 = 100(ml)
Ta có :
Số nguyên tử C = V CO2 / V hidrocacbon = 300/100 = 3
Khi đốt NH3, V H2O sinh ra = 3/2 V NH3 = 300(ml)
=> V H2O khi đốt hidrocacbon sinh ra = 700 -300 = 400(ml)
Số nguyên tử H = 2V H2O / V hidrocacbon = 400.2/100 = 8
Vậy CTPT của hidrocacbon là C3H8