Mg có thể khử được axit HNO3 thành khí N2 theo phản ứng hoá học:
aMg + bHNO 3 → cMg NO 3 2 + dN 2 + eH 2 O
Tỉ lệ a:b là :
A. 1:3
B. 5:12
C. 3:8
D. 4:15
Dãy nào dưới đây gồm các chất chứa nguyên tử nitơ có khả năng vừa thể hiện tính khử vừa thể hiện tính oxi hoá khi tham gia phản ứng?
A. N H 3 , N 2 O 5 , N 2 , N O 2
B. N H 3 , NO, H N O 3 , N 2 O 5
C. N 2 , NO, N 2 O , N 2 O 5
D. N O 2 , N 2 , NO, N2O3
Thực hiện thí nghiệm theo các sơ đồ phản ứng:
Mg + HNO3 đặc, dư → khí X
CaOCl2 + HCl → khí Y
NaHSO3 + H2SO4 → khí Z
Ca(HCO3)2 + HNO3 → khí T
Cho các khí X, Y, Z, T lần lượt tác dụng với dung dịch NaOH dư. Trong tất cả các phản ứng trên có bao nhiêu phản ứng oxi hoá - khử?
A. 4.
B. 5.
C. 2.
D. 3.
Đáp án A
Phương trình phản ứng:

Trong tất cả các phản ứng trên, có 4 phản ứng oxi hóa – khử là (1), (2), (5) và (6).
Thực hiện thí nghiệm theo các sơ đồ phản ứng :
Mg + HNO3 đặc, dư → khí X
CaOCl2 + HCl → khí Y
NaHSO3 + H2SO4 → khí Z
Ca(HCO3)2 + HNO3 → khí T
Cho các khí X, Y, Z, T lần lượt tác dụng với dung dịch NaOH dư. Trong tất cả các phản ứng trên có bao nhiêu phản ứng oxi hoá - khử ?
A. 4.
B. 3
C. 2
D. 5
Đáp án A
Phương trình phản ứng :
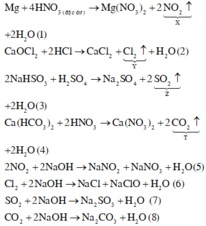
Trong tất cả các phản ứng trên, có 4 phản ứng oxi hóa – khử là (1), (2), (5) và (6).
Thực hiện thí nghiệm theo các sơ đồ phản ứng :
Mg + HNO3 đặc, dư → khí X
CaOCl2 + HCl → khí Y
NaHSO3 + H2SO4 → khí Z
Ca(HCO3)2 + HNO3 → khí T
Cho các khí X, Y, Z, T lần lượt tác dụng với dung dịch NaOH dư. Trong tất cả các phản ứng trên có bao nhiêu phản ứng oxi hoá - khử ?
A. 4
B. 3
C. 2.
D. 5
Chọn A
Trong tất cả các phản ứng trên, có 4 phản ứng oxi hóa – khử là (1), (2), (5) và (6).
Thiết lập phương trình phản ứng oxi hóa - khử theo phương pháp thăng bằng electron?Chỉ rõ chất khử, chất oxi hóa trong mỗi phản ứng.
1.Al + HNO3 → Al(NO3)3 + NH4 NO3 + H2O.
2.Mg + HNO3 → Mg(NO3)2 + NO + H2O.
3.Mg + H2SO4 → MgSO4 + H2S + H2O.
4.Fe + H2SO4 → Fe2 (SO4)3 + SO2 + H2O.
1. Chất khử: Al
Chất oxi hóa: HNO3
\(Al\rightarrow Al^{3+}+3e|\times8\\ N^{+5}+8e\rightarrow N^{-3}|\times3\)
8Al + 30HNO3 → 8Al(NO3)3 + 3NH4NO3 + 9H2O.
2. Chất khử: Mg
Chất oxi hóa: HNO3
\(Mg\rightarrow Mg^{2+}+2e|\times3\\ N^{+5}+3e\rightarrow N^{+2}|\times2\)
3Mg + 8HNO3 → 3Mg(NO3)2 + 2NO + 4H2O.
3. Chất khử: Mg
Chất oxi hóa: H2SO4
\(Mg\rightarrow Mg^{2+}+2e|\times8\\ S^{+6}+8e\rightarrow S^{-2}|\times2\)
8Mg + 10H2SO4 → 8MgSO4 + 2H2S + 8H2O.
4.Chất khử: Fe
Chất oxi hóa: H2SO4
\(2Fe\rightarrow Fe^{3+}_2+6e|\times1\\ S^{+6}+2e\rightarrow S^{+4}|\times3\)
2Fe + 6H2SO4 → Fe2 (SO4)3 + 3SO2 + 6H2O.
Hòa tan hoàn toàn 8,8 gam hợp kim Mg – Cu bằng axit H N O 3 , sau phản ứng thu được 4,48 lít hỗn hợp khí B gồm NO và NO2 (ở đktc, ngoài ra không còn sản phẩm khử nào khác). Biết tỉ khối của B so với H2 bằng 19. Thành phần của Mg trong hợp kim là
A. 22,77%.
B. 72,72%.
C. 27,27%.
D. 50,00%
Hòa tan hoàn toàn 8,8 gam hợp kim Mg – Cu bằng axit HNO3, sau phản ứng thu được 4,48 lít hỗn hợp khí B gồm NO và NO2 (ở đktc, ngoài ra không còn sản phẩm khử nào khác). Biết tỉ khối của B so với H2 bằng 19. Thành phần của Mg trong hợp kim là
A. 22,77%.
B. 72,72%.
C. 27,27%.
D. 50,00%
Cho phản ứng aMg + bHNO3 \(\rightarrow\) cMg(NO3)2 + dN2 +eH2O
a.Tổng hệ số (a+b)
b.Tỉ lệ phân tử HNO3 đóng vai trò môi trường và số phân tử bị khử
a, (a+b)=16
b, Tỉ lệ phân tử HNO3 đóng vai trò môi trường và số phân tử bị khửlà 5:1
Bài 11:Cân bằng các phản ứng oxi hóa khử sau theo phương pháp thăng bằng e
a. Mg + HNO3 => Mg(NO 3 ) 2 + NH4NO3 + H2O
b. Na + H2SO4 => Na2SO4 + H2S + H2O
c. FexOy + H2SO4 => Fe2(SO4)3 + SO2 + H2O
d. HNO3 + H2S => NO + S + H2O
e. FexOy + HNO3 => Fe(NO3)3 + NO + H2O
f. Fe + HNO3 => Fe(NO3)3 + NO2 + H2O g. FeS2 + O2 => Fe2O3 + SO2
h. FeO + H2SO4 => Fe2(SO4)3 + SO2 + H2O
Trước tiên bn cần tìm số oxi hóa của mỗi chất trước đã nhé
a. 4Mg + 10HNO3 ---> 4Mg(NO3)2 + NH4NO3 + 3H2O
b. 8Na + 5H2SO4 ---> 4Na2SO3 + 5H2S + 4H2O
c. 2FexOy + (3x - 2y)H2SO4 ---> xFe2(SO4)3 + 2ySO2 + (3x - 2y)H2O
d. 2HNO3 + 3H2S ---> 2NO + 3S + 4H2O
e. 3FexOy + (12x - 2y)HNO3 ---> 3xFe(NO3)3 + (3x - 2y)NO + (6x - y)H2O
f. Fe + 6HNO3 ---> Fe(NO3)3 + 3NO2 + 3H2O
g. 4FeS2 + 11O2 ---to---> 2Fe2O3 + 8SO2
h. 2FeO + 4H2SO4 ---> Fe2(SO4)3 + SO2 + 4H2O