Trộn 500ml dung dịch X gồm HCL 0,01M và H2SO4 0,001M với 500ml dung dịch NAOH 0,01M. Tính pH dung dịch sau phản ứng ?

Những câu hỏi liên quan
Trộn 250ml dung dịch hỗn hợp gồm H2SO4 0,005M và HCl 0,01M với 200ml dung dịch hỗn hợp gồm NaOH 0,001M và Ba(OH)2 0,0005M thu được dung dịch X. Dung dịch X có pH là:
A. 12,3
B. 1,18
C. 11,87
D. 2,13
Đáp án D
nH2SO4 = 0,005 .0,25 =0,00125(mol)
nHCl = 0,01. 0,25= 0,0025 (mol)
∑n= 0,00125 + 0,0025= 0,00375 (mol)
∑n= 0,001.0,2 + 0,0005.2.0,2=0,0004
H+ + OH- → H2O
Ban đầu: 0,00375 0,0004
Phản ứng: 0,0004 0,0004
Sau phản ứng: 0,00335 0
Vsau = 0,2 + 0,25= 0,45(lít)
Mà 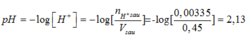
Đúng 0
Bình luận (0)
Trộn 200ml dung dịch H2SO4 0,01M vào 100ml dung dịch NaOH 0,01M. Tính pH của dung dịch X sau phản ứng
\(n_{H^+}=0.2\cdot0.01\cdot2=0.004\left(mol\right)\)
\(n_{OH^-}=0.1\cdot0.01=0.001\left(mol\right)\)
\(H^++OH^-\rightarrow H_2O\)
\(0.001.....0.001\)
\(n_{H^+\left(dư\right)}=0.004-0.001=0.003\left(mol\right)\)
\(pH=-log\left(H^+\right)=-log\left(\dfrac{0.003}{0.2+0.1}\right)=2\)
Đúng 0
Bình luận (0)
Có: \(n_{H^+}=2n_{H_2SO_4}=2.0,2.0,01=0,004\left(mol\right)\)
\(n_{OH^-}=0,1.0,01=0,001\left(mol\right)\)
PT ion: \(H^++OH^-\rightarrow H_2O\)
____0,004___0,001 (mol)
\(\Rightarrow n_{H^+\left(dư\right)}=0,003\left(mol\right)\)\\(\Rightarrow\left[H^+\right]=\dfrac{0,003}{0,3}=0,01\)
\(\Rightarrow pH=2\)
Bạn tham khảo nhé!
Đúng 0
Bình luận (0)
mọi người giúp e với ạ
Tính pH:
a) cho 500ml dung dịch H2SO4 0,01M + 300ml dung dịch HNO3 0,02
b) cho 500ml dung dịch Ca(OH)2 0,01M + 300ml dung dịch NaOH 0,02M
c) cho 500ml dung dịch Ca(OH)2 0,01M + 300ml dung dịch H2SO4 0,01M
Trộn 100ml dung dịch NaOH 0,01M với 200ml dung dịch HCl 0,01M. Tính pH của dung dịch thu được sau phản ứng
Trộn 100ml dung dịch axit HCl 0,01M với 200ml dung dịch NaOH 0,5M thu được dung dịch A sau phản ứng.Viết phương trình phân tử và ion rút gọn của phản ứng và tính pH của dung dịch sau phản ứng.
a)
$NaOH + HCl \to NaCl + H_2O$
$OH^- + H^+ \to H_2O$
b)
$n_{HCl} = 0,1.0,01 = 0,001(mol)$
$n_{NaOH} = 0,2.0,5= 0,1(mol)$
$\Rightarrow$ NaOH dư, HCl hết
$n_{NaOH\ pư} = 0,001 \Rightarrow n_{NaOH\ dư} = 0,1 - 0,001 = 0,099(mol)$
$\Rightarrow [OH^-] = \dfrac{0,099}{0,1 + 0,2} = 0,33M$
$\Rightarrow pOH = -log(0,33) = 0,48 $
$pH = 14 - pOH = 14 - 0,48 = 13,52$
Đúng 3
Bình luận (0)
Trộn 250 ml dung dịch hỗn hợp gồm HCl 0,08M và
H
2
SO
4
0,01M với 250 ml dung dịch NaOH a mol/l, thu được 500 ml dung dịch có pH 12. Giá trị của a là: A. 0,13. B. 0,10. C.0,12. D. 0,14.
Đọc tiếp
Trộn 250 ml dung dịch hỗn hợp gồm HCl 0,08M và H 2 SO 4 0,01M với 250 ml dung dịch NaOH a mol/l, thu được 500 ml dung dịch có pH = 12. Giá trị của a là:
A. 0,13.
B. 0,10.
C.0,12.
D. 0,14.
Tính pH của các dung dịch sau:
a) Dung dịch A: H2SO4 0,01M.
b) Dung dịch B: NaOH 0,01M.
c) Dung dịch C: tạo bởi dung dịch A trộn với dung dịch B theo tỉ lệ tương ứng là 1:2.
Help me
a, Giả sử H2SO4 điện li hoàn toàn cả 2 nấc.
\(H_2SO_4\rightarrow2H^++SO_4^{2-}\)
0,01 ______ 0,02 _______ M
\(\Rightarrow pH=-log\left[H^+\right]\approx1,7\)
b, NaOH → Na+ + OH-
__ 0,01 _________ 0,01 M
\(\Rightarrow\left[H^+\right]=\frac{10^{-14}}{0,01}=10^{-12}M\)
⇒ pH = 12
c, Ta có: VA = x ⇒ VB = 2x
⇒ nH+ = 0,02x (mol); nOH- = 0,02x (mol)
\(H^++OH^-\rightarrow H_2O\)
0,02x _0,02x ________ (mol)
⇒ Pư hết.
Môi trường sau pư là môi trường trung tính. ⇒ pH = 7
Bạn tham khảo nhé!
Tính pH của các dung dịch sau khi trộn:
a. Trộn 100 ml dung dịch HCl 0,002M với 400 ml dung dịch H2SO4 0,0025M
b.Pha thêm 200 ml H2O vào 300 ml dung dịch HCl có pH=3
c. Trộn 200 ml dung dịch KOH 0,001M với 300 ml dung dịch NaOH 0,001M
Trộn 250 ml dung dịch chứa hỗn hợp HCl 0,08M và H2SO4 0,01M với 250 ml dung dịch NaOH aM thu được 500 ml dung dịch có pH 12. Giá trị a là: A. 0,13M. B. 0,12M. C. 0,14M. D. 0.10M.
Đọc tiếp
Trộn 250 ml dung dịch chứa hỗn hợp HCl 0,08M và H2SO4 0,01M với 250 ml dung dịch NaOH aM thu được 500 ml dung dịch có pH = 12. Giá trị a là:
A. 0,13M.
B. 0,12M.
C. 0,14M.
D. 0.10M.




















