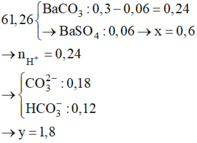Sục từ từ 6,72 lít khí CO2 ở đktc vào 200 ml dd Ca(OH)2.2M. Xác định khối lượng muối sinh ra

Những câu hỏi liên quan
1,Hấp thụ 6,72 lít khí SO2 đo ở đktc vào 100 g dd NaOH 20%. Hãy xác định khối lượng muối sinh ra
2,Sục từ từ 6,72 lít khí CO2 ở đktc vào 200 ml dd Ca(OH)2.2M. Xác định khối lượng muối sinh ra
1,hấp thụ 6,72 lít khí SO2 đo ở đktc vào 100 g đ NaOH 20%.hãy xác định khối lượng muối sinh ra
2,sục từ từ 6,72 lít khí CO2 ở đktc vào 200 ml dd Ca(OH)2.2M.xác định khối lượng muối sinh ra
Xác định khối lượng kết tủa thu được khi dẫn từ từ 6,72 lít khí CO2 (đktc) vào 400ml dung dịch Ca(OH)2 1M?
A. 30 gam
B. 40 gam
C. 35 gam
D. 45 gam
Đáp án A
nCO2= 6,72/22,4= 0,3 mol;
nCa(OH)2= 0,4.1= 0,4 mol
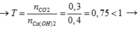
Sau phản ứng thu được muối trung hòa CaCO3
CO2 + Ca(OH)2 → CaCO3 + H2O
Ta có: 0,3 < 0,4 nên CO2 phản ứng hết, Ca(OH)2 còn dư
Ta có: nCaCO3= nCO2= 0,3 mol → mCaCO3= 0,3.100= 30,0 gam
Đúng 0
Bình luận (0)
dẫn 6,72 lít khí co2 ở đktc vào 200ml dung dịch Ca(OH)2 1M. Tính khối lượng các muối sinh ra (giải bằng 2 cách)
\(n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{Ca\left(OH\right)_2}=0,2.1=0,2\left(mol\right)\)
PTHH :
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\)(1)
0,2 0,2 0,2 0,2
\(CO_2+CaCO_3+H_2O\rightarrow Ca\left(HCO_3\right)_2\)(2)
0,1 0,1 0,1 0,1
Có :
\(\dfrac{n_{CO_2}}{n_{Ca\left(OH\right)_2}}=\dfrac{0,3}{0,2}\) => Tạo cả 2 muối: CaCO3 và Ca(HCO3)2
\(m_{CaCO_3}=\left(0,2-0,1\right).100=10\left(g\right)\)
\(m_{Ca\left(HCO_3\right)_2}=0,1.162=16,2\left(g\right)\)
Đúng 1
Bình luận (0)
Dưới đây là cách giải quyết từng bài tập của bạn:
Bài 5:
a) Tính thể tích khi Hydrogen (H2) sinh ra (ở đkc):
Theo phản ứng: 2Al + 3H2SO4 -> 3H2 + 2Al2(SO4)3
Khối lượng mol của Al = 5.4 g / 27 g/mol = 0.2 mol
Khối lượng mol của H2SO4 = 150 g / (2 g/mol + 32 g/mol + 4 g/mol) = 150 g / 98 g/mol ≈ 1.53 mol
Do phản ứng có tỷ số mol của Al và H2SO4 là 2:3, vậy Al sẽ là chất dư, và số mol H2 được sinh ra sẽ bằng 2/3 số mol H2SO4.
Số mol H2 = (2/3) * 1.53 mol ≈ 1.02 mol
Thể tích H2 ở điều kiện tiêu chuẩn (0°C và 1 atm) là 24.45 L/mol.
Vậy thể tích H2 sinh ra ≈ 1.02 mol * 24.45 L/mol ≈ 24.95 L.
b) Tính nồng độ phần trăm của dung dịch H2SO4:
Khối lượng H2SO4 ban đầu = 150 g
Nồng độ phần trăm của H2SO4 = (khối lượng H2SO4 / khối lượng dung dịch) * 100%
Nồng độ phần trăm của H2SO4 = (150 g / (150 g + 5.4 g)) * 100% ≈ 96.6%
c) Tính khối lượng muối tạo thành:
Theo phản ứng: 2Al + 3H2SO4 -> 3H2 + 2Al2(SO4)3
Khối lượng mol của Al2(SO4)3 = 0.2 mol
Khối lượng muối tạo thành = (0.2 mol * 2 * (98 g/mol)) / 2 = 19.6 g.
Bài 8:
a) Tính m:
Theo phản ứng: 2Al + 6HCl -> 2AlCl3 + 3H2
Số mol H2 = 7.437 L / 22.4 L/mol = 0.332 mol
Số mol Al = 0.5 * số mol H2 = 0.5 * 0.332 mol = 0.166 mol
Khối lượng Al = 0.166 mol * 27 g/mol = 4.482 g
b) Tính nồng độ mol dung dịch HCl cần dùng:
Số mol HCl cần dùng = số mol Al = 0.166 mol
Thể tích dung dịch HCl = 300 ml = 0.3 L
Nồng độ mol của HCl = (0.166 mol / 0.3 L) ≈ 0.553 mol/L
c) Tính nồng độ mol dung dịch muối thu được:
Theo phản ứng: 2Al + 6HCl -> 2AlCl3 + 3H2
Số mol AlCl3 = 0.166 mol
Khối lượng mol của AlCl3 = 0.166 mol * (133.5 g/mol) = 22.121 g
Nồng độ mol của AlCl3 = (0.166 mol / 0.3 L) ≈ 0.553 mol/L
Lưu ý rằng phần c của câu 8 cho biết thể tích dung dịch không đáng kể thay đổi, vì vậy nồng độ mol của muối AlCl3 sau phản ứng là tương tự nồng độ mol của dung dịch HCl ban đầu.
Đúng 0
Bình luận (0)
![]()
tính khối lượng các chất có trong dd sau phản ứng trong các trường hợp sau:
a) sục từ từ 2,24 lít CO2 vào 500ml dd NaOH 0,2M
b) dẫn 11,2 lít SO2 vào dd chứa 84 g KOH
c) sục 13,2g CO2 vào 500 ml Ca(OH)2 0,4M biết thể tích các khí đo ở đktc
a) nco2=v/22.4=0.1 mol
500ml=0.5l
=> nNaoh=Cm.v=0.2 . 0.5=0.1 mol
lập tỉ lệ:
nNaoh/nCo2=0.1/0.1=1
=> sảy ra phương trình
Naoh + co2 ->nahco3
mCo2=n.M=4.4 (g)
mNaoh=n.M=4 (g)
adđlbtkl ta có
mCo2 + mNaoh = mNahco3
=>mNahco3=8.4 (g)![]()
Đúng 0
Bình luận (1)
hấp thụ 0.336 lít hoạc 0.56 lit co2 vào 200 ml dung dịch ca(oh)2 thì thấy lượng kết tủa thu được là như nhau.thêm 100ml dung dịch naoh 0.1m vào 200ml dd ca(oh)2 thì được dung dịch x .sục từ từ đến dư khí co2 vào toàn bộ lượng dung dịch x trên .cho các thể tích đều được đo ở đktc a/ viết ptpu xảy ra. b/vẽ đô thị
Sục 6,72 lít khí CO2 (đktc) vào 200 ml dung dịch NaOH x mol/l và KOH y mol/l thu được dung dịch X chứa 4 muối. Cho từ từ 100 ml dung dịch chứa HCl 1,2M và H2SO4 x mol/l vào dung dịch X thu được 1,344 lít khí CO2 (đktc) và dung dịch Y. Cho Ba(OH)2 dư vào dung dịch Y thu được 61,26 gam kết tủa. Tỉ lệ của x : y là A. 1 : 3 B. 1 : 2 C. 1 : 1 D. 2 : 3
Đọc tiếp
Sục 6,72 lít khí CO2 (đktc) vào 200 ml dung dịch NaOH x mol/l và KOH y mol/l thu được dung dịch X chứa 4 muối. Cho từ từ 100 ml dung dịch chứa HCl 1,2M và H2SO4 x mol/l vào dung dịch X thu được 1,344 lít khí CO2 (đktc) và dung dịch Y. Cho Ba(OH)2 dư vào dung dịch Y thu được 61,26 gam kết tủa. Tỉ lệ của x : y là
A. 1 : 3
B. 1 : 2
C. 1 : 1
D. 2 : 3
Sục 6,72 lít khí CO2 (đktc) vào 200 ml dung dịch Ba(OH)2 1M. Khối lượng kết tủa thu được sau phản ứng là bao nhiêu gam?
A. 19,7 gam.
B. 39,4 gam.
C. 59,1 gam.
D. 78,8 gam.
\(n_{CO_2}=0,3\left(mol\right);n_{OH^-}=0,4\left(mol\right)\)
Lập T : \(\dfrac{n_{OH^-}}{n_{CO_2}}=\dfrac{0,4}{0,3}=1,33\) => Tạo 2 muối BaCO3 và Ba(HCO3)2
Gọi BaCO3 (x_mol) , Ba(HCO3)2 (y_mol)
Ta có : \(\left\{{}\begin{matrix}x+y=0,2\left(BTNT:Ba\right)\\x+2y=0,3\left(BTNT:C\right)\end{matrix}\right.\)
=> x= 0,1 ;y=0,1
=> \(m_{BaCO_3}=0,1.197=19,7\left(g\right)\)
=> Chọn A
Đúng 3
Bình luận (0)
Sục 6,72 lít khí CO2 (đktc) vào 200 ml dung dịch Ba(OH)2 1M. Khối lượng kết tủa thu được sau phản ứng là bao nhiêu gam?
A. 19,7 gam.
B. 39,4 gam.
C. 59,1 gam.
D. 78,8 gam.
Đúng 0
Bình luận (0)
Sục 6,72 lít CO2 (đktc) vào 100ml dd Ca(OH)2 0,5M và KOH 2M. Khối lượng kết tủa thu được sau khi phản ứng xảy ra hoàn toàn là bao nhiêu gam?