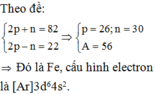Nguyên tử X có tổng số hạt cơ bản là 40. Trong đó tổng số hạt mang điện nhiều hơn số hạt ko mang điện là 12 hạt. Cấu hình electron của nguyên tử X là

Những câu hỏi liên quan
Nguyên tử của nguyên tố X có tổng số hạt cơ bản là 82, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22. Cấu hình electron của X là: A. [Ar]3d44s2 B. [Ar]3d6 C. [Ar]3d54s1 D. [Ar]3d64s2
Đọc tiếp
Nguyên tử của nguyên tố X có tổng số hạt cơ bản là 82, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22. Cấu hình electron của X là:
A. [Ar]3d44s2
B. [Ar]3d6
C. [Ar]3d54s1
D. [Ar]3d64s2
Câu 1. Cho các thông tin sau:Ion X2- có cấu hình electron: 1s22s22p63s23p6.Nguyên tố Y có tổng số hạt cơ bản trong nguyên tử là 40. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 12.Ion Z2+ có tổng số hạt mang điện tích dương trong hạt nhân bằng 29.Vị trí của X, Y, Z trong bảng tuần hoàn lần lượt là: A. (X: ô 16, chu kỳ 3, nhóm VIA); ( Y: ô 13, chu kì 3, nhóm IIIA); (Z: ô 29, chu kì 4, nhóm IB).B. (X: ô 16, chu kỳ 3, nhóm VIA); ( Y: ô 13, chu kì 3, nhóm IA); (Z: ô 29...
Đọc tiếp
Câu 1. Cho các thông tin sau:
Ion X2- có cấu hình electron: 1s22s22p63s23p6.
Nguyên tố Y có tổng số hạt cơ bản trong nguyên tử là 40. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 12.
Ion Z2+ có tổng số hạt mang điện tích dương trong hạt nhân bằng 29.
Vị trí của X, Y, Z trong bảng tuần hoàn lần lượt là:
A. (X: ô 16, chu kỳ 3, nhóm VIA); ( Y: ô 13, chu kì 3, nhóm IIIA); (Z: ô 29, chu kì 4, nhóm IB).
B. (X: ô 16, chu kỳ 3, nhóm VIA); ( Y: ô 13, chu kì 3, nhóm IA); (Z: ô 29, chu kì 4, nhóm IIB).
C. (X: ô 20, chu kỳ 4, nhóm IIA); ( Y: ô 13, chu kì 3, nhóm IIIA); (Z: ô 29, chu kì 4, nhóm IB).
D. (X: ô 16, chu kỳ 3, nhóm VIA); ( Y: ô 13, chu kì 3, nhóm IIIA); (Z: ô 31, chu kì 4, nhóm IIIA).
X có cấu hình Electron: \(1s^22s^22p^63s^23p^4\) \(\rightarrow\) X thuộc ô 16, chu kì 3, nhóm VIA
Y có: \(\left\{{}\begin{matrix}p+e+n=40\\p+e-n=12\end{matrix}\right.\) \(\Rightarrow\) \(\left\{{}\begin{matrix}p=e=13\\n=14\end{matrix}\right.\) có cấu hình Electron \(1s^22s^22p^63s^23p^1\) \(\Rightarrow\) Y thuộc ô số 13, chu kì 3, nhóm IIIA
\(Z^{2+}\) có: p = 29 \(\Rightarrow\) p của Z cũng bằng 29 (= e) nên p có cấu hình electron: \(1s^22s^22p^63s^23p^64s^13d^{10}\)
Suy ra Z thuộc ô 29, chu kì 4, nhóm IB.
Chọn câu A.
Đúng 1
Bình luận (0)
Câu 1. Cho các thông tin sau:Ion X2- có cấu hình electron: 1s22s22p63s23p6.Nguyên tố Y có tổng số hạt cơ bản trong nguyên tử là 40. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 12.Ion Z2+ có tổng số hạt mang điện tích dương trong hạt nhân bằng 29.Vị trí của X, Y, Z trong bảng tuần hoàn lần lượt là: A. (X: ô 16, chu kỳ 3, nhóm VIA); ( Y: ô 13, chu kì 3, nhóm IIIA); (Z: ô 29, chu kì 4, nhóm IB).B. (X: ô 16, chu kỳ 3, nhóm VIA); ( Y: ô 13, chu kì 3, nhóm IA); (Z: ô 29...
Đọc tiếp
Câu 1. Cho các thông tin sau:
Ion X2- có cấu hình electron: 1s22s22p63s23p6.
Nguyên tố Y có tổng số hạt cơ bản trong nguyên tử là 40. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 12.
Ion Z2+ có tổng số hạt mang điện tích dương trong hạt nhân bằng 29.
Vị trí của X, Y, Z trong bảng tuần hoàn lần lượt là:
A. (X: ô 16, chu kỳ 3, nhóm VIA); ( Y: ô 13, chu kì 3, nhóm IIIA); (Z: ô 29, chu kì 4, nhóm IB).
B. (X: ô 16, chu kỳ 3, nhóm VIA); ( Y: ô 13, chu kì 3, nhóm IA); (Z: ô 29, chu kì 4, nhóm IIB).
C. (X: ô 20, chu kỳ 4, nhóm IIA); ( Y: ô 13, chu kì 3, nhóm IIIA); (Z: ô 29, chu kì 4, nhóm IB).
D. (X: ô 16, chu kỳ 3, nhóm VIA); ( Y: ô 13, chu kì 3, nhóm IIIA); (Z: ô 31, chu kì 4, nhóm IIIA
Nguyên tử của nguyên tố X có tổng số hạt cơ bản là 82, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22. Cấu hình electron của ion
X
2
+
là A.
[
Ar
]
3
d
4
4
s
2
B.
[
Ar
]
3
d
6...
Đọc tiếp
Nguyên tử của nguyên tố X có tổng số hạt cơ bản là 82, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22. Cấu hình electron của ion X 2 + là
A. [ Ar ] 3 d 4 4 s 2
B. [ Ar ] 3 d 6
C. [ Ar ] 3 d 5 4 s 1
D. [ Ar ] 3 d 6 4 s 1
Nguyên tố X có tổng số hạt cơ bản là 34, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 10
a) Hãy viết kí hiệu nguyên tử của ngtố X
b) Việt cấu hình electron nguyên tử, cấu hình electron theo orbital của X
c) Từ cấu hình electron, dự đoán tính chất hoá học
d) Xác đinh vị trí của X trong bảng tuần hoàn
a, Ta có: P + N + E = 34
Mà: P = E (Do nguyên tử trung hòa về điện.)
⇒ 2P + N = 34 (1)
Theo đề, số hạt mang điện nhiều hơn số hạt không mang điện là 10.
⇒ 2P - N = 10 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}P=E=11=Z\\N=12\end{matrix}\right.\) ⇒ A = 11 + 12 = 23
→ KH: \(^{23}_{11}X\)
b, Cấu hình e: 1s22s22p63s1
Cấu hình e theo orbital:
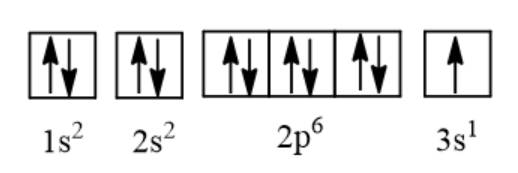
c, X có 1 e hóa trị → tính kim loại
d, - Z = 11 → ô số 11
- Có 3 lớp e → chu kỳ 3
- e cuối cùng phân bố ở phân lớp s, có 1 e hóa trị → nhóm IA
Vậy: X thuộc ô số 11, chu kỳ 3, nhóm IA
Đúng 0
Bình luận (0)
Nguyên tử nguyên tố X có tổng số hạt cơ bản (electron, proton, nơtron) cấu tạo nên nó là 34. Trong đó, số hạt mang điện nhiều hơn số hạt không mang điện là 10. Số hiệu nguyên tử của nguyên tố X là ? A. 14 B. 12 C. 11 D. 23
Đọc tiếp
Nguyên tử nguyên tố X có tổng số hạt cơ bản (electron, proton, nơtron) cấu tạo nên nó là 34. Trong đó, số hạt mang điện nhiều hơn số hạt không mang điện là 10. Số hiệu nguyên tử của nguyên tố X là ?
A. 14
B. 12
C. 11
D. 23
Cho các thông tin sau: Ion
X
2
-
có cấu trúc electron:
1
s
2
2
s
2
2
p
6
3
s
2
3
p
6
Nguyên tố Y có tổng số hạt cơ bản trong nguyên tử là 40. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là...
Đọc tiếp
Cho các thông tin sau:
Ion X 2 - có cấu trúc electron: 1 s 2 2 s 2 2 p 6 3 s 2 3 p 6
Nguyên tố Y có tổng số hạt cơ bản trong nguyên tử là 40. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 12.
Ion Z 2 + có tổng số hạt mang điện tích dương trong hạt nhân bằng 29.
Vị trí của X, Y, Z trong bảng tuần hoàn lần lượt là:
A. (X: ô 16, chu kỳ 3, nhóm VIA); ( Y: ô 13, chu kì 3, nhóm IIIA); (Z: ô 29, chu kì 4, nhóm IB).
B. (X: ô 16, chu kỳ 3, nhóm VIA); (Y: ô 13, chu kì 3, nhóm IA); (Z: ô 29, chu kì 4, nhóm IIB).
C. (X: ô 20, chu kỳ 4, nhóm IIA); (Y: ô 13, chu kì 3, nhóm IIIA); (Z: ô 29, chu kì 4, nhóm IB).
D. (X: ô 16, chu kỳ 3, nhóm VIA); ( Y: ô 13, chu kì 3, nhóm IIIA); (Z: ô 31, chu kì 4, nhóm IIIA).
tổng số hạt cơ bản trong nguyên tử X là 40 trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 20 xác định kí hiệu nguyên tử X xác định số lớp electron của nguyên tử X
Z=(S+a)/4=(40+20)/4=15 suy ra photpho. Photpho có 3 lớp e. Lớp thứ nhất có 2 e, lớp thứ 2 có 8 e, lớp thứ 3 có 5 e.
Đúng 0
Bình luận (0)
Anion
X
2
-
có tổng số hạt cơ bản là 50, trong nguyên tử X thì số hạt mang điện nhiều hơn số hạt không mang điện là 16. Cấu hình electron của
X
2
-
là:
Đọc tiếp
Anion X 2 - có tổng số hạt cơ bản là 50, trong nguyên tử X thì số hạt mang điện nhiều hơn số hạt không mang điện là 16. Cấu hình electron của X 2 - là:
![]()
![]()
![]()
![]()
Một bài tập khá đơn giản, dễ dàng nhận thấy đây là dạng bài toán (2):
+ Gọi số p, n, e trong nguyên tử lần lượt là Z, N, E (nguyên dương)
+ Anion có tổng số hạt cơ bản là 50:
![]()
+ Trong nguyên tử X thì số hạt mang điện nhiều hơn số hạt không mang điện là 16: 2Z - N = 16
Từ đó ta có:
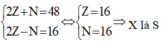
Cấu hình electron của X là: [Ne]3s23p4
Vậy cấu hình electron của S 2 - là [Ne]3s23p4
Đáp án A.
Đúng 0
Bình luận (0)
Hai nguyên tử X và Y có tổng số hạt cơ bản proton, nơtron, electron là 142. Trong đó tổng số hạt mang điện nhiều hơn số hạt không mang điện là 142. Trong đó tổng số hạt mang điệm nhiều hơn số hạt không mang điện là 42. Tỉ lệ số proton của ion X2+ và Y3+ ion là 10/13. Ở trạng thái cơ bản số electron độc thân của nguyên tử X và ion Y3+ lần lượt là A. 2 và 3 B. 0 và 4 C. 0 và 5 D. 2 và 4
Đọc tiếp
Hai nguyên tử X và Y có tổng số hạt cơ bản proton, nơtron, electron là 142. Trong đó tổng số hạt mang điện nhiều hơn số hạt không mang điện là 142. Trong đó tổng số hạt mang điệm nhiều hơn số hạt không mang điện là 42. Tỉ lệ số proton của ion X2+ và Y3+ ion là 10/13. Ở trạng thái cơ bản số electron độc thân của nguyên tử X và ion Y3+ lần lượt là
A. 2 và 3
B. 0 và 4
C. 0 và 5
D. 2 và 4
Đáp án A
Theo giả thiết ta có: 2 Z X + 2 Z Y + N X + N Y = 142 ( 2 Z X + 2 Z Y ) - ( N X + N Y ) = 42 ⇔ Z X + Z Y = 46 ( 1 ) N X + N Y = 50 ( 2 )
Mặt khác ta lại có: Tỉ lệ số proton của ion X 2 + và ion Y 3 + là 10 13 ⇒ Z X Z Y = 10 13 ( 3 )
Từ (1) và (3) ta có Z X = 20 ( C a ) v à Z Y = 26 ( F e )
X có cấu hình electron là: 1s22s22p63s23p64s2.
⇒ X có 0 electron độc thân
Fe có cấu hình là 1s22s22p63s23p63d64s2
⇒ F e 3 + có cấu hình là 1s22s22p63s23p63d5
⇒ F e 3 + có 5 electron độc thân
Chú ý: Đây là một bài khá dễ nhưng sẽ có nhiều bạn mắc phải sai lầm đáng tiếc là khi đề cho giả thiết: Tỉ lệ số proton của ion X 2 + và ion Y 3 + là 10 13
Theo quán tính sẽ có rất nhiều bạn sẽ thành lập phương trình sau: Z X - 2 Z Y - 3 = 10 13 dẫn đến không tìm ra kết quả đúng. Ở đây giả thiết cho là proton (hạt mang điện trong hạt nhân) chứ không phải electron (hạt mang điện lớp vỏ). Vì vậy trong quá trình làm bài các bạn nên đọc thật kỹ đề và không nên làm theo quán tính đọc hiểu đề và tư duy ngay cách làm.
Đúng 0
Bình luận (0)