Hỗn hợp A gồm hai kim loại X và Y . Oxi hoá hoàn toàn 15,6g hốn hợp A trong oxi dư tạo thành 28,4g hỗn hợp 2 oxit.Nếu lấy 15,6g A hoà hết trong dd HCl thì thu được V lít H2 (đktc). Tính V

Những câu hỏi liên quan
câu 1: hỗn hợp a gồm 2 kim loại x y có hóa trị không đổi. oxi hóa hoàn toàn 15,6g A trong oxi dư được 28,4g oxit,Nếu lấy 15,6g hh tác dụng hết với hỗn hợp hcl+h2so4 thì thu đc mg muối khan.tính m? câu 2: cho 100g dung dịch hno3 ,hcl tác dụng với al kim loại thu đc hỗn hợp khí h2,no,no2, có tỉ khối so với h2 là 26,3617/7. tính a) tp% theo thể tích của mỗi khí trong hh b) tính lượng al đã pư
Cho hỗn hợp X gồm A,B có hoá trị ko đổi . Oxi hoá hoàn toàn 6,3 gam hỗn hợp X trong oxi dư thu được 11,1 gam hỗn hợp hai oxit . Mặt khác nếu lấy 12,6 gam hỗn hợp X hoà tan hết trong dd HCl thì thu được V lít Khí H2 (đktc) . Tính giá trị của V
Xem chi tiết
X + O2 ---> Oxit
BKTL => mO2 = 11,1 - 6,3 = 4,8 gam <=> nO2 = 0,15 mol
O20 + 4e --> 2O-2
0,15 --- 0,6
=> số mol electron do 6,3 gam X nhường là 0,6 mol
=> số mol electron do 12,6 gam X nhường là 0,6.2 = 1,2 mol
X + HCl --> muối clorua + H2
2H+1 + 2e --> H2
1,2 ---> 0,6 mol
V H2 = 0,6.22,4 = 13,44 lít
Đúng 2
Bình luận (0)
Chia hỗn hợp gồm 2 kim loại X, Y có hoá trị không đổi thành 2 phần bằng nhau: + Phần 1: Hoà tan hoàn toàn trong dung dịch hỗn hợp gồm HCl và H2SO4 được 3,36 lít H2 (đktc). + Phần 2: Hoà tan hoàn toàn trong dung dịch HNO3 thu được V lít NO duy nhất (đktc). Giá trị của V là: A. 2,24 lít. B. 3,36 lít. C. 4,48 lít. D. 5,60 lít.
Đọc tiếp
Chia hỗn hợp gồm 2 kim loại X, Y có hoá trị không đổi thành 2 phần bằng nhau:
+ Phần 1: Hoà tan hoàn toàn trong dung dịch hỗn hợp gồm HCl và H2SO4 được 3,36 lít H2 (đktc).
+ Phần 2: Hoà tan hoàn toàn trong dung dịch HNO3 thu được V lít NO duy nhất (đktc). Giá trị của V là:
A. 2,24 lít.
B. 3,36 lít.
C. 4,48 lít.
D. 5,60 lít.
Đáp án A
Vì hai kim loại X, Y đều có hóa trị không đổi và khối lượng hai phần bằng nhau nên ở hai phần, số mol electron mà kim loại nhường bằng nhau.
Khi đó
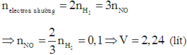
Đúng 0
Bình luận (0)
Hỗn hợp X gồm 2 kim loại A,B có hoá trị không đổi và không có kim loại nào hoá trị I Lấy 7,68g hỗn hợp X chia làm 2 phần bằng nhau. Phần 1 nung trong khí oxi dư để oxi hoá hoàn toàn thu được 6g hỗn hợp gồm 2 oxit. phần 2 hoà tan hoàn toàn vào trong dd axit clohydric và axit sunfuric loãng, thu được V lít khí hidro(dktc) và đ Y ( biết cả hai kim loại đều tác dụng được với axit) Cô cạn đ Y thu được p gam
Tính V
Giá trị của p nằm trong khoảng nào
Xác định kim loại biết số mol của hỗm hợp X ứng với...
Đọc tiếp
Hỗn hợp X gồm 2 kim loại A,B có hoá trị không đổi và không có kim loại nào hoá trị I Lấy 7,68g hỗn hợp X chia làm 2 phần bằng nhau. Phần 1 nung trong khí oxi dư để oxi hoá hoàn toàn thu được 6g hỗn hợp gồm 2 oxit. phần 2 hoà tan hoàn toàn vào trong dd axit clohydric và axit sunfuric loãng, thu được V lít khí hidro(dktc) và đ Y ( biết cả hai kim loại đều tác dụng được với axit) Cô cạn đ Y thu được p gam Tính V Giá trị của p nằm trong khoảng nào Xác định kim loại biết số mol của hỗm hợp X ứng với mỗi phần nói trên là 0,1 mol và khối lượng nguyên tử A và B đều lớn hoen 20dvC
Đốt cháy hoàn toàn m gam hỗn hợp A gồm Mg, Al,Cu trong oxi dư thu được hỗn hợp ba oxit cs khối lượng là 1,72.m gam. mặt khác, đem hoà tan m gam A bằng đ Hcl dư thấy thoát ra 0,953.m lít khí H2 ở đktc. Tính thành phần % mỗi kim loại trong A
\(n_{H_2}=\dfrac{0,953m}{22,4}=0,042545m\left(mol\right)\\ Đặt:n_{Mg}=x\left(mol\right);n_{Al}=y\left(mol\right);n_{Cu}=z\left(mol\right)\left(x,y,z>0\right)\\\Rightarrow \left\{{}\begin{matrix}24x+27y+64z=m\\40x+51y+80z=1,72m\\x+1,5y=0,042545m\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}x\approx0,012845m\\y\approx0,0198m\\z\approx0,002455m\end{matrix}\right.\\ \Rightarrow\%m_{Cu}\approx\dfrac{0,002455.64m}{m}.100\%\approx15,712\%\\ \%m_{Al}\approx\dfrac{27.0,0198m}{m}.100\%\approx53,46\%\\ \%m_{Mg}\approx\dfrac{0,012845.24m}{m}.100\%\approx30,828\%\)
Đúng 1
Bình luận (0)
Chia hỗn hợp gồm 2 kim loại X, Y có hoá trị không đổi thành 2 phần bằng nhau: Phần 1: Hoà tan hoàn toàn trong dung dịch hỗn hợp gồm HCl và H2SO4 thu được 3,36 lít H₂(ở đktc). Phần 2: Hoà tan hoàn toàn trong dung dịch HNO3 thu được V lít NO duy nhất (ở đktc). Giá trị của V
Chia hỗn hợp X gồm K, Al và Fe thành hai phần bằng nhau.- Cho phần 1 vào dung dịch KOH (dư) thu được 0,784 lít khí
H
2
(đktc).- Cho phần 2 vào một lượng dư
H
2
O
, thu được 0,448 lít khí
H
2
(đktc) và m gam hỗn hợp kim loại Y. Hoà tan hoàn toàn Y vào dung dịch HCl (dư) thu được 0,56 lít khí
H
2
(đktc). Tính khối lượng mỗi kim loại trong mỗi phần.
Đọc tiếp
Chia hỗn hợp X gồm K, Al và Fe thành hai phần bằng nhau.
- Cho phần 1 vào dung dịch KOH (dư) thu được 0,784 lít khí H 2 (đktc).
- Cho phần 2 vào một lượng dư H 2 O , thu được 0,448 lít khí H 2 (đktc) và m gam hỗn hợp kim loại Y. Hoà tan hoàn toàn Y vào dung dịch HCl (dư) thu được 0,56 lít khí H 2 (đktc). Tính khối lượng mỗi kim loại trong mỗi phần.
Chia 10 gam hỗn hợp gồm 2 kim loại A,B có hoá trị không đổi thành 2 phần bằng nhau. Phần 1 đốt cháy hoàn toàn cần V lít khí O2 ở đktc, thu được 5,32 gam hỗn hợp 2 oxit. Phần còn lại hoà tan hoàn toàn trong dung dịch hcl (dư) thấy có V' lít khí H2 thoát ra ở đktc và m gam muối clorua. Tính các giá trị: V, V', m?
mKL 1phần = 5gTN1: td với \(O_2\)Bảo toàn klg\(\Rightarrow m_{O_2}\)=5,32-5=0,32g\(\Rightarrow mol\) \(O_2\)=0,01 mol\(\Rightarrow\)V=0,224l\(O_2+4e\rightarrow2O_2-\)0,01 mol\(\Rightarrow\)0,04 molMol e nhận=0,04 molP2: lượng KL vẫn thế\(\Rightarrow\)mol e nhận và nhường ko đổi=0,04 mol\(2H++2e\rightarrow H_2\)0,04 mol\(\Leftarrow\)0,04 mol\(\Rightarrow\)0,02 molV'=0,02.22,4=0,448lMol \(HCl\)=2mol\(H_2\)=0,04 mol\(\Rightarrow\)\(m_{HCl}\)=1,46gBảo toàn klg=>m=5+1,46-0,02.2=6,42g
Đúng 1
Bình luận (0)
Hoà tan hết 20 gam hỗn hợp X gồm 2 kim loại trước H trong dãy hoạt động kim loại bằng dd HCl dư thấy thoát ra 4,48 lít khí đktc và dd B.
a) Cô cạn dd B thu được bao nhiêu gam muối khan?
b) Nếu nung 20 gam hỗn hợp này trong oxi dư sẽ thu được hỗn hợp oxit C. Cho C tác dụng với dd H2SO4 loãng vừa đủ thì được bao nhiêu gam muối sunfat?
a) \(n_{H_2}=0,2\left(mol\right)\)
Bảo toàn nguyên tố H : \(n_{HCl}=2n_{H_2}=0,4\left(mol\right)\)
=> \(n_{Cl^-}=0,4\left(mol\right)\)
=> \(m_{muối}=m_{KL}+m_{Cl^-}=20+0,4.35,5=34,2\left(g\right)\)
Đúng 2
Bình luận (1)


















