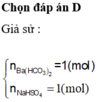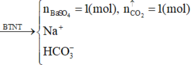Dung dịch X chứa BaCl2 0.05M và HCl 0.1M .Bỏ qua sự điện li của nước a. viết pt điện li của các chất trong X b.Tính nồng độ số mol/l của các ion trong x c. Tính thể tích dung dịch AgNO3 0.2M tác dụng với X để thu được kết tủa tối đa

Những câu hỏi liên quan
Dung dịch X chứa Bacl2 0.05M và HCl 0.10M Bỏ qua sự điện li của nước a, viết phương trình điện li của các chất trong X b, tính. Nồng độ mol/l của các ion trong X
1) \(BaCl_2\) 0,05M \(BaCl_2\rightarrow Ba^{2+}+2Cl^-\)
\(\left[Ba^{2+}\right]=0,05M\)
\(\left[Cl^-\right]=0,1M\)
2) \(HCl\) 0,1M \(HCl\rightarrow H^++Cl^-\)
\(\left[H^+\right]=0,1M\)
\(\left[Cl^-\right]=0,1M\)
Đúng 1
Bình luận (0)
dung dịch X chứa BaCl2 0,05M và HCl 0,10M. Bỏ qua sự điện li của nước.
a. Viết phương trình điệ li của các chất trong X
b. Tính nồng độ mol/l của các ion trong X
a)\(BaCl_2\rightarrow Ba^{2+}+2Cl^-\)
0,05 0,05 0,1
\(\left[Ba^{2+}\right]=0,05M\)
\(\left[Cl^-\right]=0,1M\)
b)\(HCl\rightarrow H^++Cl^-\)
0,1 0,1 0,1
\(\left[H^+\right]=0,1M\)
\(\left[Cl^-\right]=0,1M\)
Đúng 1
Bình luận (0)
Trộn hai dung dịch
Ba
HCO
3
2
và
NaHSO
4
có cùng nồng độ mol với nhau theo tỉ lệ thể tích 1 : 1 thu được kết tủa và dung dịch. Bỏ qua sự thủy phân của các ion và sự điện li của nước, các ion có mặt trong dung dịch Y là A.
Na
+
,
SO
4
2...
Đọc tiếp
Trộn hai dung dịch Ba HCO 3 2 và NaHSO 4 có cùng nồng độ mol với nhau theo tỉ lệ thể tích 1 : 1 thu được kết tủa và dung dịch. Bỏ qua sự thủy phân của các ion và sự điện li của nước, các ion có mặt trong dung dịch Y là
A. Na + , SO 4 2 -
B. Ba 2 + , HCO 3 2 - , Na +
C. HCO 3 2 - , Na +
D. SO 4 2 - , HCO 3 2 - , Na +
Đáp án C
Ba(HCO3)2 + NaHSO4® BaSO4 ↓+ NaHCO3 + CO2 ↑+ H2O
Vậy sau phản ứng, trong dung dịch còn lại các ion Na+ và HCO3-.
Đúng 0
Bình luận (0)
Trộn 2 dung dịch:
B
a
H
C
O
3
2
,
N
a
H
S
O
4
có cùng nồng độ mol/l với nhau theo tỉ lệ thể tích 1: 1 thu được kết tủa X và dung dịch Y. Hãy cho biết các ion có mặt trong dung dịch Y. (Bỏ qua sự thủy phân của các ion và sự điện ly của...
Đọc tiếp
Trộn 2 dung dịch: B a H C O 3 2 , N a H S O 4 có cùng nồng độ mol/l với nhau theo tỉ lệ thể tích 1: 1 thu được kết tủa X và dung dịch Y. Hãy cho biết các ion có mặt trong dung dịch Y. (Bỏ qua sự thủy phân của các ion và sự điện ly của nước).
A. N a + , H C O 3 - v à S O 4 2 - .
B. B a 2 + , H C O 3 - v à N a + .
C. N a + , H C O 3 - .
D. N a + v à S O 4 2 - .
Trộn 2 dung dịch: Ba(HCO3)2; NaHSO4 có cùng nồng độ mol/l với nhau theo tỉ lệ thể tích 1:1 thu được kết tủa X và dung dịch Y. Hãy cho biết các ion có mặt trong dung dịch Y. (Bỏ qua sự thủy phân của các ion và sự điện ly của nước).
Đọc tiếp
Trộn 2 dung dịch: Ba(HCO3)2; NaHSO4 có cùng nồng độ mol/l với nhau theo tỉ lệ thể tích 1:1 thu được kết tủa X và dung dịch Y. Hãy cho biết các ion có mặt trong dung dịch Y. (Bỏ qua sự thủy phân của các ion và sự điện ly của nước).
![]()
![]()
![]()
![]()
Trộn 2 dung dịch: Ba(HCO3)2 ; NaHSO4 có cùng nồng độ mol/l với nhau theo tỷ lệ thể tích 1: 1 thu được kết tủa X và dung dịch Y. Hãy cho biết các ion có mặt trong dung dịch Y. ( Bỏ qua sự thủy phân của các ion và sự điện ly của nước). A. Na+, HCO3- và SO42- B. Ba2+, HCO3- và Na+ C. Na+ và SO42- D. Na+, HCO3-
Đọc tiếp
Trộn 2 dung dịch: Ba(HCO3)2 ; NaHSO4 có cùng nồng độ mol/l với nhau theo tỷ lệ thể tích 1: 1 thu được kết tủa X và dung dịch Y. Hãy cho biết các ion có mặt trong dung dịch Y. ( Bỏ qua sự thủy phân của các ion và sự điện ly của nước).
A. Na+, HCO3- và SO42-
B. Ba2+, HCO3- và Na+
C. Na+ và SO42-
D. Na+, HCO3-
Trộn 2 dung dịch: Ba(HCO3)2; NaHSO4 có cùng nồng độ mol/l với nhau theo tỉ lệ thể tích 1: 1 thu được kết tủa X và dung dịch Y. Hãy cho biết các ion có mặt trong dung dịch Y. (Bỏ qua sự thủy phân của các ion và sự điện ly của nước) A. Na+ và SO42-. B. Ba2+, HCO-3 và Na+ . C. Na+, HCO3-. D. Na+, HCO-3 và SO42-.
Đọc tiếp
Trộn 2 dung dịch: Ba(HCO3)2; NaHSO4 có cùng nồng độ mol/l với nhau theo tỉ lệ thể tích 1: 1 thu được kết tủa X và dung dịch Y. Hãy cho biết các ion có mặt trong dung dịch Y. (Bỏ qua sự thủy phân của các ion và sự điện ly của nước)
A. Na+ và SO42-.
B. Ba2+, HCO-3 và Na+ .
C. Na+, HCO3-.
D. Na+, HCO-3 và SO42-.
Trộn 2 dung dịch: Ba(HCO3)2 ; NaHSO4 có cùng nồng độ mol/l với nhau theo tỷ lệ thể tích 1: 1 thu được kết tủa X và dung dịch Y. Hãy cho biết các ion có mặt trong dung dịch Y. ( Bỏ qua sự thủy phân của các ion và sự điện ly của nước). A. Na+, HCO3- và SO42-. B. Na+, HCO3- . C. Ba2+, HCO3- và Na+. D. Na+ và SO42
Đọc tiếp
Trộn 2 dung dịch: Ba(HCO3)2 ; NaHSO4 có cùng nồng độ mol/l với nhau theo tỷ lệ thể tích 1: 1 thu được kết tủa X và dung dịch Y. Hãy cho biết các ion có mặt trong dung dịch Y. ( Bỏ qua sự thủy phân của các ion và sự điện ly của nước).
A. Na+, HCO3- và SO42-.
B. Na+, HCO3- .
C. Ba2+, HCO3- và Na+.
D. Na+ và SO42
Đáp án : B
Theo tỉ lệ pha thì trước khi phản ứng trong dung dịch sẽ có giả sử :
1 mol Ba2+ ; 2 mol HCO3- ; 1 mol Na+ ; 1 mol HSO4-
HCO3- + HSO4- à CO2 + SO42-
SO42- + Ba2+ à BaSO4
=> Trong dung dịch lúc này còn HCO3- và Na+
Đúng 0
Bình luận (0)
Cho 2 dung dịch HCl và CH3COOH có cùng nồng độ. Dung dịch HCl có pH x, dung dịch CH3COOH có pH y. Bỏ qua sự điện li của nước, các dung dịch ở cùng nhiệt độ phòng. Biết ở nhiệt độ phòng, cứ 100 phân tử CH3COOH thì có 1 phân tử phân li ra ion. Mối liên hệ của x và y là: A. x y - 2 B. y x – 2 C. x 2y D. y 2x
Đọc tiếp
Cho 2 dung dịch HCl và CH3COOH có cùng nồng độ. Dung dịch HCl có pH = x, dung dịch CH3COOH có pH = y. Bỏ qua sự điện li của nước, các dung dịch ở cùng nhiệt độ phòng. Biết ở nhiệt độ phòng, cứ 100 phân tử CH3COOH thì có 1 phân tử phân li ra ion. Mối liên hệ của x và y là:
A. x = y - 2
B. y = x – 2
C. x = 2y
D. y = 2x
Không mất tính tổng quát, ta đặt:
![]()
Vì HCl là chất điện li mạnh nên ta có phương trình điện li như sau:
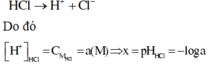
Vì CH3COOH là chất điện li yếu nên ta có phương trình điện li như sau
Xét cân bằng điện li: CH3COOH ⇌ CH3COO- + H+
Nồng độ ban đầu: aM 0
Nồng độ phân li: 0,01a M → 0,01a M
Nồng độ cân bằng: 0,99a M 0,01a M
Ta có
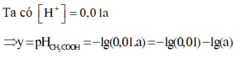
![]()
Đáp án A.
Đúng 0
Bình luận (0)