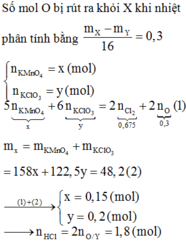45. Hoà tan hoàn toàn 61g hỗn hợp KMNO4 và K2CR2O7 vào dd HCl đặc , dư. Sau phản ứng thu đc 17,92 lít khí Cl2(ở đktc) . Thành phần % số mol KMnO4 và K2CR2O7 trong hỗn hợp ban đầu lần lượt là?

Những câu hỏi liên quan
45. Hoà tan hoàn toàn 61 gam hỗn hợp KMNO4 và K2CR2O7 vào dd HCl đặc , dư. Sau phản ứng thu đc 17,92 lít khí Cl2(đktc). Thành phần % số mol KMnO4 và K2CR2O7 trong hỗn hợp ban đầu lần lượt là?
46. Hoà tan hoàn toàn 24,5g hỗn hợp KMNO4 và MnO2 vào dd HCl đặc , dư , đun nóng. Sau phản ứng thu đc 2,87 lít khí Cl2( ở 27°C và 3atm). Thành phần % khối lượng mỗi chất trong hỗn hợp ban đầu là?
Câu 1:
Gọi \(\left\{{}\begin{matrix}n_{KMnO4}:x\left(mol\right)\\n_{K2Cr2O7}:y\left(mol\right)\end{matrix}\right.\)
Ta có:
\(n_{Cl2}=\frac{17,92}{22,4}=0,8\left(mol\right)\)
\(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
\(K_2Cr_2O_7+14HCl\rightarrow2KCl+2CrCl_3+3Cl_2+7H_2O\)
Giải hệ PT:
\(\left\{{}\begin{matrix}158x+294y=61\\\frac{5}{2}x+3y=0,8\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%n_{KMnO4}=\frac{0,2}{0,3}.100\%=66,67\%\\\%n_{K2Cr2O7}=100\%-66,67\%=33,33\%\end{matrix}\right.\)
Câu 2:
Gọi \(\left\{{}\begin{matrix}n_{KMnO4}:x\left(mol\right)\\n_{MnO2}:y\left(mol\right)\end{matrix}\right.\)
Ta có:
\(n_{Cl2}=\frac{2,87.3}{0,082.\left(27+273\right)}=0,35\left(mol\right)\)
Giải hệ PT:
\(\left\{{}\begin{matrix}158x+87y=24,5\\5x+2y=2n_{Cl2}=0,7\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{KMnO4}=\frac{0,1.158}{24,5}.100\%=64,5\%\\\%m_{MnO2}=100\%-64,5\%=35,5\%\end{matrix}\right.\)
Đúng 0
Bình luận (0)
44. Cho m gam KCLO3 tác dụng với dd HCl đặc dư, đun nóng thì thu đc V lót Cl2(đktc). Hấp thụ hết V lít khí Clo ở trên vào dd KOH vừa đủ, đun nóng thì thu đc dd chứa 17,433g muối clorua. Biết hiệu suất của pư điều chế là 75%. Giá trị m là?
A. 5,733g
B. 7,644g
C. 7,301g
D. 9,735g
45. Hoà tan hoàn toàn 61g hỗn hợp Kmno4 và K2CR2O7 vào dd HCl đặc , dư. Sau phản ứng thu đc 17,92lit khí Cl2(đktc). Thành phần % số mol KMnO4 và K2CR2O7 trong hỗn hợp ban đầu lần lượt là?
Đọc tiếp
44. Cho m gam KCLO3 tác dụng với dd HCl đặc dư, đun nóng thì thu đc V lót Cl2(đktc). Hấp thụ hết V lít khí Clo ở trên vào dd KOH vừa đủ, đun nóng thì thu đc dd chứa 17,433g muối clorua. Biết hiệu suất của pư điều chế là 75%. Giá trị m là?
A. 5,733g
B. 7,644g
C. 7,301g
D. 9,735g
45. Hoà tan hoàn toàn 61g hỗn hợp Kmno4 và K2CR2O7 vào dd HCl đặc , dư. Sau phản ứng thu đc 17,92lit khí Cl2(đktc). Thành phần % số mol KMnO4 và K2CR2O7 trong hỗn hợp ban đầu lần lượt là?
Câu 44
Phản ứng điều chế là KClO3 vs HCl
\(n_{KCl}=\frac{17,433}{74,5}=0,234\left(mol\right)\)
\(KClO_3+6HCl\rightarrow KCl+3Cl_2+3H_2O\)
0,0624_______________0,1872________
\(3Cl_2+6KOH\rightarrow KClO_3+5KCl+3H_2O\)
0,1404__________________0,234__________
\(n_{Cl\left(lt\right)}=\frac{0,1404}{75\%}=0,1872\left(mol\right)\)
\(\Rightarrow m_{KClO3}=0,0624.122,5=7,644\)
Câu 45
\(n_{Cl2}=\frac{17,92}{22,4}=0,8\left(mol\right)\)
Gọi số mol KMnO4;K2Cr2O7 lần lượt là a;ba;b
Phản ứng xảy ra:
\(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+6H_2O\)
\(14HCl+K_2Cr_2O_7\rightarrow2KCl+2CrCl_3+3Cl_2+7H_2O\)
Ta có hệ phương trình:
\(\left\{{}\begin{matrix}158x+194y=61\\2,4x+3y=0,8\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,2\left(mol\right)\\y=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n\%_{KMnO4}=\frac{0,2}{01+0,2}.100\%=66,67\%\)
\(\Rightarrow\%n_{K2Cr2O7}=100\%-66,67\%=33,33\%\)
Hòa tan hoàn toàn m gam hỗn hợp E gồm: KMnO4, K2Cr2O7, K2MnO4, MnO2, PbO2 ( các chất trong E có số mol bằng nhau) bằng dung dịch HCl (đặc nóng). Sau phản ứng thu được (m + 11,856) gam hỗn hợp muối X ( X gồm: KCl, MnCl2, CrCl3, PbCl2) và a mol khí Cl2. Giá trị a là?A. 0,302. B. 0,304. C. 0,305. D. 0,306.Mọi người giúp mình với! Thanks you very much!
Đọc tiếp
Hòa tan hoàn toàn m gam hỗn hợp E gồm: KMnO4, K2Cr2O7, K2MnO4, MnO2, PbO2 ( các chất trong E có số mol bằng nhau) bằng dung dịch HCl (đặc nóng). Sau phản ứng thu được (m + 11,856) gam hỗn hợp muối X ( X gồm: KCl, MnCl2, CrCl3, PbCl2) và a mol khí Cl2. Giá trị a là?
A. 0,302. B. 0,304. C. 0,305. D. 0,306.
Mọi người giúp mình với! Thanks you very much!
Gọi :
\(n_{KMnO_4} = n_{K_2Cr_2O_7} = n_{K_2MnO_4} = n_{MnO_2} = n_{PbO_2} = x(mol)\)
Suy ra : 975x = m(1)
Bảo toàn nguyên tố với K,Mn,Cr,Pb ,Muối gồm :
\(\left\{{}\begin{matrix}KCl:x+2x+2x=5x\left(mol\right)\\MnCl_2:x+x+x=3x\left(mol\right)\\CrCl_3:2x\left(mol\right)\\PbCl_2:x\left(mol\right)\end{matrix}\right.\)
Suy ra : 1345,5x = m + 11,856(2)
Từ (1)(2) suy ra : m = 31,2 ; x = 0,032
Bảo toàn electron :
\(5n_{KMnO_4} + 6n_{K_2Cr_2O_7} + 4n_{K_2MnO_4} + 2n_{MnO_2} + 2n_{PbO_2} = 2n_{Cl_2}\)
Suy ra :
\(a = \dfrac{0,032.5+0,032.6 + 0,032.4 + 0,032.2 + 0,032.2}{2} = 0,304(mol)\)
(Đáp án B)
Đúng 8
Bình luận (0)
Đun nóng 48,2 g hỗn hợp KMnO4, KClO3, sau một thời gian thu được 43,4 gam hỗn hợp chất rắn Y. Cho Y tác dụng hoàn toàn với dung dịch HCl đặc, sau phản ứng thu đc 15,12 lít Cl2 (đktc) và dung dịch gồm MnCl2, KCl, HCl dư. Số mol HCl phản ứng là A. 1,9 B. 2,4 C. 2,1 D. 1,8
Đọc tiếp
Đun nóng 48,2 g hỗn hợp KMnO4, KClO3, sau một thời gian thu được 43,4 gam hỗn hợp chất rắn Y. Cho Y tác dụng hoàn toàn với dung dịch HCl đặc, sau phản ứng thu đc 15,12 lít Cl2 (đktc) và dung dịch gồm MnCl2, KCl, HCl dư. Số mol HCl phản ứng là
A. 1,9
B. 2,4
C. 2,1
D. 1,8
Đáp án D
Đặt a, b là số mol KMnO4 và KClO3 ban đầu
=> 158a + 122,5b = 48,2 (1)
nO (X) = 4a + 3b
=> nO(Y) = 4a + 3b – 0,3
=> nHCl = 2nH2O = 2 (4a + 3b – 0,3)
Dung dịch thu được chứa KCl ( a + b) ; MnCl2 ( a)
Bảo toàn nguyên tố Cl: b + 2( 4a + 3b – 0,3) = a + b + 2a + 2.0,675 (2)
Từ ( 1) và (2) => a = 0,15 và b = 0,2
=> nHCl = 1,8 mol
Đúng 0
Bình luận (0)
Đun nóng 48,2 g hỗn hợp KMnO4, KClO3, sau một thời gian thu được 43,4 gam hỗn hợp chất rắn Y. Cho Y tác dụng hoàn toàn với dung dịch HCl đặc, sau phản ứng thu đc 15,12 lít Cl2 (đktc) và dung dịch gồm MnCl2, KCl, HCl dư. Số mol HCl phản ứng là A. 1,9. B. 2,4. C. 2,1. D. 1,8
Đọc tiếp
Đun nóng 48,2 g hỗn hợp KMnO4, KClO3, sau một thời gian thu được 43,4 gam hỗn hợp chất rắn Y. Cho Y tác dụng hoàn toàn với dung dịch HCl đặc, sau phản ứng thu đc 15,12 lít Cl2 (đktc) và dung dịch gồm MnCl2, KCl, HCl dư. Số mol HCl phản ứng là
A. 1,9.
B. 2,4.
C. 2,1.
D. 1,8
Chọn D
Đặt a, b là số mol KMnO4 và KClO3 ban đầu
=> 158a + 122,5b = 48,2 (1)
nO (X) = 4a + 3b
=> nO(Y) = 4a + 3b – 0,3
=> nHCl = 2nH2O = 2 (4a + 3b – 0,3)
Dung dịch thu được chứa KCl ( a + b) ; MnCl2 ( a)
Bảo toàn nguyên tố Cl: b + 2( 4a + 3b – 0,3) = a + b + 2a + 2.0,675 (2)
Từ ( 1) và (2) => a = 0,15 và b = 0,2
=> nHCl = 1,8 mol
Đúng 0
Bình luận (0)
Đun nóng 48,2 g hỗn hợp KMnO4, KClO3, sau một thời gian thu được 43,4 gam hỗn hợp chất rắn Y. Cho Y tác dụng hoàn toàn với dung dịch HCl đặc, sau phản ứng thu đc 15,12 lít Cl2 (đktc) và dung dịch gồm MnCl2, KCl, HCl dư. Số mol HCl phản ứng là A. 1,9. B. 2,4. C. 2,1. D. 1,8.
Đọc tiếp
Đun nóng 48,2 g hỗn hợp KMnO4, KClO3, sau một thời gian thu được 43,4 gam hỗn hợp chất rắn Y. Cho Y tác dụng hoàn toàn với dung dịch HCl đặc, sau phản ứng thu đc 15,12 lít Cl2 (đktc) và dung dịch gồm MnCl2, KCl, HCl dư. Số mol HCl phản ứng là
A. 1,9.
B. 2,4.
C. 2,1.
D. 1,8.
Đáp án D
Đặt a, b là số mol KMnO4 và KClO3 ban đầu
=> 158a + 122,5b = 48,2 (1)
nO (X) = 4a + 3b
=> nO(Y) = 4a + 3b – 0,3
=> nHCl = 2nH2O = 2 (4a + 3b – 0,3)
Dung dịch thu được chứa KCl
( a + b) ; MnCl2 ( a)
Bảo toàn nguyên tố Cl:
b + 2( 4a + 3b – 0,3) = a + b + 2a + 2.0,675 (2)
Từ ( 1) và (2) => a = 0,15 và b = 0,2
=> nHCl = 1,8 mol
Đúng 0
Bình luận (1)
Cho m gam hỗn hợp X gồm Kmno4,MnO2,K2Cr2O7 tác dụng dung dịch HCl( đặc) lấy dư đun nóng,thu được dd Y có 2,1168 lít khí Cl2 thoát ra, số mol HCl đã phản ứng là 0,39 mol .Cô cạn cẩn thận dd Y thu được a gam muối khan, cho a gam muối trên tác dụng dd AgNO3 dư thu được x gam muối kết tỉa.Các phản ứng xảy ra hoàn toàn.Giá trị của x là?
\(n_{Cl_2}=\dfrac{2,1168}{22,4}=0,0945\left(mol\right)\)
=> nCl(muối) = 0,39 - 0,0945 = 0,201 (mol)
=> nAgCl = 0,201 (mol)
=> mAgCl = 0,201.143,5 = 28,8435 (g)
Đúng 2
Bình luận (0)
Đun nóng 48,2gam hỗn hợp X gồm KMnO4 và KClO3 sau một thời gian thu được 43,4gam hỗn hợp chất rắn Y. Cho Y tác dụng hoàn toàn với dung dịch HCl đặc, đun nóng, sau phản ứng thu được 15,12 lít khí clo (đktc) và dd Z gồm các chất tan MnCl2, KCl, HCl dư. Tính thành phần % về khối lượng của các chất trong hỗn hợp X.
Gọi số mol KMnO4 và KClO3 trong hỗn hợp ban đầu lần lượt là x,y
158x + 122,5y= 48,2 (1)
Bảo toàn elcton toàn quá trình ta có
Mn+7+5e →Mn+2
x 5x
Cl+5 + 6e → Cl–1
y 6y
(về bản chất có 1 phần Cl+5 có 1 phần chuyển sang Cl0, nhưng Cl–1 lại nhường e tạo Cl0 vì vậy để đơn giản ta có thể coi tất cả Cl+5 tạo thành Cl–1)
2Cl–1→ Cl2 +2e
0,675 0,135
2O–2 → O2 + 4e
0,15 0,6
Áp dụng định luật bảo toàn e ta có 5x+6y=1,95 (2)
Từ 1 và 2 ta có hệ phương trình
Giải ta được x=0,15 và y=0,2
% mKMnO4 = 49,17 % và % mKClO3 =50,83%
Đúng 0
Bình luận (0)
Đun nóng 48,2 gam hỗn hợp X gồm KMnO4 và KClO3, sau một thời gian thu được 43,4 gam hỗn hợp chất rắn Y. Cho Y tác dụng hoàn toàn với dung dịch HCl đặc, sau phản ứng thu được 15,12 lít Cl2 (đktc) và dung dịch gồm MnCl2, KCl và HCl dư. Số mol HCl phản ứng là A. 1,9 B. 2,4 C. 1,8 D. 2,1
Đọc tiếp
Đun nóng 48,2 gam hỗn hợp X gồm KMnO4 và KClO3, sau một thời gian thu được 43,4 gam hỗn hợp chất rắn Y. Cho Y tác dụng hoàn toàn với dung dịch HCl đặc, sau phản ứng thu được 15,12 lít Cl2 (đktc) và dung dịch gồm MnCl2, KCl và HCl dư. Số mol HCl phản ứng là
A. 1,9
B. 2,4
C. 1,8
D. 2,1