Hỗn hợp X gồm Ba và Na. Cho 6,4g X vào b gam nước thu đc 1,344 lít khí H2(ở đktc) và dd Y chứa 2 chất tan. Biết nồng độ của Ba(OH)2 trong dd Y là 3,42%
a. Viết PTHH của các phản ứng xảy ra
b. Tính b và nồng độ phần trăm(C%) của NaOH trong dd Y
Hòa tan hoàn toàn 5,49 gam hỗn hợp A gồm Na, Ba vào nước được dd B và 1,344 lít khí H2. Sục V lít khí CO2 vào dd B thì thu được lượng kết tủa lớn nhất. Tính V ( biết các khí đo ở đktc )
Gọi $n_{Na} = a(mol) ; n_{Ba} = b(mol) \Rightarrow 23a + 137b = 5,49(1)$
$2Na + 2H_2O \to 2NaOH + H_2$
$Ba + 2H_2O \to Ba(OH)_2 + H_2$
$n_{H_2} = 0,5a + b = \dfrac{1,344}{22,4} = 0,06(2)$
Từ (1)(2) suy ra a = 0,06 ; b = 0,03
$CO_2 + Ba(OH)_2 \to BaCO_3 + H_2O$
$n_{CO_2} = n_{Ba(OH)_2} = 0,03 \Rightarrow V = 0,03.22,4 = 0,672(lít)$
Hòa tan 4,4 gam hỗn hợp gồm Mg vag MgO bằng một lượng dd H2SO4 loãng có nồng độ 19,6%, sau phản ứng, thu được 2,24 lít khí H2(ở đktc)
a) Viết PTHH của các phản ứng xảy ra?
b) Tính kl mỗi chất có trong hỗn hợp ban đầu
c) Tính kl dd H2SO4 cần dùng để hòa tan hỗn hợp
a, \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
\(MgO+H_2SO_4\rightarrow MgSO_4+H_2O\)
b, \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Theo PT: \(n_{Mg}=n_{H_2}=0,1\left(mol\right)\Rightarrow m_{Mg}=0,1.24=2,4\left(g\right)\)
\(\Rightarrow m_{MgO}=4,4-2,4=2\left(g\right)\)
c, \(n_{MgO}=\dfrac{2}{40}=0,05\left(mol\right)\)
Theo PT: \(n_{H_2SO_4}=n_{Mg}+n_{MgO}=0,15\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4}=0,15.98=14,7\left(g\right)\)
\(\Rightarrow m_{ddH_2SO_4}=\dfrac{14,7}{19,6\%}=75\left(g\right)\)
Hỗn hợp X gồm Na và Ba trong đó Na chiếm 14,375% về khối lượng. Hòa tan hoàn toàn m gam X vào nước thu được 1,344 lít khí H2 (đktc) và dung dịch Y. Hấp thụ hoàn toàn 2,016 lít khí CO2 (đktc) vào dung dịch Y. Các phản ứng xảy ra hoàn toàn. Khối lượng kết tủa thu được là:
A. 7,88 gam
B. 2,14 gam
C. 5,91 gam
D. 3,94 gam
Đáp án C
Ba+ 2H2O → Ba(OH)2+ H2
Na + H2O → NaOH + ½ H2
Đặt nBa = x mol; nNa = y mol → mhỗn hợp = 137x + 23y
→ % m N a = 23 y 137 x + 23 y . 100 % = 14 , 375 %
n H 2 = x+ ½ y =1,344/22,4 = 0,06mol ; n O H - = 2. n H 2 = 0,12 mol; n C O 2 = 0,09 mol
Giải hệ trên ta có: x = 0,04 mol; y = 0,04 mol
ta thấy : T = n O H - n C O 2 = 0 , 12 0 , 09 = 1 , 333 → CO2 phản ứng với OH- theo PT sau:
CO2 + OH- → HCO3-
a a a mol
CO2 + 2OH- → CO32- + H2O
b 2b b mol
Có n C O 2 = a+ b = 0,09 mol;
n O H - = a+ 2b = 0,12 suy ra a = 0,06 mol; b = 0,03 mol
Ba2+ + CO32- → BaCO3↓
0,04 0,03 mol 0,03 mol
m B a C O 3 = 0,03. 197 = 5,91(gam)
Hoà tan 6,13g hỗn hợp D gồm Na,K,Ba và Al2O3(trong đó nguyên tố oxi chiếm 23,491% về khối lượng) vào nước dư,đến khi phản ứng xảy ra hoàn toàn thì thu đc dd G và 1,456 lít khí H2(đktc).Cho 1,6 lít dd HCl 0,1M vào G thì thu đc dd F và m gam kết tủa
a)xác định giá trị của m
b)Tính khối longwj chất tan trong dd F
a)
n O = 6,13.23,491%/16 = 0,09(mol)
=> n Al2O3 = 1/3 n O = 0,03(mol)
n H2 = 1,456/22,4 = 0,065(mol)
$H_2O \to OH^- + \dfrac{1}{2}H_2$
Suy ra: n OH = 2n H2 = 0,065.2 = 0,13(mol)
Al2O3 + 2OH- → 2AlO2- + H2O
0,03......0,06..........0,06.....................(mol)
DUng dịch G có :
AlO2- : 0,06
OH- : 0,13 - 0,06 = 0,07(mol)
Áp dụng CT :
n H+ = 4n AlO2- + n OH- - 3n Al(OH)3
<=> 0,16 = 0,06.4 + 0,07 - 3n Al(OH)3
<=> n Al(OH)3 = 0,05(mol)
<=> m = 0,05.78 = 3,9(gam)
Trong F :
m Na + m K + m Ba = m D - m Al2O3 = 6,13 - 0,03.102 = 3,07(gam)
n Cl = n HCl = 0,16(mol)
n Al3+ = 0,06 - 0,05 = 0,01(mol)
=> m chất tan = 3,07 + 0,16.35,5 + 0,01.27 = 9,02(gam)
Câu1: 10g hỗn hợp X gồm Na và Na₂O tác dụng hoàn toàn với nước thu đc 2 lít dd A và 3,36 lít khí H₂ (đktc)
a) Viết các PTHH xảy ra
b) Tính % khối lượng các chất có trong hỗn hợp X
c) Tính nồng độ mol/lít của dd A
Câu 2: Cho 7,2g kim loại hóa trị II phản ứng hoàn toàn với 100ml dd HCl 6M. Tìm tên kim loại.
Hỗn hợp X gồm Na, Ba, Na2O, BaO. Hòa tan hoàn toàn 21,9g X vào nước, thu đc 1,12 lít H2 ( đktc) và dd Y, trong đó có 20,52g Ba(OH)2 và m gam NaOH. Tính m
Coi X gồm Na, Ba và O.
Ta có: \(n_{Ba\left(OH\right)_2}=\dfrac{20,52}{171}=0,12\left(mol\right)\)
BTNT Ba, có: nBa = nBa(OH)2 = 0,12 (mol)
Gọi: \(\left\{{}\begin{matrix}n_{Na}=x\left(mol\right)\\n_O=y\left(mol\right)\end{matrix}\right.\) ⇒ 23x + 16y = 21,9 - 0,12.137 (1)
Ta có: \(n_{H_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
BT e, có: nNa + 2nBa = 2nO + 2nH2 ⇒ x + 0,12.2 = 2y + 0,05.2 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,14\left(mol\right)\\y=0,14\left(mol\right)\end{matrix}\right.\)
BTNT Na, có: nNaOH = nNa = 0,14 (mol)
⇒ m = mNaOH = 0,14.40 = 5,6 (g)
Hòa tan m gam hỗn hợp X gồm Ba và Al vào nước dư, thu được 1,344 lít khí (đktc). Mặt khác khi cho 2m gam X tác dụng với dung dịch Ba(OH)2 dư thu được 20,832 lít khí (đktc). Biết rằng các phản ứng đều xảy ra hoàn toàn. Phần trăm khối lượng của Al trong hỗn hợp X ban đầu là:
A. 88,9%
B. 95,2%
C. 79,8%
D. 62,7%
Đáp án C
Các phản ứng xảy ra:
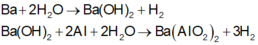
Khi cho m gam X tác dụng với dung dịch Ba (OH)2 dư thu được 20,832/2=10,416 lít H2 (đktc)
Vì thể tích H2 thu được ở hai trường hợp (khi sử dụng cùng khối lượng hỗn hợp X) khác nhau nên khi hòa tan hỗn hợp vào nước thì còn một phần kim loại Al dư không tan.
Trong m gam X gọi n Ba = a n Al = b
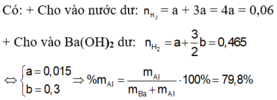
Cho 4.6 gam Na tác dụng hết với nước thu được 200 gam dd X và thấy có V lít khí H2 thoát ra ở đktc a) Viết PTHH xảy ra b) Tính V? c) dd X là gì/ Tính nồng độ phần trăm của dd X tạo thành
\(n_{Na}=\dfrac{4.6}{23}=0.2\left(mol\right)\)
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
\(0.2......................0.2.......0.1\)
\(V_{H_2}=0.1\cdot22.4=2.24\left(l\right)\)
Dung dịch X : NaOH
\(m_{dd_X}=4.6+200-0.1\cdot2=204.4\left(g\right)\)
\(C\%_{NaOH}=\dfrac{0.2\cdot40}{204.4}\cdot100\%=3.9\%\%\)
a) $2Na + 2H_2O \to 2NaOH + H_2$
n Na = 4,6/23 = 0,2(mol)
n H2 = 1/2 n Na = 0,1(mol)
V H2 = 0,1.22,4 = 2,24(lít)
c) Dung dịch X là dd NaOH
n NaOH = n Na = 0,2(mol)
C% NaOH = 0,2.40/200 .100% = 4%
Cho 8,63 gam hỗn hợp X gồm Na, K, Ba và Al2O3 (trong đó oxi chiếm 19,47% về khối lượng) tan hết vào nước thu được dung dịch Y và 1,344 lít khí H2 (đktc). Cho 320 ml dung dịch HCl 0,75M vào dung dịch Y, sau khi phản ứng xảy ra hoàn toàn thu được m gam kết tủa. Giá trị của m là
A. 2,73.
B. 5,46.
C. 1,04.
D. 2,34.
Đáp án D
Theo đề ta có:
![]()
Khi hòa tan hỗn hợp X bằng nước. Xét dung dịch Y ta có:
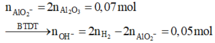
Khi cho dung dịch Y tác dụng với 0,24 mol HCl, vì: