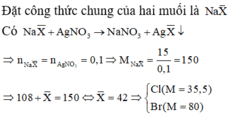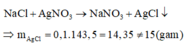1. X, Y là 2 ngto halogen thuộc 2 chu kì liên tiếp. Hỗn hợp A chứa 2 muối natri cỉa X,Y. Cho 2,2v A tác dụng vừa đủ 150ml dd AgNO3 0,2M. Tên X,Y? Hỏi khối lượng kết tủa.( giải 2 trường hợp)
2.dd chứa 6,23g hỗn hợp NaCl, NaBr, NaI. Chia làm 2 phần bằng nhau:
Phần 1: Cho tác dụng dd Brom dư thấy khối lượng muối giảm 0,47g
Phần 2 cho clo dư qua thấy khối lượng muối giảm 1,36g. Tính % khối lượng mỗi muối trong hỗn hợp trên
3. X,Y là 2 ngto halogen ơt 2 chu kì liên tiếp. Cho lượng dư AgNO3 tác dụng với dd chứa 0,015 mol NaX, NaY thu 1,435 gam kết tủa. Tên X,Y. Tính khối lượng NaX