Tính thể tích dd H2SO4 98% (D=1,84 g/ml) cần dùng để pha thành 200g dd H2SO4 loãng 9,8%

Những câu hỏi liên quan
Có 100ml dung dịch H2SO4 98%, khối lượng riêng là 1,84 g/ml. Người ta muốn pha loãng thể tích H2SO4 trên thành dung dịch H2SO4 20%.
Tính thể tích nước cần dung để pha loãng.
Thể tích nước cần dùng để pha loãng.
Khối lượng của 100ml dung dịch axit 98%
100ml × 1,84 g/ml = 184g
Khối lượng H2SO4 nguyên chất trong 100ml dung dịch trên: 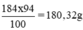
Khối lượng dung dịch axit 20% có chứa 180,32g H2SO4 nguyên chất: 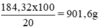
Khối lượng nước cần bổ sung vào 100ml dung dịch H2SO4 98% để có được dung dịch 20%: 901,6g – 184g = 717,6g
Vì D của nước là 1 g/ml nên thể tích nước cần bổ sung là 717,6 ml.
Đúng 1
Bình luận (0)
1)Tính thể tích dung dịch H2SO4 1M thu được khi pha loãng 30ml dug dịch H2SO4 98%(D=1,84g/ml)
2)Tính khối lượng SO3 cần dùng để khi pha vào 200g dung dịch H2SO4 9,8% thu được dung dịch H2SO4 49%
3)Tính tỉ lệ khối lượng oleum 71% SO3 cần để khi trộn với dung dịch H2SO4 nguyên chất tạo oleum 62%SO3
1. \(n_{H_2SO_4\left(98\%\right)}=\dfrac{30.1,84.98\%}{98}=0,552\left(mol\right)\)
=>\(V_{H_2SO_4\left(1M\right)}=\dfrac{0,552}{1}=0,552\left(l\right)\)
Đúng 1
Bình luận (0)
Tính thể tích dd H2SO4 98% (d = 1,83g/ml) cần dùng để pha đc 500ml dd H2SO4 0,1M. Nêu cáCh pha chế dd trên.
n H2SO4 = 0,5.0,1 = 0,05(mol)
m H2SO4 = 0,05.98 = 4,9(gam)
m dd H2SO4 = \(\dfrac{4,9}{98\%}\) = 5(gam)
V dd H2SO4 = \(\dfrac{5}{1,83}\) = 2,7322(cm3)
Đúng 2
Bình luận (1)
Tính toán và trình bày cách pha chế 0,5 lít dd H2SO4 1M từ dd H2SO4 98% có D= 1,84 g/ml
\(n_{H_2SO_4}=0.5\cdot1=0.5\left(mol\right)\)
\(m_{dd_{H_2SO_4}}=\dfrac{0.5\cdot98\cdot100}{98}=50\left(g\right)\)
\(V_{dd_{H_2SO_4}}=\dfrac{50}{1.84}=27.17\left(ml\right)=0.02717\left(l\right)\)
Đúng 4
Bình luận (0)
Sorry chút nhé , đọc thiếu đề.
Cách pha chế :
- Đong lấy 100 ml nước cất cho vào bình đựng có dung tích 1 (l) , cho từ từ 50 (g) dung dịch H2SO4 vào cốc. Rót từ từ nước cất đến vạch 0.5 (l) thì dừng lại.
Đúng 3
Bình luận (1)
Có 100 ml H2SO4 98% , khối lượng riêng là 1,84 g/ml. Nếu muốn pha loãng thể tích H2SO4 trên thành dung dịch H2SO4 20% thì cần thêm vào bao nhiêu ml nước? Bồ ơi giúp với❤
\(C\%_{sau}=0,2=\dfrac{100.1,84.0,98}{100.1,84+V_{H_2O}}\\ V_{H_2O}=717,6mL\)
Đúng 1
Bình luận (0)
Có 100ml dung dịch H2SO4 98%, khối lượng riêng là 1,84 g/ml. Người ta muốn pha loãng thể tích H2SO4 trên thành dung dịch H2SO4 20%.
Khi pha loãng phải tiến hành như thế nào?
Cách tiến hành khi pha loãng
Khi pha loãng lấy 717,6 ml H2O vào ống đong hình trụ có thể tích khoảng 2 lít. Sau đó cho từ từ 100ml H2SO4 98% vào lượng nước trên, đổ axit chảy theo một đũa thủy tinh, sau khi đổ vài giọt nên dùng đũa thủy tinh khuấy nhẹ đều. Không được đổ nước vào axit 98%, axit sẽ bắn vào da, mắt..và gây bỏng rất nặng
Đúng 0
Bình luận (0)
Cho 3,06 g Bari oxit tác dụng với nước, thu được 20 ml dd bazơ.
a) Tính nồng độ mol của dd bazơ thu được.
b) Tính khối lượng dd H2SO4 20% cần dùng để trung hòa hết lượng bazơ nói trên. Từ đó tính thể tích dd H2SO4 đem dùng, biết D (dd H2SO4) = 1,14g/ml.
BaO+H2O -> Ba(OH)2
0,02 0,02
a) CM = n/V = 0,02/0,02 = 1M
b) Ba(OH)2 + H2SO4 -> BaSO4 +2H2O
0,02 0,02
=> m = 0,392 g
D = m/V = 1,14
=> 0,392/V = 1,14 => V = 0,34l
Đúng 2
Bình luận (2)
Tính thể tích dd H2SO4 98% (d = 1,83g/ml) cần dùng để pha đc 500ml dd H2SO4 0,1M. Nêu cáh pha chế dd trên.
Tính thể tích dd H2SO4 98% (d = 1,83g/ml) cần dùng để pha đc 500ml dd H2SO4 0,1M. Nêu cáh pha chế dd trên.


















