X và Y : 2 ng.tố thuộc cùng 1 nhóm ở 2 CK liên tiếp , pk rằng X đứng tr Y tr BTH . Tổng các hat mang điện trong ng.tử X và Y là 52. Số hiệu nguyên tử của X và Y:

Những câu hỏi liên quan
X và Y là hai nguyên tố thuộc cùng một nhóm ở hai chu kì liên tiếp, biết rằng X đứng trước Y trong bảng tuần hoàn. Tổng các hạt mang điện trong nguyên tử X và Y là 52. Số hiệu nguyên tử của X là
A. 22
B. 17
C. 9
D. 5
X và Y là 2 nguyên tố cùng 1 nhóm A và ở 2 chu kì liên tiếp trong bảng tuần hoàn. Tổng số hạt mang điện trong hạt nhân của 2 nguyên tử X và Y bằng 32. Số hiệu của chúng lần lượt là
X và Y là hai nguyên tố thuộc cùng nhóm A, ở hai chu kì liên tiếp,
Z
X
Z
Y
và Y là nguyên tố thuộc chu kì lớn của bảng tuần hoàn. Biết rằng tổng số hạt proton, nơtron, electron trong X và Y là 156, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 36. X là A. As B. P C. O D. Ca
Đọc tiếp
X và Y là hai nguyên tố thuộc cùng nhóm A, ở hai chu kì liên tiếp, Z X < Z Y và Y là nguyên tố thuộc chu kì lớn của bảng tuần hoàn. Biết rằng tổng số hạt proton, nơtron, electron trong X và Y là 156, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 36. X là
A. As
B. P
C. O
D. Ca
B
X và Y là hai kim loại cùng nhóm A.
=> Y có nhiều hơn X là 8 hoặc 18 hoặc 32 electron.
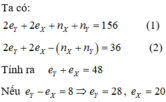
(không thuộc 2 chu kì)(loại).
![]()
Vậy 2 nguyên tố này là As và P, cùng thuộc nhóm VA và thuộc 2 chu kì (nhận).
![]()
(không thuộc 2 chu kì liên tiếp) (loại).
Vậy X là photpho (P).
Đúng 0
Bình luận (0)
X và Y là 2 nguyên cùng 1 nhóm A thuộc 2 chu kì liên tiếp. Xác định vị trí X và Y biết tổng số hạt mang điện X và Y là 116
Vì X và Y thuộc cùng một nhóm A và ở chu kì liên tiếp nên ta có:
\(\left[{}\begin{matrix}\left\{{}\begin{matrix}2Z_X+2Z_Y=116\\Z_Y-Z_X=8\end{matrix}\right.\\\left\{{}\begin{matrix}2Z_X+2Z_Y=116\\Z_Y-Z_X=18\end{matrix}\right.\end{matrix}\right.\Rightarrow\left[{}\begin{matrix}\left\{{}\begin{matrix}Z_X=25\\Z_Y=33\end{matrix}\right.\\\left\{{}\begin{matrix}Z_X=20\\Z_y=38\end{matrix}\right.\end{matrix}\right.\)
TH1 : ZX= 25 (Mn) , ZY=33 (As ) loại do không cùng nhóm và không thuộc 2 chu kì liên tiếp
TH2 : ZX=20 (Ca) ; ZY=38 (Sr) chọn vì thỏa mãn yêu cầu đề bài : Thuộc nhóm IIA và ở 2 chu kì liên tiếp là 3 và 4
Đúng 1
Bình luận (0)
Câu 5: X và Y thuộc cùng chu kì ở hai nhóm A liên tiếp nhau trong bảng HTTH, tổng số e của X và Y là 51. Xác định X,Y.Câu 8: Hai nguyên tố A và B ở hai nhóm A liên tiếp trong BTH. B thuộc nhóm VA. Ở trạng thái đơn chất A và B không phản ứng với nhau. Tổng số proton trong hạt nhân của A và B là 23. Xác định A, B. Viết cấu hình e và xác định tính chất hóa học cơ bản của chúng.Ai giúp mình 2 câu này với :
Đọc tiếp
Câu 5: X và Y thuộc cùng chu kì ở hai nhóm A liên tiếp nhau trong bảng HTTH, tổng số e của X và Y là 51. Xác định X,Y.
Câu 8: Hai nguyên tố A và B ở hai nhóm A liên tiếp trong BTH. B thuộc nhóm VA. Ở trạng thái đơn chất A và B không phản ứng với nhau. Tổng số proton trong hạt nhân của A và B là 23. Xác định A, B. Viết cấu hình e và xác định tính chất hóa học cơ bản của chúng.
Ai giúp mình 2 câu này với :<
Câu 52: X và Y là hai kim loại thuộc cùng một nhóm A. Biết ZX ZY và ZX + ZY 32. Có các phát biểu sau:(1) Số hạt mang điện trong hạt nhân Y nhiều hơn số hạt mang điện trong hạt nhân X là 8.(2) Bán kính nguyên tử của X lớn hơn Y. (3) Tính kim loại của X mạnh hơn của Y.(4) X có độ âm điện lớn hơn Y. (5) X và Y đều có 2 electron ở lớp ngoài cùng.(6) Các ion tạo ra từ X và Y đều có 8 electron ở lớp ngoài cùng. Các phát biểu đúng làA. (1), (2), (5),...
Đọc tiếp
Câu 52: X và Y là hai kim loại thuộc cùng một nhóm A. Biết ZX < ZY và ZX + ZY = 32. Có các phát biểu sau:
(1) Số hạt mang điện trong hạt nhân Y nhiều hơn số hạt mang điện trong hạt nhân X là 8.
(2) Bán kính nguyên tử của X lớn hơn Y.
(3) Tính kim loại của X mạnh hơn của Y.
(4) X có độ âm điện lớn hơn Y.
(5) X và Y đều có 2 electron ở lớp ngoài cùng.
(6) Các ion tạo ra từ X và Y đều có 8 electron ở lớp ngoài cùng. Các phát biểu đúng là
A. (1), (2), (5), (6). B. (2), (3), (4), (5).
C. (1), (2), (3), (5). D. (1), (4), (5), (6).
X là nguyên tố Magie (Z = 12)
Y là nguyên tố Canxi (Z = 20)
Vậy Chọn đáp án D
(2) Sai vì X có bán kính nguyên tử nhỏ hơn Y
(3) Sai vì Y có tính kim loại mạnh hơn
Đúng 1
Bình luận (0)
Câu 6: X và Y là 2 nguyên tố ở cùng 1 nhóm A và thuộc 2 chu kì liên tiếp trong bảng hệ thống tuần hoàn. Tổng số proton trong 2 hạt nhân nguyên tử X và Y bằng 30. Hãy viết cấu hình electron của X, Y và của các ion mà X và Y có thể tạo thành.
Đọc tiếp
Câu 6: X và Y là 2 nguyên tố ở cùng 1 nhóm A và thuộc 2 chu kì liên tiếp trong bảng hệ thống
tuần hoàn. Tổng số proton trong 2 hạt nhân nguyên tử X và Y bằng 30. Hãy viết cấu hình
electron của X, Y và của các ion mà X và Y có thể tạo thành.
X và Y là 2 nguyên tố thuộc hai chu kỳ liên tiếp nhau trong cùng một nhóm A của bảng tuần hoàn, X có điện tích hạt nhân nhỏ hơn Y. Tổng số proton trong hạt nhân nguyên tử của X và Y là 32. X, Y là A. Na(Z11) và K(Z19). B. Si(Z14) và Ar(Z18). C. Al(Z13) và K(Z19). D. Mg(Z12) và Ca(Z20).
Đọc tiếp
X và Y là 2 nguyên tố thuộc hai chu kỳ liên tiếp nhau trong cùng một nhóm A của bảng tuần hoàn, X có điện tích hạt nhân nhỏ hơn Y. Tổng số proton trong hạt nhân nguyên tử của X và Y là 32. X, Y là
A. Na(Z=11) và K(Z=19).
B. Si(Z=14) và Ar(Z=18).
C. Al(Z=13) và K(Z=19).
D. Mg(Z=12) và Ca(Z=20).
Đáp án D
Hai nguyên tố thuộc cùng một nhóm A, thuộc hai chu kỳ liên tiếp = Điện tích hạt nhân cách nhau 8, 18 hay 32
Trường hợp 1:
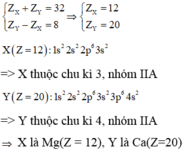
Trường hợp 2:
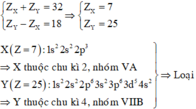
Trường hợp 3:
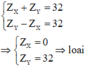
Đúng 0
Bình luận (0)
Bài 5: Tìm số hiệu nguyên tử các nguyên tố
Hai nguyên tố X và Y thuộc 2 nhóm A liên tiếp trong cùng một chu kì của bảng hệ thống tuần hoàn và có tổng số điện tích hạt nhân bằng 33.
Giả sử pX < pY
Do X, Y thuộc 2 nhóm A liên tiếp trong cùng 1 chu kì
=> pY - pX = 1
Có pX + pY = 33
=> pX = 16, pY = 17
=> Số hiệu nguyên tử của X là 16, của Y là 17
Đúng 1
Bình luận (0)














