1 13, 6 g hỗn hợp Fe fe2O3 tác dụng hết với dung dịch HCl thu được 2, 24 lít H2 ở điều kiện tiêu chuẩn dung dịch thu được cho tác dụng với NaOH dư tạo kết tủa rồi nung trong không khí đến khối lượng không đổi được a gam chất rắn tính a

Những câu hỏi liên quan
Hỗn hợp x gồm fe FeO Fe2O3 có tỉ lệ khối lượng tương ứng là 35 72 160 cho m gam x tan hết vừa hết vào 500 ml dung dịch H2SO4 0,7 M thu được dung dịch y và v lít khí h2 ở điều kiện tiêu chuẩn cho Y tác dụng với dung dịch NaOH dư lọc kết tủa rồi nung ở nhiệt độ cao trong không khí đến khối lượng không đổi thu được 23,2 g chất rắn xác định V và khối lượng mỗi muối trong dung dịch Y
cho 18,8 g hỗn hợp Fe Fe2O3 tác dụng hết với dung dịch Hcl thu được 1,12l khí H2 dung dịch thu được cho tác dụng NaOH dư. kết tủa thu được đem nung trong không khi đến khối lượng không đổi thu được m g chất rắn.giá trị của m là
\(n_{Fe}=n_{H_2}=\frac{1,12}{22,4}\)=0,05 mol
\(m_{Fe_2O_3}\)=18,8-0,05.56=16g\(\rightarrow n_{Fe.trong.Fe_2O_3}=\frac{16}{160}.2\)=0,2 molchất rắn là \(Fe_2O_3\) nên bảo toàn nguyên tố \(Fe\) ta có:\(n_{Fe}=n_{Febanđầu}+n_{Fe.trong.Fe_2O_3}\)=0,05+0,2=0,25 mol\(\Rightarrow m_{Fe_2O_3}=\frac{0,25}{2}.160\)=20g
Đúng 0
Bình luận (0)
1.cho hỗn hợp gồm 1,8.1022nguyên tử Fe,24g Fe2O3 và 23,2g Fe3O4 tác dụng hết với dung dịch H2SO4 loãng thu được dung dịch A.Cho dung dịch A tác dụng với dung dịch NaOH dư,lọc kết tủa đem nung trong không khí đến khối lượng không đổi thu được m g chất rắn Ca)lập pthh b)tính m2.Cho 14,6g hỗn hợp 3 kim loại Cu Al Fe tác dụng với HCl dư thu được 7,48l H2(đktc),m g hỗn hợp muối và 6,4g chất rắn không tana)lập pthh b)tính m ,thành phần % về khối lượng của mỗi kim loại trong hỗn hợp kim loại trên
Đọc tiếp
1.cho hỗn hợp gồm 1,8.1022nguyên tử Fe,24g Fe2O3 và 23,2g Fe3O4 tác dụng hết với dung dịch H2SO4 loãng thu được dung dịch A.Cho dung dịch A tác dụng với dung dịch NaOH dư,lọc kết tủa đem nung trong không khí đến khối lượng không đổi thu được m g chất rắn C
a)lập pthh b)tính m
2.Cho 14,6g hỗn hợp 3 kim loại Cu Al Fe tác dụng với HCl dư thu được 7,48l H2(đktc),m g hỗn hợp muối và 6,4g chất rắn không tan
a)lập pthh b)tính m ,thành phần % về khối lượng của mỗi kim loại trong hỗn hợp kim loại trên
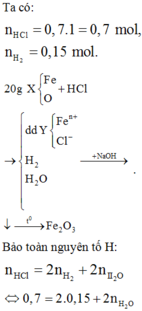
Cho 20 gam hỗn hợp X gồm Fe, FeO, Fe3O4, Fe2O3 tan vừa hết trong 700 ml dung dịch HCl 1M thu được 3,36 lít H2 (đktc) và dung dịch D. Cho dung dịch D tác dụng với dung dịch NaOH dư, lọc kết tủa và nung trong không khí đến khối lượng không đổi được chất rắn Y. Khối lượng của Y là: A. 16 gam. B. 32gam. C. 8gam. D. 24gam.
Đọc tiếp
Cho 20 gam hỗn hợp X gồm Fe, FeO, Fe3O4, Fe2O3 tan vừa hết trong 700 ml dung dịch HCl 1M thu được 3,36 lít H2 (đktc) và dung dịch D. Cho dung dịch D tác dụng với dung dịch NaOH dư, lọc kết tủa và nung trong không khí đến khối lượng không đổi được chất rắn Y. Khối lượng của Y là:
A. 16 gam.
B. 32gam.
C. 8gam.
D. 24gam.
Cho 8,3g hỗn hợp kim loại Fe và Al tác dụng với dung dịch HCL dư thu được dung dịch X và 5,6 lít H2(đktc) Cho dung dịch X tác dụng với lượng dư NaOH thu được m gam kết tủa.Nung kết tủa trong không khí đến khối lượng không đổi thu được a gam chất rắn.Viết PTPƯ và tính m,a
Các PTHH :
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
\(FeCl_2+2NaOH\rightarrow Fe\left(OH\right)_2\downarrow+2NaCl\)
\(AlCl_3+3NaOH\rightarrow Al\left(OH\right)_3\downarrow+3NaCl\)
\(4Fe\left(OH\right)_2+O_2\xrightarrow[]{t^o}2Fe_2O_3+4H_2O\)
\(2Al\left(OH\right)_3\xrightarrow[]{t^o}Al_2O_3+3H_2O\)
Kết tủa thu được gồm Fe(OH)2 và Al(OH)3
Đặt : \(n_{Fe}=a\left(mol\right),n_{Al}=b\left(mol\right)\)
\(\Rightarrow56a+27b=8,3g\left(1\right)\)
\(Bte:2n_{Fe}+3n_{Al}=2n_{H2}=2a+3b=2.\dfrac{5,6}{22,4}=\left(2\right)\)
Từ(1),(2) \(\Rightarrow\left\{{}\begin{matrix}a=0,1=n_{Fe\left(OH\right)2}\\b=0,1=n_{Al\left(OH\right)3}\end{matrix}\right.\)
\(\Rightarrow m_{kết.tủa}=m_{Fe\left(OH\right)2}+m_{Al\left(OH\right)3}=0,1.90+0,1.78=16,8\left(g\right)\)
\(Bt\left(Al\right):n_{Al}=n_{Al2O3}=0,1\left(mol\right)\)
\(Bt\left(Fe\right):n_{Fe}=n_{Fe2O3}=0,1\left(mol\right)\)
\(\Rightarrow m_{Chất.rắn}=0,1.160+0,1.102=26,2\left(g\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (1)
Đầu tiên, chúng ta sẽ viết các phương trình phản ứng cho mỗi bước của quá trình.
Bước 1: Phản ứng giữa hỗn hợp Fe và Al với dung dịch HCl: HCl (dung dịch) + Fe (kim loại) → FeCl2 (dung dịch) + H2 (khí)
2HCl + Fe → FeCl2 + H2
Bước 2: Phản ứng giữi dung dịch X với NaOH tạo kết tủa: X (dung dịch) + 2NaOH → 2NaX (dung dịch) + H2O (lỏng) + Al(OH)3 (kết tủa)
Bước 3: Nung kết tủa Al(OH)3 trong không khí: 2Al(OH)3 → Al2O3 + 3H2O
Bây giờ, chúng ta sẽ tính toán m và a.
Bước 1: Tính lượng H2 thoát ra.
Trước hết, chúng ta cần biết lượng mol của Fe trong hỗn hợp. Công thức của FeCl2 là Fe2+ (một cation sẽ tạo ra 1 mol H2 khi phản ứng với HCl). Vì vậy, số mol của Fe là bằng số mol H2.
Khối lượng mol của H2 là 2 g/mol, vì vậy số mol H2:
n(H2) = 5.6 l / 22.4 l/mol (ở điều kiện tiêu chuẩn) = 0.25 mol
Do đó, số mol Fe = 0.25 mol.
Khối lượng mol của Fe là 55.85 g/mol, vậy khối lượng của Fe là:
m(Fe) = 0.25 mol × 55.85 g/mol = 13.96 g
Bước 2: Tính lượng kết tủa Al(OH)3.
Al(OH)3 có khối lượng mol là 78 g/mol, và theo phương trình phản ứng ta thấy rằng mỗi mol Al(OH)3 tạo ra một mol kết tủa. Vì vậy, số mol Al(OH)3 tạo ra là bằng số mol NaOH đã sử dụng.
Số mol NaOH đã sử dụng được tính theo số mol H2O được tạo ra khi NaOH phản ứng. Một mol NaOH phản ứng với một mol H2O.
n(Al(OH)3) = n(NaOH) = n(H2O) = 0.25 mol
Khối lượng của Al(OH)3:
m(Al(OH)3) = 0.25 mol × 78 g/mol = 19.5 g
Bước 3: Nung kết tủa Al2O3 trong không khí.
Khối lượng của Al2O3 không thay đổi sau quá trình nung. Vì vậy, a = 19.5 g (cùng với m(Al(OH)3)).
Tóm lại:
m = 19.5 g (kết tủa Al(OH)3)a = 19.5 g (sau khi nung thành Al2O3)
Đúng 0
Bình luận (0)
13, 6 gam hỗn hợp Fe Fe2 O3 tác dụng hết với dung dịch HCl thu được 2, 24 lít H2 ở điều kiện tiêu chuẩn. dung dịch thu được cho tác dụng với NaOH dư tạo kết tủa rồi nung nóng trong không khí đến khối lượng không đổi được a gam chất rắn a có giá trị là bao nhiêu
Đun nóng hỗn hợp X gồm bột Fe và S trong điều kiện không có không khí, thu được hỗn hợp rắn A. Cho A tác dụng với một lượng dư dung dịch HCl thu được sản phẩm khí Y cñ tỉ khối so với H2 là 13. Lấy 2,24 lít (đo ở điều kiện tiêu chuẩn) khí Y đem đốt cháy rồi cho toàn bộ sản phẩm cháy đñ đi qua 100 ml dung dịch H2O2 5,1% (có khối lượng riêng bằng 1g/ml), sau phản ứng thu được dung dịch B. Các phản ứng xảy ra hoàn toàn.a. Tính thành phần % khối lượng các chất trong hỗn hợp X. (%Fe 70%; %S 30%)b. X...
Đọc tiếp
Đun nóng hỗn hợp X gồm bột Fe và S trong điều kiện không có không khí, thu được hỗn hợp rắn A. Cho A tác dụng với một lượng dư dung dịch HCl thu được sản phẩm khí Y cñ tỉ khối so với H2 là 13. Lấy 2,24 lít (đo ở điều kiện tiêu chuẩn) khí Y đem đốt cháy rồi cho toàn bộ sản phẩm cháy đñ đi qua 100 ml dung dịch H2O2 5,1% (có khối lượng riêng bằng 1g/ml), sau phản ứng thu được dung dịch B. Các phản ứng xảy ra hoàn toàn.
a. Tính thành phần % khối lượng các chất trong hỗn hợp X. (%Fe = 70%; %S = 30%)
b. Xác định nồng độ % các chất trong dung dịch B. (C%H2SO4 = 6,695%; C%H2O2 = 2,392%)Đun nóng hỗn hợp X gồm bột Fe và S trong điều kiện không có không khí, thu được hỗn hợp rắn A. Cho A tác dụng với một lượng dư dung dịch HCl thu được sản phẩm khí Y cñ tỉ khối so với H2 là 13. Lấy 2,24 lít (đo ở điều kiện tiêu chuẩn) khí Y đem đốt cháy rồi cho toàn bộ sản phẩm cháy đñ đi qua 100 ml dung dịch H2O2 5,1% (có khối lượng riêng bằng 1g/ml), sau phản ứng thu được dung dịch B. Các phản ứng xảy ra hoàn toàn.
a. Tính thành phần % khối lượng các chất trong hỗn hợp X. (%Fe = 70%; %S = 30%)
b. Xác định nồng độ % các chất trong dung dịch B. (C%H2SO4 = 6,695%; C%H2O2 = 2,392%)
a) PTHH : Fe + S \(\rightarrow\) FeS
=> A gồm : Fe , FeS
Fe + 2 HCl -> FeCl2 + H2
FeS + 2 HCL -> FeCl2 + H2S
=> Y gồm : H2 , H2S
nY = n H2 + n H2S = 0,1 mol (I)
dY/H2 = 13 -> m Y = 2.nH2 + 34.n H2S = 13.2.0,1 = 2,6 g (II)
Từ (I),(II) => n H2 = 0,025 mol ; n H2S = 0,075 mol
Fe + 2 HCl \(\rightarrow\) FeCl2 + H2
0,025<---------------------0,025 mol
FeS + 2 HCl \(\rightarrow\) FeCl2 + H2S
0,075<-------------------------0,075 mol
Ta có: n S = n Fe phản ứng = n FeS = 0,075 mol
=>m S =0,075.32 = 2,4 g
n Fe ban đầu = 0,075 + 0,025 = 0,1mol
=>m Fe=0,1.56 = 5,6 g
=> %m S = \(\dfrac{2,4}{2,4+5,6}.100=30\%\)
=> %m Fe = 100 - 70 = 30%
b ) 2 H2 + O2 \(\rightarrow\) 2 H2O
0,025-------------->0,025 mol
2 H2S + 3 O2 \(\rightarrow\) 2 SO2 + 2 H2O
0,075--------------->0,075--->0,075 mol
m H2O2 = 5,1 g -> n H2O2 = 0,15 mol
PTHH : SO2 + H2O2 \(\rightarrow\) H2SO4
Ban đầu :0,075---->0,15 mol
Phản ứng:0,075--->0,075------>0,075 mol
Sau phản ứng:0----->0,075----->0,075 mol
m dd sau phản ứng = 18.(0,025 + 0,075 ) + 64.0,075 + 100 = 106,6 g
m H2O2 dư = 0,075.34 =2,55g
\(\Rightarrow C\%_{H_2O_2dư}=\dfrac{2,55}{106,6}.100=2,392\%\)
m H2SO4 = 0,075.98 = 7,35g
\(\Rightarrow C\%_{H_2SO_4}=\dfrac{7,35}{106,6}.100=6,895\%\)
Đúng 1
Bình luận (1)
hòa tan 15,25 g hỗn hợp gồm Fe và 1 kim loại hóa trị 2 bằng dung dich HCl dư sau phản ứng kết thúc thu được 4,48 lít khí H2 ở điều kiện tiêu chuẩn và dung dịch X cho dung dịch X tác dụng với NaOH dư thu được kết tủa lọc lấy kết tủa đem nung ở nhiệt độ cao thu được 12g một oxit xác định kim loại hóa trị 2 biết rằng kim loại này ko tạo kết tủa với hidro oxitgiúp mk vs mai mk thi hóa r !
Đọc tiếp
hòa tan 15,25 g hỗn hợp gồm Fe và 1 kim loại hóa trị 2 bằng dung dich HCl dư sau phản ứng kết thúc thu được 4,48 lít khí H2 ở điều kiện tiêu chuẩn và dung dịch X cho dung dịch X tác dụng với NaOH dư thu được kết tủa lọc lấy kết tủa đem nung ở nhiệt độ cao thu được 12g một oxit xác định kim loại hóa trị 2 biết rằng kim loại này ko tạo kết tủa với hidro oxit
giúp mk vs mai mk thi hóa r !
ong mk k cho ! ng VN nói là lm ! " 3 cái "
Hòa tan hoàn toàn 26 gam hỗn hợp rắn gồm Fe2O3, Fe3O4, FeO, Fe trong 910 ml dung dịch HCl 1M (vừa đủ) thu được dung dịch X và giải phóng 4,368 lít H2 (đkc). Cho X tác dụng với dung dịch NaOH dư, lọc kết tủa và nung trong không khí đến khối lượng không đổi thu được m gam chất rắn. Giá trị m là: A. 37,44 gam B. 31,20 gam C. 28,08 gam D. 24,96 gam
Đọc tiếp
Hòa tan hoàn toàn 26 gam hỗn hợp rắn gồm Fe2O3, Fe3O4, FeO, Fe trong 910 ml dung dịch HCl 1M (vừa đủ) thu được dung dịch X và giải phóng 4,368 lít H2 (đkc). Cho X tác dụng với dung dịch NaOH dư, lọc kết tủa và nung trong không khí đến khối lượng không đổi thu được m gam chất rắn. Giá trị m là:
A. 37,44 gam
B. 31,20 gam
C. 28,08 gam
D. 24,96 gam
Qui hỗn hợp về dạng : x mol Fe ; y mol FeO ; z mol Fe2O3
=> mhh = 56x + 72y + 160z = 26 (1)
Có nHCl = 2x + 2y + 6z = 0,91 mol (2)
Và nH2 = nFe = x = 0,195 mol (3)
Từ (1) ; (2) ; (3) => y = z = 0,065 mol
=> Khi nung kết tủa thì sản phẩm chỉ còn Fe2O3
Bảo toàn Fe : nFe2O3 = ½ nFe(hh đầu) = ½ . ( x + y + 2z) = 0,195 mol
=>m = 31,2g
=>B
Đúng 0
Bình luận (0)