Hòa tan m gam hỗn hợp X gồm Fe và kim loại M (có hóa trị không đổi) trong dung dịch HCL dư thì thu được 1.008 lít (đktc) và dung dịch chứa 4.575 gam muối.Tính m.
Hòa tan 12 gam hỗn hợp gồm Fe và một kim loại M hóa trị II vào dung dịch H2SO4 dư thu được 4,48 lít H2 (đktc). Nếu hòa tan 23,8 gam kim loại M vào dung dịch chứa 0,7 mol HCl thì M không tan hết. Tìm M
\(n_{Fe} = a(mol) ; n_M = b(mol)\\ \Rightarrow 56a + Mb = 12\)
\(Fe + 2HCl \to FeCl_2 + H_2\\ M + 2HCl \to MCl_2 + H_2\\ n_{H_2} = a + b = \dfrac{4,48}{22,4} = 0,2(mol)\\ \Rightarrow a = 0,2 - b ( 0< b < 0,2)\)
Suy ra:
56(0,2 - b) + Mb = 12
\(\Rightarrow M = \dfrac{0,8 + 56b}{b}\)
Vì 0 < b < 0,12
Nên M > 62,67(1)
Mặt khác,
\(n_M > \dfrac{1}{2}n_{HCl} = 0,35\\ \Rightarrow M < \dfrac{23,8}{0,35} = 68(2)\)
Từ (1)(2) suy ra: 62,67 < M < 68
Do đó, M = 65(Zn) thì thỏa mãn
Vậy M là Zn(Kẽm)
Hòa tan hoàn toàn m gam hỗn hợp A gồm Fe và kim loại M ( hóa trị không đổi) trong dung dịch HCl dư, thu được 1,008 lít khí (đktc) và dung dịch chứa 4,575 gam muối.
1. Tính khối lượng m.
2. Hòa tan hết m gam hỗn hợp A trong dung dịch chứa đồng thời hai axit: HNO3 ( đặc) và H2SO4 ( khi đun nóng) thu được 1,8816 lít hỗn hợp B gồm 2 khí (đktc). Tỉ khối của hỗn hợp B so với H2 bằng 25,25. Xác định kim loại M biết rằng trong dung dịch tạo thành không chứa muối amoni.
Câu 1

Áp dụng định luật bảo toàn nguyên
tố H ta có:
nHCl = 2nH2 = 2.0,045 = 0,09 mol
Áp dụng định luật bảo toàn khối lượng
ta có: mA + mHCl = m muối + mH2
=> m = m muối + mH2 – mA = 4,575 + 0,045.2 – 0,09.36,5 = 1,38 (gam)
Câu 2

Do cho kim loại phản ứng với H2SO4 đặc và HNO3 đặc nên khí sinh ra là SO2 và NO2.
Áp dụng phương pháp đường chéo ta có:
SO2: 64 4,5
50,5
NO2: 46 13,5
→nSO2=nNO2=4,513,5=13

Đặt số mol của Fe và M lần lượt là x và y (mol)
- Khi cho hỗn hợp tác dụng với HCl:
Fe + 2HCl → FeCl2 + H2
x x (mol)
M + nHCl → MCln + 0,5nH2
y 0,5ny (mol)
nH2 = 0,045 => x + 0,5ny = 0,045 (1)
- Khi cho hỗn hợp tác dụng với HNO3 đặc và H2SO4 đặc:
Ta có các bán phản ứng oxi hóa – khử:
Fe → Fe3+ + 3e
x 3x
M → Mn+ + ne
y ny
S+6 + 2e → S+4 (SO2)
0,021 0,042
N+5 + 1e → N+4 (NO2)
0,063 0,063
Áp dụng định luật bảo toàn electron ta có: 3x + ny = 0,042 + 0,063 hay 3x + ny = 0,105 (2)
Từ (1) và (2) ta có hệ phương trình sau:

Mặt khác: mA = mFe + mM => 1,38 = 0,015.56 + My => My = 0,54(4)
Từ (3) và (4) suy ra M = 9n
Ta có bảng sau:
| n |
1 |
2 |
3 |
| M |
9 (loại) |
18 (loại) |
27 (nhận) |
Vậy kim loại M là nhôm, kí hiệu là Al.
Hòa tan hoàn toàn m gam hỗn hợp E gồm Sn và một kim loại R (có hóa trị không đổi) trong lượng dư dung dịch HCl, thu được 5,04 lít khí H2 (đktc) và dung dịch chứa 36,27 gam muối. Mặt khác, để đốt cháy cũng m gam hỗn hợp E cần vừa đủ 3,696 lít O2 (đktc). Kim loại R là
A. Al
B. Zn
C. Ca
C. Ca
Gọi hóa trị của R là n và số mol Sn và R lần lượt là a và b mol
+/ Khi phản ứng với HCl :
Sn + HCl → SnCl2 + H2
R + nHCl → RCln + 0,5nH2
+/ Khi đốt trong oxi :
Sn + O2 → SnO2
2R + 0,5nO2 → R2On
=> Ta có : nH2 = a + 0,5nb = 0,225 mol
Và nO2 = a + 0,25nb = 0,165 mol
=> a = 0,105 mol ; nb = 0,24 mol
Có mmuối = 0,105.190 + 0,24/n . (R + 35,5n) = 36,27
=>R = 32,5n
=>Cặp n =2 ; R =65 (Zn) thỏa mãn
=>B
Hòa tan hỗn hợp A gồm Fe, FeO, Fe2O3, Fe3O4, Fe(OH)2, Fe(OH)3, FeCO3 trong dung dịch HCl dư thu được 2,688 lít (đktc) hỗn hợp khí có tỉ khối so với He bằng 5,75 và dung dịch chứa m gam muối. Mặt khác hòa tan hoàn toàn lượng hỗn hợp rắn A như trên trong dung dịch HNO3 dư thu được dung dịch X chứa 96,8 gam một muối và 4,48 lít (đktc) gồm 2 khí, trong đó có một khí hóa nâu trong không khí. Giá trị của m là
A. 29,660
B. 59,320
C. 27,175
D. 54,350
Đáp án : D
+) A + HCl : 2 khí là H2 và CO2 => nH2 = nCO2 = 0,06 mol
=> nFe = nFeCO3 = 0,06 mol
+) A + HNO3 -> 1 muối là Fe(NO3)3 có n = 0,4 mol
Hỗn hợp khí gồm CO2 và khí hóa nâu ngoài không khí là NO
=> nCO2 + nNO = 0,2 mol => nNO = 0,14 mol
Bảo toàn e : 3nFe + nFe2+(oxit,hidroxit) + nFeCO3 = 3nNO
=> nFe2+(oxit,hidroxit) = 0,18 mol
Bảo toàn Fe : nFe2+(oxit,hidroxit) + nFe3+(oxit,hidroxit) + nFe + nFeCO3 = 0,4 mol
=> nFe3+(oxit,hidroxit) = 0,1 mol
+) A + HCl -> muối gồm FeCl2 và FeCl3
=> nFeCl3 = nFe3+(oxit,hidroxit) = 0,1 mol
Và nFeCl2 = nFe2+(oxit,hidroxit) + nFe + nFeCO3 = 0,3 mol
=> m = 54,35g
Hòa tan hoàn toàn 9,6 gam hỗn hợp A gồm Fe và một kim loại M (có hóa trị không đổi trong mọi hợp chất) bằng dung dịch HCl 14,6% vừa đủ thu được 4,48 lít khí H2 (đktc) và dung dịch X. Tỉ lệ số mol của M và Fe trong hỗn hợp A là 1: 3. Mặt khác cho 9,6 gam hỗn hợp A tác dụng hết với khí Cl2 thì cần dùng 6,16 lít khí Cl2 (đktc). Xác định kim loại M.
Hòa tan hoàn toàn 24 gam hỗn hợp X gồm MO, M(OH)2 và MCO3 (M là kim loại có hóa trị không đổi) trong 100 gam dung dịch H2SO4 39,2%, thu được 1,12 lít khí(đktc) và dung dịch Y chỉ chứa một chất tan duy nhất có nồng độ 39,41%. Kim loại M là:
A. Zn
B. Ca
C. Mg
D. Cu
Hòa tan hoàn toàn 24 gam hỗn hợp X gồm MO, M ( O H ) 2 và M C O 3 (M là kim loại có hóa trị không đổi) trong 100 gam dung dịch H 2 S O 4 39,2% thu được 1,12 lít khí (đktc) và dung dịch Y chỉ chứa một chất tan duy nhất có nồng độ 39,41%. M là kim loại
A. Mg
B. Ca
C. Zn
D. Ba
Hòa tan hoàn toàn 24 gam hỗn hợp X gồm MO, M(OH)2 và MCO3 (M là kim loại có hóa trị không đổi) trong 100 gam dung dịch H2SO4 39,2% thu được 1,12 lít khí (đktc) và dung dịch Y chỉ chứa một chất tan duy nhất có nồng độ 39,41%. Kim loại M là
A. Cu
B. Mg
C. Ca
D. Zn
Đáp án B
n H 2 SO 4 = 100 . 0 , 392 98 = 0 , 4 mol
Sau phản ứng thu được dung dịch Y chỉ chứa một chất tan Þ phản ứng vừa đủ, H2SO4 phản ứng hết
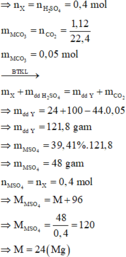
Hòa tan hoàn toàn 24 gam hỗn hợp X gồm MO, M ( O H ) 2 và M C O 3 (M là kim loại có hóa trị không đổi) trong 100 gam dung dịch H 2 S O 4 39,2%, thu được 1,12 lít khí (đktc) và dung dịch Y chỉ chứa một chất tan duy nhất có nồng độ 39,41%. Kim loại M là
A. Zn
B. Ca
C. Mg
D. Cu