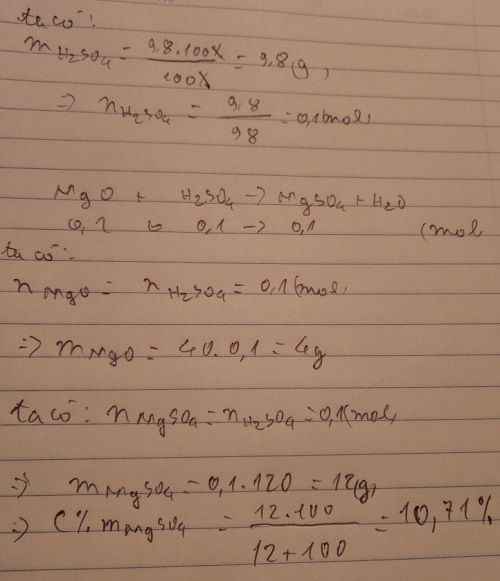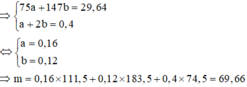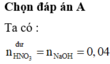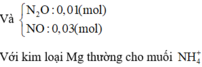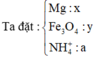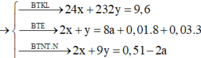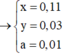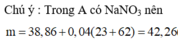Để trung hòa vừa đủ 200ml dung dịch hỗn hợp HCl xM cần 300ml dung dịch NaOH 2M, thu được dung dịch X.Cô cạn dung dịch X thu được (m) gam muối khan .Xác định X và M

Những câu hỏi liên quan
Để trung hòa vừa đủ 200ml dung dịch hỗn hợp HCl xM cần 300ml dung dịch NaOH 2M, thu được dung dịch X.Cô cạn dung dịch X thu được (m) gam muối khan .Xác định X và M
NaOH + HCl --> NaCl+H2O (1)
2NaOH +H2SO4 --> Na2SO4 +2H2O (2)
Đặt nNaOH (1)= a(mol)
nNaOH(2) = b (mol)
=>a + b = 0,3.2 =0,6( *)
Theo PT (1) : nNaCl = nNaOH(1) = a(mol)
Theo PT (2) : nNa2SO4=12
nNaOH(2) = 0,5b(mol)
=>58,5a + 71b =40,1(**)
Từ (*), (**) => a= 0,2 ; b = 0,4
nHCl = nNaOH (1)=0,2 mol
=> x=CMHCl=0,20,2=1M
nH2SO4 = nNaOH (2)=0,4 mol
y=CMH2SO4=0,40,2=2M
Để trung hòa vừa đủ 200ml dung dịch hỗn hợp HCl xM và H2SO4 yM cần 300ml dung dịch NaOH 2M,thu được dung dịch X.Cô cạn dung dịch X thu được 40,1g hỗn hợp muối khan.Xác định x,y
NaOH + HCl --> NaCl+H2O (1)
2NaOH +H2SO4 --> Na2SO4 +2H2O (2)
Đặt nNaOH (1)= a(mol)
nNaOH(2) = b (mol)
=>a + b = 0,3.2 =0,6( *)
Theo PT (1) : nNaCl = nNaOH(1) = a(mol)
Theo PT (2) : nNa2SO4=\(\dfrac{1}{2}\) nNaOH(2) = 0,5b(mol)
=>58,5a + 71b =40,1(**)
Từ (*), (**) => a= 0,2 ; b = 0,4
nHCl = nNaOH (1)=0,2 mol
=> \(x=CM_{HCl}=\dfrac{0,2}{0,2}=1M\)
nH2SO4 = nNaOH (2)=0,4 mol
\(y=CM_{H_2SO_4}=\dfrac{0,4}{0,2}=2M\)
Đúng 1
Bình luận (1)
1. Để trung hòa vừa đủ 200ml dung dịch hỗn hợp gồm HCl xM, H2SO4 yM cần 300ml dung dịch NaOh 2M thu được dung dịch X .
Cô cạn X thu được 40,1g hỗn hợp muối khan. Xác định x, y
2. Cho 25,8g một ôlêum X hòa tan trong 174,2 g H2O -> dung dịch H2SO4. Xác định CTHH của ôlêum X và tính % khối lượng SO3 trong X . CT ôlêum: H2SO4. nSO3
1.
NaOH + HCl --> NaCl+H2O (1)
2NaOH +H2SO4 --> Na2SO4 +2H2O (2)
giả sử nNaOH (1)=x(mol)
nNaOH(2)=y(mol)
=>x+y=0,3.2=0,6(I)
theo (1) : nNaCl=nNaOH(1)=x(mol)
theo (2) : nNa2SO4=1/2nNaOH(2)=0,5y(mol)
=>58,5x+71y=40,1(II)
từ (I,II)
=>\(\left\{{}\begin{matrix}x=0,2\left(mol\right)\\y=0,4\left(mol\right)\end{matrix}\right.\)
theo (1) : nHCl=nNaOH(1)=0,2(mol)
=>x=CM dd HCl=1(M)
theo (2) : nH2SO4=1/2nNaOH(2)=0,2(mol)
=>y=1(M)
Đúng 0
Bình luận (0)
để trung hòa 50ml dung dịch hỗn hợp axit gồm H2SO4 và HCl cần dg 200ml dung dịch NaOH 1M
. Mặt khác lấy 100ml dung dịch hỗn hợp axit trên đem trung hòa với 1 lượng dung dịch NaOH vừa đủ rồi cô cạn thì thu được 24,65g muối khan. Tinh nồng độ mol/L của mỗi axit trong dung dịch ban đầu
E là este thuần chức, mạch không phân nhánh. Đun nóng m gam E với 150 ml dung dịch NaOH 2M đến hoàn toàn thu được dung dịch X. Trung hòa X cần 200 ml dung dịch HCl 0,3M thu được dung dịch Y. Cô cạn Y thu được 22,95 gam hỗn hợp 2 muối khan và 11,04 gam hỗn hợp 2 ancol đơn chức. E là: A.
CH
3
-
CH
2
-
OOC
-
CH
2
COO...
Đọc tiếp
E là este thuần chức, mạch không phân nhánh. Đun nóng m gam E với 150 ml dung dịch NaOH 2M đến hoàn toàn thu được dung dịch X. Trung hòa X cần 200 ml dung dịch HCl 0,3M thu được dung dịch Y. Cô cạn Y thu được 22,95 gam hỗn hợp 2 muối khan và 11,04 gam hỗn hợp 2 ancol đơn chức. E là:
A. CH 3 - CH 2 - OOC - CH 2 COOCH 3
B. HCOOCH3 và CH3COOC2H5
C. C2H5-COO-C2H5
D. CH3CH2CH2-OOC-CH2CH2COOCH3
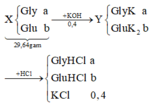
Để trung hòa hết 29,64 gam hỗn hợp X glyxin và axit glutamic cần vừa đủ 400ml dung dịch KOH 1M, thu được dung dịch Y. Cho dung dịch HCl dư vào Y thu được dung dịch chứa m gam muối khan. Giá trị của m là A. 62,98 B. 69,38 C. 69,66 D. 59,44
Đọc tiếp
Để trung hòa hết 29,64 gam hỗn hợp X glyxin và axit glutamic cần vừa đủ 400ml dung dịch KOH 1M, thu được dung dịch Y. Cho dung dịch HCl dư vào Y thu được dung dịch chứa m gam muối khan. Giá trị của m là
A. 62,98
B. 69,38
C. 69,66
D. 59,44
Bài 6: Hòa tan hoàn toàn m gam hỗn hợp X gồm 4 oxit bazơ cần dùng vừa đúng 1,6 lít dung dịch H2SO4 0,5M thu được dung dịch Y chứa 4 muối sunfat trung hòa. Cô cạn dung dịch Y được 107,4g muối khan. Xác định giá trị m?Bài 7: Để trung hòa V ml dung dịch X gồm HCl 1M và H2SO4 0,5M thì cần 200 ml dung dịch Ba(OH)2 1M thu được m gam kết tủa, dung dịch Y. a) Tính V, m. b) Tính khối lượng muối khan thu được khi cô cạn dung dịch Y.Bài 8: Cho 2,88 gam một kim loại X có hóa trị không đổi tác dụng với 300 m...
Đọc tiếp
Bài 6: Hòa tan hoàn toàn m gam hỗn hợp X gồm 4 oxit bazơ cần dùng vừa đúng 1,6 lít dung dịch H2SO4 0,5M thu được dung dịch Y chứa 4 muối sunfat trung hòa. Cô cạn dung dịch Y được 107,4g muối khan. Xác định giá trị m?
Bài 7: Để trung hòa V ml dung dịch X gồm HCl 1M và H2SO4 0,5M thì cần 200 ml dung dịch Ba(OH)2 1M thu được m gam kết tủa, dung dịch Y. a) Tính V, m. b) Tính khối lượng muối khan thu được khi cô cạn dung dịch Y.
Bài 8: Cho 2,88 gam một kim loại X có hóa trị không đổi tác dụng với 300 ml dung dịch HCl 1M thu được dung dịch A. Để trung hòa vừa đủ trong dung dịch A cần 60 ml dung dịch NaOH 1M. Xác định tên kim loại X.
Bài 6 :
Bảo toàn nguyên tố H :
$n_{H_2O} = n_{H_2SO_4} =1,6.0,5 = 0,8(mol)$
Bảo toàn khối lượng :
$m = 107,4 + 0,8.18 - 0,8.98 = 43,4(gam)$
Bài 7 :
$Ba(OH)_2 + 2HCl \to BaCl_2 + 2H_2O$
$Ba(OH)_2 + H_2SO_4 \to BaSO_4 + 2H_2O$
$n_{HCl} = 0,001V(mol) ; n_{H_2SO_4} = 5.10^{-4}V(mol)$
Theo PTHH :
$n_{Ba(OH)_2} = \dfrac{0,001}{2} + 5.10^{-4}V = 10^{-3}V = 0,2$
$\Rightarrow V = 200(ml)$
$n_{BaSO_4} = n_{H_2SO_4} = 0,1(mol)$
$m = 0,1.233 = 23,3(gam)$
b)
$n_{BaCl_2} = \dfrac{1}{2}n_{HCl} = 0,1(mol)$
$m_{BaCl_2} = 0,1.208 = 20,8(gam)$
Đúng 2
Bình luận (0)
Câu 8 :
$n_{HCl} = 0,3(mol)$
$HCl + NaOH \to NaCl + H_2O$
$n_{HCl\ dư} = n_{NaOH} = 0,06(mol)$
$\Rightarrow n_{HCl\ pư} = 0,3 - 0,06 = 0,24(mol)$
Gọi n hóa trị của X
$2X + 2nHCl \to 2XCl_n + nH_2$
Theo PTHH :
$n_X = \dfrac{1}{n}.n_{HCl} = \dfrac{0,24}{n}(mol)$
$\Rightarrow \dfrac{0,24}{n}.X = 2,88 \Rightarrow X = 12n$
Với n = 2 thì $X = 24(Magie)$
Đúng 2
Bình luận (0)
Cho 9,6 gam hỗn hợp X gồm Mg và Fe3O4 vào 300ml dung dịch HNO3 2M thu được dung dịch Y và 0,896 lít (đktc) hỗn hợp N2O và NO có tỷ khối so với hidro là 16,75. Trung hòa Y cần dung 40ml NaOH 1M thu được dung dịch A, cô cạn A thu được m gam muối khan. Biết rằng phản ứng xảy ra hoàn toàn và khi cô cạn muối không bị nhiệt phân. Giá trị m là: A. 42,26. B. 19,76 C. 28,46 D. 72,45
Đọc tiếp
Cho 9,6 gam hỗn hợp X gồm Mg và Fe3O4 vào 300ml dung dịch HNO3 2M thu được dung dịch Y và 0,896 lít (đktc) hỗn hợp N2O và NO có tỷ khối so với hidro là 16,75. Trung hòa Y cần dung 40ml NaOH 1M thu được dung dịch A, cô cạn A thu được m gam muối khan. Biết rằng phản ứng xảy ra hoàn toàn và khi cô cạn muối không bị nhiệt phân. Giá trị m là:
A. 42,26.
B. 19,76
C. 28,46
D. 72,45
Cho 9,6 gam hỗn hợp X gồm Mg và Fe3O4 vào 300ml dung dịch HNO3 2M thu được dung dịch Y và 0,896 lít (đktc) hỗn hợp N2O và NO có tỷ khối so với hidro là 16,75. Trung hòa Y cần dung 40ml NaOH 1M thu được dung dịch A, cô cạn A thu được m gam muối khan. Biết rằng phản ứng xảy ra hoàn toàn và khi cô cạn muối không bị nhiệt phân. Giá trị m là: A. 42,26 B. 19,76 C. 28,46 D. 72,45
Đọc tiếp
Cho 9,6 gam hỗn hợp X gồm Mg và Fe3O4 vào 300ml dung dịch HNO3 2M thu được dung dịch Y và 0,896 lít (đktc) hỗn hợp N2O và NO có tỷ khối so với hidro là 16,75. Trung hòa Y cần dung 40ml NaOH 1M thu được dung dịch A, cô cạn A thu được m gam muối khan. Biết rằng phản ứng xảy ra hoàn toàn và khi cô cạn muối không bị nhiệt phân. Giá trị m là:
A. 42,26
B. 19,76
C. 28,46
D. 72,45
Định hướng tư duy giải
Ta có:
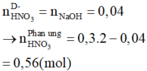
Và N 2 O : 0 , 01 mol NO : 0 , 03 mol
Với kim loại Mg thường cho muối NH 4 +
Ta đặt:
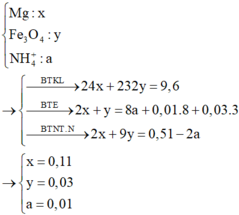
→ BTKL + BTNT 0 , 11 . 24 + 62 . 2 + 0 , 09 56 + 62 . 3 + 0 , 01 . 80 = 38 , 86 g a m
Đúng 0
Bình luận (0)