Đốt nóng 6,4g bột đồng trong khí clo người ta thu được 13,5g đồng clorua.Hãy cho biết:
a)CTHH đơn giản của đồng clorua.Giả sử rằng chứa biết hóa trị của đồng và clorua
b)Tính thể tích clo đã tham gia p.ứ với đồng ở đktc
11/ Đốt nóng 1,35 g bột nhôm trong khí Clo thu được 6,675g Nhôm Clorua cho biết :
a) Công thức đơn giản của Nhôm Clorua ( giả sử chưa biết hóa trị của Al và Cl )
b) Viết PTHH của phản ứng và tính thể tích khí Clo ( đktc) đã tham gia phản ứng với Al .
\(PTHH:2Al+3Cl_2\) → \(2AlCl_3\)
\(n_{Al}=\dfrac{m}{M}=\dfrac{1,35}{27}=0,05\left(mol\right)\)
Theo PTHH
⇒ \(n_{Cl_2}=\dfrac{3}{2}n_{Al}=\dfrac{3}{2}.0,05=0,075\left(mol\right)\)
⇒ \(V_{Cl_2\left(đktc\right)}=n.22,4=0,075.22,4=1,68\left(l\right)\)
Đốt nóng 1,35g bột nhôm trong khi clo, người ta thu được 6,675g nhôm clorua. Em hãy cho biết: Công thức hóa học đơn giản của nhôm clorua, giải sử rằng ta chưa biết hóa trị của nhôm và clo.
m C l = m A l C l 3 - m A l = 6,675 - 1,35 = 5,325 g
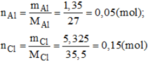
n C l = 3 . n A l ⇒ số nguyên tử Cl gấp 3 số nguyên tử Al. Công thức hóa học đơn giản của nhôm clorua: A l C l 3
Đun nóng 3.2 g bột đồng trong khí clo, người ta thu được 6.75 g đồng clorua. Tìm công thức đơn giản của đồng clorua
Giúp mk nha. Thank you💖💖💖💖💖💖
Đặt công thức đơn giản của đồng clorua là \(Cu_xCl_y\left(x,y\inℕ^∗\right)\)
Ta có : \(n_{Cu}=\frac{3,2}{64}=0,05\left(mol\right)\)
\(PTHH:2xCu+yCl_2\rightarrow^{t^o}2Cu_xCl_y\)
\(\left(mol\right):0,05\rightarrow\) \(\frac{0,05}{x}\)
\(\Rightarrow m_{Cu_xCl_y}=m.M=\frac{0,05}{x}.\left(64x+35,5y\right)\)\(hay:6,75=\frac{0,05}{x}.\left(64x+35,5y\right)\)
\(\Leftrightarrow6,75x=0,05.\left(64x+35,5y\right)\)\(\Leftrightarrow6,75x=3,2x+1,775y\Leftrightarrow6,75x-3,2x=1,775y\)
\(\Leftrightarrow3,55x=1,775y\Rightarrow\frac{x}{y}=\frac{1,775}{3,55}=\frac{1}{2}\)
Vậy công thức đơn giản của đồng clorua là \(CuCl_2\)
Đốt nóng 1,35g bột nhôm trong khi clo, người ta thu được 6,675g nhôm clorua. Em hãy cho biết: Thể tích khí clo (đktc) đã tham gia phản ứng với nhôm.
Câu 1:Tính khối lượng đồng và thể tích khí clo (đktc) đã tham gia phản ứng nếu có 27 gam CuCl2 tạo thành sau phản ứng
Câu 2: Đốt nhôm trong khí clo người ta thu được 26,7 gam nhôm clorua. Tính khối lượng nhôm và thể tích clo (ở đktc) đã tham gia phản ứng
Đốt cháy 12,8g đồng trong lọ chứa khí Clo. Sau phản ứng thu được muối đồng (II) Clorua ( Cu (II) và Cl ), phản ứng xảy ra hoàn toàn
a, viết PTHH xảy ra ?
b, Tính thể tích khí Clo ở đktc đã tham gia phản ứng ?
c, Tính khối lượng muối đồng (II) clorua thu được ?
a. Cu+Cl2-> CuCl2
1 1 1 (mol)
0,2 0,2 0,2(mol)
nCu=m/M=12,8:64=0,2 mol
b. VCl2= n.22,4= 0,2.22,4= 4,48 (l)
c. mCl2= n.M=0,2. 71= 14,2 g
K nha
đốt cháy 12,8g đồng trong lọ chứa khí clo. sau phản ứng thu được muối đồng (II) Clorua ( Cu (II) và Cl ), phản ứng xảy ra hoàn toàn
a) Viết PTHH xảy ra?
b) Tính thế tích khí Clo ở đktc đã tham gia phản ứng?
c) Tính khối lượng muối đồng (II) Clorua thu được?
a, PTHH:\(Cu+Cl_2\rightarrow CuCl_2\)
b, \(n_{Cu}=\frac{m}{M}=\frac{12,8}{64}=0,2\left(mol\right)\)
Ta thấy \(n_{CuCl_2}=n_{Cl_2}=n_{Cu}=0,2\left(mol\right)\)
\(V_{Cl_2}=n_{Cl_2}.22,4=0,2.22,4=4,48\left(l\right)\)
c, \(m_{CuCl_2}=n_{CuCl_2}.M=0,2.135=27\left(g\right)\)
Câu 2: Đốt nóng bột nhôm trong khí clo, người ta thu được 13,35g nhôm clorua AlCl3.
a/ Viết PTHH của phản ứng
b/ Tính thể tích khí clo cần dùng.
c/ Tính khối lượng bột nhôm tham gia phản ứng.
a) 2Al + 3Cl2 --to--> 2AlCl3
b) \(n_{AlCl_3}=\dfrac{13,35}{133,5}=0,1\left(mol\right)\)
PTHH: 2Al + 3Cl2 --to--> 2AlCl3
0,1<-0,15<---------0,1
=> VCl2 = 0,15.22,4 = 3,36(l)
c) mAl = 0,1.27 = 2,7(g)
\(a.PTHH:2Al+3Cl_2\overset{t^o}{--->}2AlCl_3\)
b. Ta có: \(n_{AlCl_3}=\dfrac{13,35}{133,5}=0,1\left(mol\right)\)
Theo PT: \(n_{Cl_2}=\dfrac{3}{2}.n_{AlCl_3}=\dfrac{3}{2}.0,1=0,15\left(mol\right)\)
\(\Rightarrow V_{Cl_2}=0,15.22,4=3,36\left(lít\right)\)
c. Theo PT: \(n_{Al}=n_{AlCl_3}=0,1\left(mol\right)\)
\(\Rightarrow m_{Al}=0,1.27=2,7\left(g\right)\)
Đốt nóng 1,35g bột nhôm trong khi clo, người ta thu được 6,675g nhôm clorua. Em hãy cho biết: Phương trình hóa học của nhôm tác dụng với khí clo.
Phương trình hóa học: 2 A l + 3 C l 2 → 2 A l C l 3