b)đốt cháy hoàn toàn m gam chất X cần dùng 4,48 lít khí O2 (đktc)thu được 2,24 lít CO2(đktc)và 3,6 gam H2O . viết sơ dồ phản ứng và tính khối lượng chất ban đầu đem đốt
giúp mk với
Đốt cháy hoàn toàn m gam chất X cần dùng 4,48 lít O 2 (đktc) thu được 2,24 lít C O 2 (đktc) và 3,6 gam H 2 O . Hãy tính khối lượng chất ban đầu đem đốt.
Sơ đồ X + O 2 → C O 2 + H 2 O ( 1 )
Áp dụng định luật bảo toàn khối lượng cho sơ đồ (1), ta có :
m + m O 2 = m C O 2 + m H 2 O
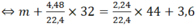
⇔ m = 1,6 gam
Đốt cháy hoàn toàn m gam chất X dung 4,48 lít O 2 (đktc) thu được 2,24 lít C O 2 (đktc) và 3,6 gam H 2 O . Xác định khối lượng chất X đem dùng.
@ tính khối lượng,thể tích(ở đktc) và số phân tử CO2 có trong 0,5 mol khí CO2
đốt cháy hoàn toàn m gam chất X càn dùng 4,8 lít khí 02(dktc) thu được 2,24 lít CO2(đktc) và 3,6 gam H2O. Viết theo sơ đồ phảm ứng và tính khổi lượng chất ban đầu đem đốt
\(V_{CO_2}=0,5.22,4=11,2\left(l\right)\)
\(A_{CO_2}=0,5.6.10^{23}=3.10^{23}\) (phân tử \(CO_2\) )
2.
\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
=> \(n_C=n_{CO_2}=0,1\left(mol\right)\) (1)
=> \(n_O=2nCO_2=0,1.2=0,2\left(mol\right)\) (*)
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\)
=> \(n_H=2n_{H_2O}=0,2.2=0,4\left(mol\right)\) (2)
=> \(n_O=n_{H_2O}=0,2\left(mol\right)\) (**)
\(n_{O_2}=\dfrac{4,8}{22,4}=0,2\left(mol\right)\)
=> \(n_O=2n_{O_2}=2.0,2=0,4\left(mol\right)\) (3)
\(X+O_2\underrightarrow{t^o}CO_2+H_2O\)
Từ (1),(2),(3), (*), (**) suy ra: \(n_C:n_H:n_O=0,1:0,4:0\)
=> Công thức tổng quát của X là \(C_xH_y\)
có: \(x:y=n_C:n_H=0,1:0,4=1:4\)
=> X là: \(CH_4\)
Sơ đồ pứ: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(m_{CH_4}=3,6+0,2.44-0,2.32=6\left(g\right)\)
đốt cháy hoàn toàn m gam chất X cần dùng 4,48lít khí O2(đktc) thu đc 4,4g CO2 và3,6g H2O.Viết sơ đồ phản ứng và tính khối lượng X ban đầu đem đốt
a, Tính thể tích của oxi (đktc) cần dùng để đốt cháy hết 3,1 gam P, biết phản ứng sinh ra chất rắn P2O5.
b, Đốt cháy hoàn toàn 1,12 lít khí CH4 (đktc) cần dùng V lít khí O2 (đktc), sau phản ứng thu được sản phẩm là khí cacbonic (CO2) và nước (H2O). Giá trị của V là
a, Theo giả thiết ta có: \(n_P=\dfrac{3,1}{31}=0,1\left(mol\right)\)
\(4P+5O_2--t^o->2P_2O_5\)
Ta có: \(n_{O_2}=\dfrac{5}{4}.n_P=0,125\left(mol\right)\Rightarrow V_{O_2\left(đktc\right)}=0,125.22,4=2,8\left(l\right)\)
b, Theo giả thiết ta có: \(n_{CH_4}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
\(CH_4+2O_2--t^o->CO_2+2H_2O\)
Ta có: \(n_{O_2}=2.n_{CH_4}=0,1\left(mol\right)\Rightarrow V_{O_2\left(đktc\right)}=2,24\left(l\right)\)
Đốt cháy hoàn toàn m gam hợp chất hữu cơ X ( C, H, O ). Cần vừa đủ 6,72 lít O 2 (đktc), thu được 4,48 lít CO 2 (đktc) và 5,4 gam H 2 O . Thành phần phần trăm khối lượng oxi trong X là
A. 34,78%
B. 69,56 %
C. 76,19 %
D. 67,71%
Đốt cháy hoàn toàn chất X cần dùng 3,36 lít khí O2 thu được 2,24 lít khí CO2 và 3,6 gam H2O. (biết các khí đo ở đktc). Xác định công thức hóa học của X? (biết công thức đơn giản cũng chính là công thức hóa học của X)
Mọi người giúp mình với !!!
nO2= 0,15(mol)
nCO2 = 0,1 (mol)-> nC=0,1 (mol)
nH2O=0,2(mol) -> nH= 0,4(mol)
n(O,sản phẩm)=0,1.2+0,2=0,4(mol) > 0,15.2 =0,3(mol)
=> X gồm 3 nguyên tố: C,H,O
Gọi CTTQ là CxHyOz (x,y,z:nguyên,dương)
z=0,4-0,3=0,1(mol)
x=nC=0,1(mol); y=nH=0,4(mol)
=>x:y:z=0,1:0,4:0,1=1:4:1
=> CTĐG của X cũng chín là CTHH của X là: CH4O
Đốt cháy hoàn toàn m gam hợp chất hữu cơ A cần dùng 11,2 gam khí oxi, thu được 8,8 gam C O 2 và 5,4 gam H 2 O . Ở đktc 2,24 lít khí A có khối lượng 3 gam. Xác định CTPT của A?
A. C 2 H 6
B. C 2 H 4
C. C 3 H 8
D. C 3 H 6
n O 2 = 11,2/32 = 0,35 mol
n C O 2 = 8,8/44 = 0,2 mol ⇒ n C = 0,2 mol
n H 2 O = 5,4/18 = 0,3 mol
⇒ n H = 2.0,3 = 0,6 mol
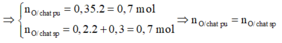
Vậy hợp chất hữu cơ A chỉ có C và H.
Gọi CTTQ của A là C x H y , khi đó ta có:
Vậy CTĐGN của A là C H 3 n
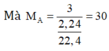
⇒ n = 30/15 = 2
Vậy A là C 2 H 6 .
⇒ Chọn A.
Đốt cháy hoàn toàn 6 gam este X bằng lượng O2 vừa đủ, thu được 4,48 lít khí CO2 (đktc) và 3,6 gam H2O. Công thức phân tử của X là
A. C3H6O2
B. C2H4O2
C. C4H6O2
D. C4H8O2
Đáp án : B
nC = nCO2 = 0,2 mol ; nH = 2nH2O = 0,4 mol
CÓ : mX = mC + mH + mO => nO = 0,2 mol
=> nC : nH : nO = 0,2 : 0,4 : 0,2 = 1 : 2 : 1
Vì X là este => số O chẵn
=> Nếu số O = 2 => C2H4O2