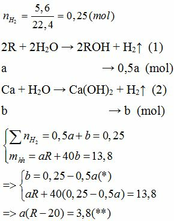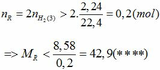1)Cho 3,33g kim loại kiềm R tác dụng hết với nước thu được 0,48g H2.
A) tìm tên R
B) trung hoà dung dịch sau phản ứng bằng 200 ml dung dịch HCl xM, tìm x.
2) Cho 0,6g kim loại kiềm thổ R tác dụng hết với nước sinh ra 0,336 ml H2 đkc
A) tìm tên R
B) khô cạn dung dịch sau phản ứng thì thư được bao nhiêu g rắn.