4.3 Cho biết sơ đồ 1 số nguyên tử sau
Hãy chỉ ra số p trong hạt nhân , số e trong nguyên tử , số lớp e và số e lớp ngoài cùng của mỗi nguyên tử . Vẽ hơi xấu nhé
Biết số proton trong hạt nhân của oxi là 8, kali là 19, clo là 17, silic là 14, canxi là 20, nhôm là 13, lưu huỳnh là 16. Hãy xác định số electron trong các nguyên tử sau : S i O 2 ; A l 2 O 3 ; C a C l 2 ; K C l .
Đáp án
Số electron của S i O 2 là 14 + 8 x 2 = 30 electron
Số electron của A l 2 O 3 là 13 x 2 + 8 x 3 = 50 electron
Số electron của C a C l 2 là 20 + 17 x 2 = 54 electron
Số electron của KCl là 19 + 17 = 36 electron
câu 1: Cho nguyên tử Silic có số P=14 và nguyên tử cacbon có số P=6 a.Hãy vẽ sơ đồ cấu tạo nguyên tử của hai nguyên tử. b. Cho biết điểm giống và khác nhau của hai nguyên tử trên Câu 2: Mỗi hợp chất có phân tử gồm hai nguyên tử X liên kết với 5 nguyên tử Oxy và nặng hơn nguyên tử Flo là 4 lần a. Xác định phân tử khối của hợp chất b. Xác định nguyên tử khối của Z. Cho biết Z là nguyên tố nào. Viết kí hiệu hóa học. Câu 3: a. Tính hóa trị Cu trong hợp chất CuO b. Lập công thức hóa học của hợp chất tạo bởi Fe có hóa trị III và SO4 có hóa trị II c. Cho biết ý nghĩa công thức hóa học hợp chất mới lập được ( cho Fe=56, S=32, Cu=64, Na= 23) Câu 4: Nguyên tử D có tổng số các hạt là 40 trong đó số hạt mang điện chiếm 35%. Tính số hạt mỗi loại
Biết số proton trong hạt nhân của oxi là 8, kali là 19, clo là 17, silic là 14, canxi 20, nhôm là 13, lưu huỳnh là 16. Phân tử nào sau đây có số electron nhiều nhất?
A. S i O 2
B. A l 2 O 3
C. C a C l 2
D. KCl
Chọn C
Số electron của C a C l 2 là: 20 + 17 x 2 = 54 electron.
Có thể vẽ sơ đồ đơn giản gồm vòng tròn con là hạt nhân, mỗi vòng cung nhỏ là một lớp với số electron của lớp ghi ở chân. Thí dụ sơ đồ đơn giản của nguyên tử sillic trong bài tập 4.3 như sau:
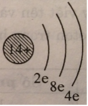
Biết rằng, trong nguyên tử các electron có ở lớp 1 (tính từ hạt nhân) tối đa là 2e, ở lớp 2 tối đa là 8e, ở lớp 3 tạm thời cũng là 8e, nếu còn electron sẽ ở lớp 4.
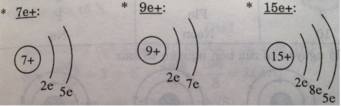
Vẽ sơ đồ đơn giản của năm nguyên tử mà trong hạt nhân có số proton bằng 7, 9, 15, 17, 19.
Nguyên tử có hạt nhân có số proton lần lượt à 7e+; 9e+; 15e+; 17e+; 19e+.

Vẽ mô hình nguyên tử
a)của oxi,biết oxi có số p là 8;có 2 lớp e;lớp ngoài cùng có 6e
b)của neon biết neon có số p là 10;có 2 lớp e;lớp ngoài cùng có 8e
c)của kali,biết kali có số p là 19;có 4 lớp e;lớp ngoài cùng có 1e
d)của crom,biết crom có số p là 24;có 4 lớp e;lớp ngoài cùng có 6e
Cho sơ đồ minh họa thành phần cấu tạo của một số nguyên tử dưới đây:
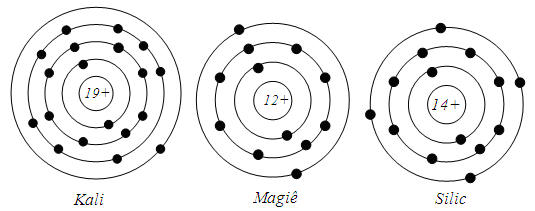
Số lớp e của nguyên tử Silic là:
1
4
3
2
Theo sơ đồ một số nguyên tử ở bài tập 4.3, hãy chỉ ra: Nguyên tử nào có số lớp electron như nguyên tử natri. (xem sơ đồ trong Bai 4 - SGK).
Nguyên tử sillic có cùng số lớp electron như nguyên tử natri. (3 lớp e)
Cho sơ đồ chuyển hóa sau:
X → C H 3 O H / H C l , t ° Y → C 2 H 5 O H / H C l , t ° Z → N a O H d u T
Biết X là axit glutamic. Y, Z, T là các chất hữu cơ chứa Nito. Số nguyên tử hiđro của Y và T là :
A. 12 và 7
B. 14 và 7
C. 13 và 8
D. 15 và 8
X : H O O C − [ C H 2 ] 2 − C H ( N H 2 ) − C O O H
Y : H O O C − [ C H 2 ] 2 − C H ( N H 3 C l ) − C O O C H 3 → số H của Y là 12
Z : C 2 H 5 O O C − [ C H 2 ] 2 − C H ( N H 3 C l ) − C O O C H 3
T : N a O O C − [ C H 2 ] 2 − C H ( N H 2 ) − C O O N a → số H của T là 7
Đáp án cần chọn là: A
Có thể vẽ sơ đồ đơn giản gồm vòng tròn con là hạt nhân, mỗi vòng cung nhỏ là một lớp với số electron của lớp ghi ở chân. Thí dụ sơ đồ đơn giản của nguyên tử sillic trong bài tập 4.3 như sau:
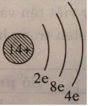
Biết rằng, trong nguyên tử các electron có ở lớp 1 (tính từ hạt nhân) tối đa là 2e, ở lớp 2 tối đa là 8e, ở lớp 3 tạm thời cũng là 8e, nếu còn electron sẽ ở lớp 4.
Mấy nguyên tử có số electron ở lớp ngoài cùng bằng 5, mấy nguyên tử có số electron ở lớp ngoài cùng bằng 7 ?
- Hai nguyên tử có số eletron lớp ngoài cùng là 5.
- Hai nguyên tử có số electron ngoài cùng 7.
Cho sơ đồ minh họa thành phần cấu tạo của một số nguyên tử dưới đây:
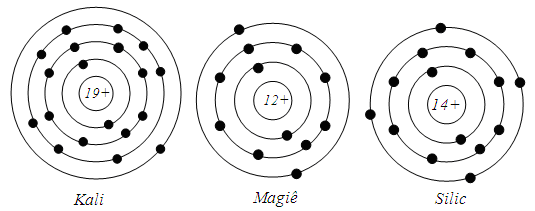
Tổng số hạt mang điện trong nguyên tử Kali là:
38
4
19
1