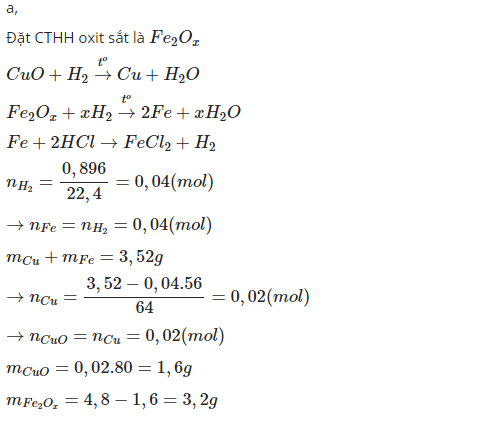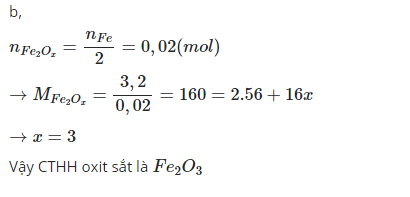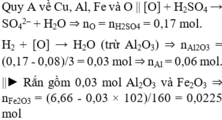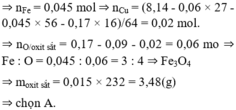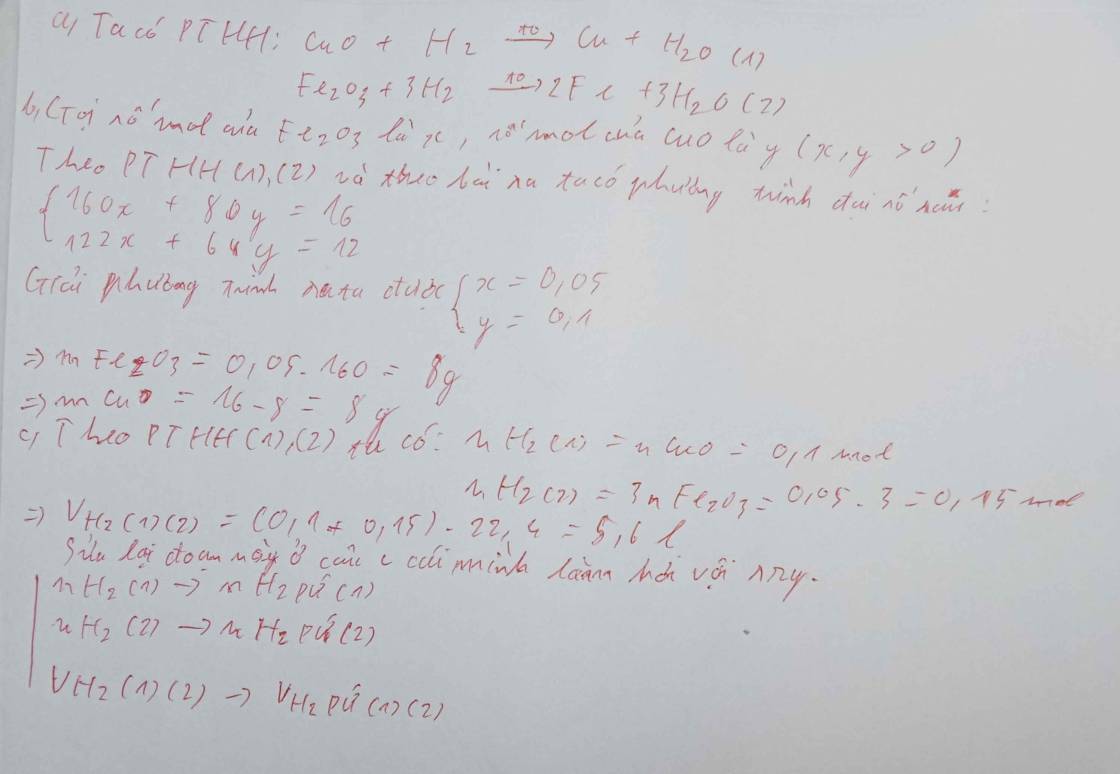cho một dòng khí h2 dư qua 4.8g hỗn hợp Cuo và 1 oxit sắt nung nóng thu được 0.896 lít H2 . Xác định khối lượng của mỗi oxit trong hỗn hợp và công thức phân tử của oxit sắt

Những câu hỏi liên quan
Cho một dòng khí hiđrô dư qua 4,8 gam hỗn hợp CuO và một oxit sắt nung nóng thu được 3,52 gam chất rắn. Đem chất rắn đó hòa tan trong axit HCl dư thu được 0,896 lit khí(đktc).
a. Xác định khối lượng mỗi oxit trong hỗn hợp.
b. Xác định công thức phân tử oxit sắt
Bài 1: Cho 3,6g một oxit sắt vào dung dịch HCl dư. Sau khi phản ứng xảy ra hoàn toàn thu được một muối sắt clorua. Hãy xác định công thức phân tử của oxit sắtBài 2: Dẫn 5,61 lít (đktc) hỗn hợp 2 khí CO và H2 từ từ qua hỗn hợp 2 oxit CuO và FeO nung nóng lấy dư, sau phản ứng thấy khối lượng hỗn hợp giảm a gama) Viết các PTHHb) Tính ac) Tính % theo thể tích của cá khí, biết tỉ khối hỗn hợp khí so với khí CH4 là 0,4
Đọc tiếp
Bài 1: Cho 3,6g một oxit sắt vào dung dịch HCl dư. Sau khi phản ứng xảy ra hoàn toàn thu được một muối sắt clorua. Hãy xác định công thức phân tử của oxit sắt
Bài 2: Dẫn 5,61 lít (đktc) hỗn hợp 2 khí CO và H2 từ từ qua hỗn hợp 2 oxit CuO và FeO nung nóng lấy dư, sau phản ứng thấy khối lượng hỗn hợp giảm a gam
a) Viết các PTHH
b) Tính a
c) Tính % theo thể tích của cá khí, biết tỉ khối hỗn hợp khí so với khí CH4 là 0,4
Xem thêm câu trả lời
Cho một dòng khi hiđrô dư qua 4,8 gam hỗn hợp CuO và một oxit sắt nung nóng thu được 3,52 gam chất rắn. Đem chất rắn đó hòa tan trong axit HCl dư thu được 0,896 lit khi(dktc). a. Xác định khối lượng mỗi oxit trong hỗn hợp. b. Xác định công thức phân tử oxit sắt Giúp mình với!
PTHH: \(CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\) (1)
\(Fe_xO_y+yH_2\xrightarrow[t^o]{}xFe+yH_2O\) (2)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\) (3)
a) Ta có: \(n_{H_2\left(3\right)}=\dfrac{0,896}{22,4}=0,04\left(mol\right)=n_{Fe}\) \(\Rightarrow n_{Cu}=\dfrac{3,52-0,04\cdot56}{64}=0,02\left(mol\right)=n_{CuO}\)
\(\Rightarrow\left\{{}\begin{matrix}m_{CuO}=0,02\cdot80=1,6\left(g\right)\\m_{Fe_xO_y}=4,8-1,6=3,2\left(g\right)\end{matrix}\right.\)
b) Theo PTHH: \(n_{Fe_xO_y}=\dfrac{0,04}{x}=\dfrac{3,2}{56x+16y}\)
\(\Rightarrow0,96x=0,64y\) \(\Rightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
Vậy CTPT cần tìm là Fe2O3
Đúng 2
Bình luận (0)
PTHH: CuO+H2to→Cu+H2OCuO+H2→toCu+H2O (1)
FexOy+yH2→toxFe+yH2OFexOy+yH2→toxFe+yH2O (2)
Fe+2HCl→FeCl2+H2↑Fe+2HCl→FeCl2+H2↑ (3)
a) Ta có: ⇒nCu=3,52−0,04⋅5664=0,02(mol)=nCuO⇒nCu=3,52−0,04⋅5664=0,02(mol)=nCuO
⇒{mCuO=0,02⋅80=1,6(g)mFexOy=4,8−1,6=3,2(g)⇒{mCuO=0,02⋅80=1,6(g)mFexOy=4,8−1,6=3,2(g)
b) Theo PTHH: ⇒xy=23⇒xy=23
Vậy CTPT cần tìm là Fe2O3
Đúng 0
Bình luận (0)
Nung nóng 2,4 g hỗn hợp CuO và một oxit sắt (FexOy), rồi cho luồng khí H2 đi qua cho
đến khi khử hết các oxit thì thu được 1,76 g chất rắn. Nếu hoà tan chất rắn đó bằng dung dịch
HCl dư thì thấy có 0,448 lít khí H2 (đktc) thoát ra. Xác định công thức của oxit sắt đó? Cho biết số mol của 2 oxit trong hỗn hợp bằng nhau
nH2= 0,448/22,4= 0,02(mol)
PTHH :
CuO + H2 -tdo--> Cu + H20
FexOy + yH2 -tdo-> xFe + yH20
Cu + HCl --> k pu
Fe + 2HCl ---> FeCl2 + H2
0,02 -- 0,04---> 0,02 --- 0,02 (mol)
mFe = 0,02 .56= 1,12(g)
=> mCu = 1,76 - 1,12= 0,64(g)
n Cu = 0,64 /64 =0,01(mol)
PTHH :
CuO + H2 -tdo-> Cu + H20
0,,01 --0,01 ----> 0,01(mol)
mCuO= 0,01 . 80 = 0,8(g)
=> mFexOy = 2,4-0,8= 1,6(g)
PTHH :
FexOy + yH2 ---> xFe + yH20
56x+ 16y ---------> 56x
1,6 (g) -------------> 1,12(g)
<=> 1,6 .56x = 1,12( 56x + 16y)
<=> 89,6x = 62,72 x + 17,92y
<=> 89,6x - 62,72x = 17,92y
<=> 26,88 x = 17,92y
=> x/y= 17,92 / 26,88 =2/3
Vậy công thức đúng là Fe203.
Đúng 0
Bình luận (0)
Hỗn hợp A có khối lượng 8,14 gam gồm: CuO,
Al
2
O
3
và một oxit sắt. Cho
H
2
dư qua A nung nóng, sau khi phản ứng xong thu được 1,44 gam
H
2
O
. Hòa tan hoàn toàn A cần 170 ml dung dịch...
Đọc tiếp
Hỗn hợp A có khối lượng 8,14 gam gồm: CuO, Al 2 O 3 và một oxit sắt. Cho H 2 dư qua A nung nóng, sau khi phản ứng xong thu được 1,44 gam H 2 O . Hòa tan hoàn toàn A cần 170 ml dung dịch H 2 SO 4 1M loãng được dung dịch B. Cho B tác dụng với NH 3 dư lọc lấy kết tủa đem nung trong không khí thu được 6,66 gam chất rắn. Công thức phân tử của oxit sắt và khối lượng của nó trong A là
A. Fe3O4; 3,48 gam.
B. Fe3O4; 2,32 gam.
C. FeO; 1,44 gam.
D. Fe2O3; 1,60 gam.
Hỗn hợp A có khối lượng 8,14 gam gồm: CuO, Al2O3 và một oxit sắt. Cho H2 dư qua A nung nóng, sau khi phản ứng xong thu được 1,44 gam H2O. Hòa tan hoàn toàn A cần 170 ml dung dịch H2SO4 1M loãng được dung dịch B. Cho B tác dụng với NH3 dư lọc lấy kết tủa đem nung trong không khí thu được 6,66 gam chất rắn. Công thức phân tử của oxit sắt và khối lượng của nó trong A là A. Fe3O4; 3,48 gam. B. Fe3O4; 2,32 gam. C. FeO; 1,44 gam. D. Fe2O3; 1,60 gam.
Đọc tiếp
Hỗn hợp A có khối lượng 8,14 gam gồm: CuO, Al2O3 và một oxit sắt. Cho H2 dư qua A nung nóng, sau khi phản ứng xong thu được 1,44 gam H2O. Hòa tan hoàn toàn A cần 170 ml dung dịch H2SO4 1M loãng được dung dịch B. Cho B tác dụng với NH3 dư lọc lấy kết tủa đem nung trong không khí thu được 6,66 gam chất rắn. Công thức phân tử của oxit sắt và khối lượng của nó trong A là
A. Fe3O4; 3,48 gam.
B. Fe3O4; 2,32 gam.
C. FeO; 1,44 gam.
D. Fe2O3; 1,60 gam.
Chọn đáp án A
Quy A về Cu, Al, Fe và O || [O] + H2SO4 → SO42– + H2O ⇒ nO = nH2SO4 = 0,17 mol.
H2 + [O] → H2O (trừ Al2O3) ⇒ nAl2O3 = (0,17 - 0,08)/3 = 0,03 mol ⇒ nAl = 0,06 mol.
||► Rắn gồm 0,03 mol Al2O3 và Fe2O3 ⇒ nFe2O3 = (6,66 - 0,03 × 102)/160 = 0,0225 mol
⇒ nFe = 0,045 mol ⇒ nCu = (8,14 - 0,06 × 27 - 0,045 × 56 - 0,17 × 16)/64 = 0,02 mol.
⇒ nO/oxit sắt = 0,17 - 0,09 - 0,02 = 0,06 mo ⇒ Fe : O = 0,045 : 0,06 = 3 : 4 ⇒ Fe3O4
⇒ moxit sắt = 0,015 × 232 = 3,48(g) ⇒ chọn A.
Đúng 0
Bình luận (0)
Một hỗn hợp A có khối lượng 5,08g gồm CuO và một oxit của sắt. Hòa tan hoàn toàn A trong dd H 2 S O 4 đặc, nóng, dư thu được 0,168 lít khí S O 2 ở điều kiện tiêu chuẩn và dung dịch B chứa 12,2 gam muối sunfat. Xác định công thức của oxit sắt và % khối lượng từng oxit trong A?
Dẫn luồng khí H2 dư đi qua 16g hoá hợp A chứa hai oxit CuO và Fe2O3 nung nóng sau khi hỗn hợp kết thúc thu được 12g hỗn hợp B chứa 2 kim loại Đồng và Sắt a, Viết pthhb,Tính khối lượng mỗi oxit trong hoá hợp A c,Tính thể tích H2 đã dùng ở đktc
Đọc tiếp
Dẫn luồng khí H2 dư đi qua 16g hoá hợp A chứa hai oxit CuO và Fe2O3 nung nóng sau khi hỗn hợp kết thúc thu được 12g hỗn hợp B chứa 2 kim loại Đồng và Sắt
a, Viết pthh
b,Tính khối lượng mỗi oxit trong hoá hợp A
c,Tính thể tích H2 đã dùng ở đktc
Cho 1 dòng khí \(H_2\) dư đi qua 4,8 g hh gồm CuO và 1 oxit sắt nung nóng thu đc 3,52 g chất rắn. Nếu cho chất rắn đó hòa tan trong axit HCl thì thu đc 0,892 lít \(H_2\) ở đktc.
a) Tính khối lượng mỗi oxit trong hh ban đầu
b) Xác định công thức phân tử của oxit sắt
a)
Gọi \(\left\{{}\begin{matrix}n_{CuO}=a\left(mol\right)\\n_{Fe_xO_y}=b\left(mol\right)\end{matrix}\right.\)
=> 80a + b(56x + 16y) = 4,8 (1)
PTHH: CuO + H2 --to--> Cu + H2O
a------------->a
FexOy + yH2 --to--> xFe + yH2O
b----------------->bx
=> 64a + 56bx = 3,52 (2)
PTHH: Fe + 2HCl --> FeCl2 + H2
bx-------------------->bx
=> \(bx=\dfrac{0,892}{22,4}\approx0,04\left(mol\right)\)
(2) => a = 0,02 (mol)
(1) => by = 0,06
Xét \(\dfrac{bx}{by}=\dfrac{x}{y}=\dfrac{0,04}{0,06}=\dfrac{2}{3}\)
=> CTPT: Fe2O3
=> b = 0,02 (mol)
\(\left\{{}\begin{matrix}m_{CuO}=0,02.80=1,6\left(g\right)\\m_{Fe_2O_3}=0,02.160=3,2\left(g\right)\end{matrix}\right.\)
b) CTPT: Fe2O3
Đúng 0
Bình luận (0)