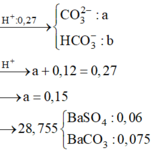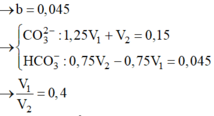trộn 500mk dung dịch hỗn hợp HCl 0,75M và H2SO4 1,25M với V(ml) dung dịch hỗn hợp NaOH 1M và Ba(OH)2 0,75M thu được dung dịch có pH=13 và a(g) kết tủa. tính V,a

Những câu hỏi liên quan
Cho từ từ 100 ml dung dịch chứa hỗn hợp NaHCO3 2M, Na2CO3 1M vào 100 ml dung dịch chứa HCl 1M và H2SO4 0,5M thu được V lít khí (đktc) và dung dịch X. Cho 100ml dung dịch Ba(OH)2 2M và NaOH 0,75M vào dung dịch X thu được m (g) kết tủa. Giá trị của m, V là: A. 45 gam và 2,24 lít B. 43 gam và 2,24 lít C. 41,2 gam và 3,36 lít D. 43 gam và 3,36 lít
Đọc tiếp
Cho từ từ 100 ml dung dịch chứa hỗn hợp NaHCO3 2M, Na2CO3 1M vào 100 ml dung dịch chứa HCl 1M và H2SO4 0,5M thu được V lít khí (đktc) và dung dịch X. Cho 100ml dung dịch Ba(OH)2 2M và NaOH 0,75M vào dung dịch X thu được m (g) kết tủa. Giá trị của m, V là:
A. 45 gam và 2,24 lít
B. 43 gam và 2,24 lít
C. 41,2 gam và 3,36 lít
D. 43 gam và 3,36 lít
Đáp án C
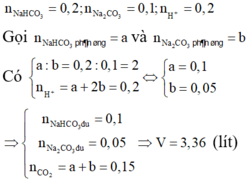
n Ba ( OH ) 2 = 0 , 2 ; n NaOH = 0 , 075
![]()
Đúng 0
Bình luận (0)
Trộn 100 ml dung dịch hỗn hợp gồm H2SO4, 0,05M và HCL 0,1M với 100 ml dung dịch hỗn hợp NaOH 0,2M và Ba(OH)2 0,1M, được dung dịch X. Tính giá trị pH của dung dịch X và tính khối lượng kết tủa thu được.
`100mL=0,1L`
`n_{H^+}=0,1.0,05.2+0,1.0,1=0,02(mol)`
`n_{SO_4^{2-}}=0,1.0,05=0,005(mol)`
`n_{OH^-}=0,1.0,2+0,1.0,1.2=0,04(mol)`
`n_{Ba^{2+}}=0,1.0,1=0,01(mol)`
`Ba^{2+}+SO_4^{2-}->BaSO_4`
Do `0,01>0,005->` Tính theo `SO_4^{2-}`
`n_{BaSO_4}=n_{SO_4^{2-}}=0,005(mol)`
`->m_↓=0,005.233=1,165(g)`
`H^{+}+OH^{-}->H_2O`
Do `0,02<0,04->OH^-` dư
`n_{OH^{-}\ pu}=n_{H^+}=0,02(mol)`
`->n_{OH^{-}\ du}=0,04-0,02=0,02(mol)`
Trong X: `[OH^-]={0,02}/{0,1+0,1}=0,1M`
`->pH=14-pOH=14+lg[OH^-]=13`
Đúng 4
Bình luận (0)
2,43 g Al tác dụng với 800 ml hỗn hợp gồm NaOH, KOH và Ba(OH)2 có pH hỗn hợp là 13, thu được dung dịch A. Cho 2,1lít dung dịch hỗn hợp gồm HCl và H2SO4 có pH=1 vào dung dịch A thu được m gam kết tủa. Giá trị của m là.
Xem chi tiết
Trộn 200 ml dung dịch chứa hỗn hợp HCl 0,1M và H2SO4 0,05M với 300 ml dung dịch Ba(OH)2 aM thu được m gam kết tủa và dung dịch có pH 13. Giá trị của a và m là A. 0,3 và 104,85. B. 0,3 và 23,3. C. 0,15 và 104,85. D. 0,15 và 23,3.
Đọc tiếp
Trộn 200 ml dung dịch chứa hỗn hợp HCl 0,1M và H2SO4 0,05M với 300 ml dung dịch Ba(OH)2 aM thu được m gam kết tủa và dung dịch có pH = 13. Giá trị của a và m là
A. 0,3 và 104,85.
B. 0,3 và 23,3.
C. 0,15 và 104,85.
D. 0,15 và 23,3.
Trộn 200 ml dung dịch chứa hỗn hợp HCl 0,1M và H2SO4 0,05M với 300 ml dung dịch Ba(OH)2 aM thu được m gam kết tủa và dung dịch có pH 13. Giá trị của a và m là A. 0,3 và 10,485 B. 0,3 và 2,33 C. 0,15 và 10,485 D. 0,15 và 2,33
Đọc tiếp
Trộn 200 ml dung dịch chứa hỗn hợp HCl 0,1M và H2SO4 0,05M với 300 ml dung dịch Ba(OH)2 aM thu được m gam kết tủa và dung dịch có pH = 13. Giá trị của a và m là
A. 0,3 và 10,485
B. 0,3 và 2,33
C. 0,15 và 10,485
D. 0,15 và 2,33
Dung dịch X chứa Na2CO3 0,5M và NaOH 0,75M; dung dịch Y chứa KHCO3 0,75M và K2CO3 1M. Trộn V1 lít dung dịch X với V2 lít dung dịch Y thu được dung dịch Z chỉ chứa các muối. Cho từ từ đến hết 200 ml dung dịch HCl 0,75M và H2SO4 0,3M vào dung dịch Z thu được 2,688 lít khí CO2 (đktc) và dung dịch G. Cho Ba(OH)2 dư vào dung dịch G thu được 28,755 gam kết tủa. Tỉ lệ V1 : V2 là A. 0,6 B. 0,5 C. 0,4 D. 0,75
Đọc tiếp
Dung dịch X chứa Na2CO3 0,5M và NaOH 0,75M; dung dịch Y chứa KHCO3 0,75M và K2CO3 1M. Trộn V1 lít dung dịch X với V2 lít dung dịch Y thu được dung dịch Z chỉ chứa các muối. Cho từ từ đến hết 200 ml dung dịch HCl 0,75M và H2SO4 0,3M vào dung dịch Z thu được 2,688 lít khí CO2 (đktc) và dung dịch G. Cho Ba(OH)2 dư vào dung dịch G thu được 28,755 gam kết tủa. Tỉ lệ V1 : V2 là
A. 0,6
B. 0,5
C. 0,4
D. 0,75
Trộn 100 ml dung dịch hỗn hợp gồm H2SO4 0,05M và HCl với 100 ml dung dịch hỗn hợp gồm NaOH 0,2M và Ba(OH)2 0,1M thu được dung dịch X. Dung dịch có pH là A. 13,0. B. 1,2. C. 12,8. D. 1,0.
Đọc tiếp
Trộn 100 ml dung dịch hỗn hợp gồm H2SO4 0,05M và HCl với 100 ml dung dịch hỗn hợp gồm NaOH 0,2M và Ba(OH)2 0,1M thu được dung dịch X. Dung dịch có pH là
A. 13,0.
B. 1,2.
C. 12,8.
D. 1,0.
Đáp án A
∑ nH+ = 2nH2SO4 + nHCl = 2. 0,1.0,05 + 0,1.0,1 = 0,02 (mol)
∑ nOH- = nNaOH + 2nBa(OH)2 = 0,1.0,2 + 2. 0,1.0,1 = 0,04 (mol)
H+ + OH- → H2O
0,02 → 0,02
=> nOH- dư = 0,04 – 0,02 = 0,02 (mol)
=> [OH-] = n: V = 0,02 : 0,2 = 0,01 M
pH = 14 + log(OH-) = 14 + (-1) = 13
Chú ý:
pH được tính theo giá trị của log[H+] chứ không phải log [OH-]
Đúng 0
Bình luận (0)
Trộn 100 ml dung dịch hỗn hợp gồm H2SO4 0,05M và HCl với 100 ml dung dịch hỗn hợp gồm NaOH 0,2M và Ba(OH)2 0,1M thu được dung dịch X. Dung dịch có pH là
A. 13,0.
B. 1,2.
C. 12,8.
D. 1,0.
Đáp án A
∑ nH+ = 2nH2SO4 + nHCl = 2. 0,1.0,05 + 0,1.0,1 = 0,02 (mol)
∑ nOH- = nNaOH + 2nBa(OH)2 = 0,1.0,2 + 2. 0,1.0,1 = 0,04 (mol)
H+ + OH- → H2O
0,02 → 0,02
=> nOH- dư = 0,04 – 0,02 = 0,02 (mol)
=> [OH-] = n: V = 0,02 : 0,2 = 0,01 M
pH = 14 + log(OH-) = 14 + (-1) = 13
Đúng 0
Bình luận (0)
Trộn 100 ml dung dịch hỗn hợp gồm H2SO4 0,05M và HCl với 100 ml dung dịch hỗn hợp gồm NaOH 0,2M và Ba(OH)2 0,1M thu được dung dịch X. Dung dịch có pH là A. 13,0. B. 1,2. C. 12,8 D. 1,0.
Đọc tiếp
Trộn 100 ml dung dịch hỗn hợp gồm H2SO4 0,05M và HCl với 100 ml dung dịch hỗn hợp gồm NaOH 0,2M và Ba(OH)2 0,1M thu được dung dịch X. Dung dịch có pH là
A. 13,0.
B. 1,2.
C. 12,8
D. 1,0.
Chọn A
∑ nH+ = 2nH2SO4 + nHCl = 2. 0,1.0,05 + 0,1.0,1 = 0,02 (mol)
∑ nOH- = nNaOH + 2nBa(OH)2 = 0,1.0,2 + 2. 0,1.0,1 = 0,04 (mol)
H+ + OH- → H2O
0,02 → 0,02
=> nOH- dư = 0,04 – 0,02 = 0,02 (mol)
=> [OH-] = n: V = 0,02 : 0,2 = 0,01 M
pH = 14 + log(OH-) = 14 + (-1) = 13
Đúng 0
Bình luận (0)