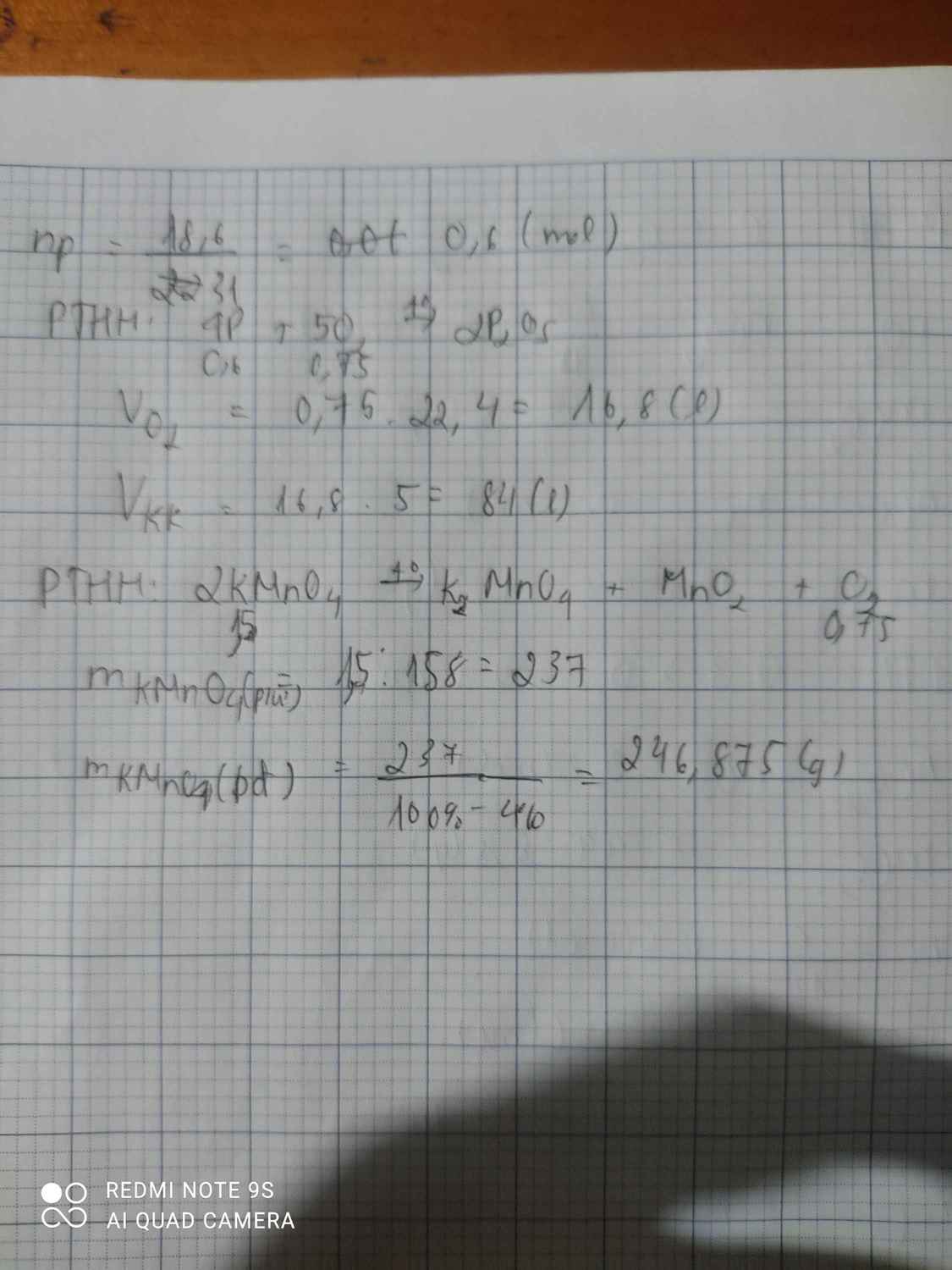Cần bao nhiêu gkg muối chứa 80% FeSO4 đẻ có một lượng oxi bằng lượng oxi trong 2kg thuốc tím chúa 94,8% KMnO4

Những câu hỏi liên quan
Cần bao gam muối chứa 80% Fe2(SO4)3 để có 1 lượng sắt bằng lượng sắt trong 1 tấn quặng Mahetit chứa 81,2%Fe3O4?Để có 1 lượng O bằng lượng O trong 2 kg thuốc tím chứa 94,8% KMnO4 Cần bao gam muối chứa 80% Fe2(SO4)3 để có 1 lượng sắt bằng lượng sắt trong 1 tấn quặng Mahetit chứa 81,2%Fe3O4?Để có 1 lượng O bằng lượng O trong 2 kg thuốc tím chứa 94,8% KMnO4
Cần bao gam muối chứa 80% Fe2(SO4)3 để có 1 lượng sắt bằng lượng sắt trong 1 tấn quặng Mahetit chứa 81,2%Fe3O4?
- Khối lượng Fe3O4 trong 1 tấn quặng Mahetit:
1.81,2% =0,812 ( tấn)
- Trong quặng manhetit ta có:
Fe3O4 --------> 3 Fe
232 g ..................112g
0,812 tấn...............x (tấn)
=> x=\(\dfrac{0,812.112}{232}=0,392\left(tấn\right)\)
- Mặc khác trong muối chứa 80% Fe2(SO4)3 ta có :
Fe2(SO4)3 ---------> 2 Fe
400g .......................112 g
y tấn <-------------------0,392 (tấn)
=>\(y=\dfrac{0,392.400}{112}=1,4\left(tấn\right)\)
Khối lượng muối chứa 80% Fe2(SO4)3 là: \(\dfrac{1,4}{80\%}=1,75\left(tấn\right)\)
Đúng 1
Bình luận (0)
Cần bao gam muối chứa 80% Fe2(SO4)3 để có 1 lượng O bằng lượng O trong 2 kg thuốc tím chứa 94,8% KMnO4
Khối lượng của KMnO4 trong 2 kg thuốc tím chứa 94,8% KMnO4
m KMnO4 = \(2.94,8\%\) = 1,896 kg
KMnO4 ----------> 2O2
158g ....................64 g
1,896kg .................x kg
=> x = \(\dfrac{1,896.64}{158}\)= 0,768 (kg)
Ta có :
2Fe2(SO4)3 ⟶ 2Fe2O3 + 6O2 + 6SO2
800g.....................................192g
y (kg).....................................0,768(kg)
=> y =\(\dfrac{0,768.800}{192}=3,2\left(kg\right)\)
=>Khối lượng muối cần dùng : \(\dfrac{3,2}{80\%}=4\left(kg\right)\)
Đúng 0
Bình luận (0)
Cần bao gam muối chứa 80% Fe2(SO4)3 để có 1 lượng sắt bằng lượng sắt trong 1 tấn quặng Mahetit chứa 81,2%Fe3O4?Để có 1 lượng O bằng lượng O trong 2 kg thuốc tím chứa 94,8% KMnO4
Trong phòng thí nghiệm cần dùng 28 bình chứa khí oxi để làm thí nghiệm, mỗi bình có dung tích là 100ml. Tính khối lượng thuốc tím (KMnO4) cần dùng để khi nhiệt phân thu đc đủ lượng khí oxi trên, biết khi thu lượng khí oxi bị hao hụt mất 20%
Giúp mik vs ạ mik cám ơn trc :33
\(V_{O_2\left(thu.được\right)}=28=0,1=2,8\left(l\right)\)
=> \(V_{O_2\left(sinh.ra\right)}=\dfrac{2,8.100}{80}=3,5\left(l\right)\)
=> \(n_{O_2\left(sinh.ra\right)}=\dfrac{3,5}{22,4}=0,15625\left(mol\right)\)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
0,3125<------------------------0,15625
=> mKMnO4 = 0,3125.158 = 49,375 (g)
Đúng 2
Bình luận (0)
( Toán hiệu suất)
a Tính thể tích khí oxi thu được ( ở đktc) khi đem nhiệt phân 94,8 gam thuốc tím ( KMno4). Biết phản ứng đạt hiệu suất 75%
b Để thu được 33,6 lít khí oxi ( ở đktc) cần dùng bao nhiêu gam thuốc tím? Biết phản ứng đạt hiệu suất 80%
a. \(2KMnO_4\rightarrow K_2MnO_4+MnO_2+O_2\)
\(n_{KMnO_4}=0,6mol\)
\(\rightarrow n_{O_2}=\frac{1}{2}n_{KMnO_4}=0,3mol\)
\(\rightarrow V_{O_2}=6,72l\)
\(V_{O_2\text{thực}}=\frac{6,72.75}{100}=5,04l\)
b. \(2KMnO_4\rightarrow K_2MnO_4+MnO_2+O_2\)
\(n_{O_2}=1,5mol\)
\(\rightarrow n_{KMnO_4}=2n_{O_2}=3mol\)
\(\rightarrow m_{KMnO_4\text{cần}}=\frac{474.100}{80}=592,5g\)
Đun nóng 40g thuốc tím thành phần chính là KMnO4 và 21 tạp chất trơ Tính khối lượng oxi thu được biết có 80% KMnO4 về khối lượng đã bị phân hủy
\(n_{KMnO_4} = \dfrac{40.(100\%-21\%)}{158} = 0,2(mol)\\ n_{KMnO_4\ pư} = 0,2.80\% = 0,16(mol)\\ 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ n_{O_2} = \dfrac{1}{2}n_{KMnO_4\ pư} = 0,08(mol)\\ m_{O_2} = 0,08.32 = 2,56(gam)\)
Đúng 1
Bình luận (0)
bn ơi cho mình hỏi 80% K2MnO4 của riêng hc hay là all sản phẩm?
Đúng 0
Bình luận (0)
khi nung nóng KMnO4 thu được K2MnO4,MnO2 và O2
a/viết PTHH xảy ra
b/nếu sau phản ứng thu được bao nhiêu chất rắn có khối lượng giảm đi 2,4g so với khối lượng chất rắn ban đàu thì có bao nhiêu KMnO4 đã bị phân hủy?
c/cần bao nhiêu gam thuốc tím (chứa 96% KMnO4 về khối lượng) đẻ có được lượng KMnO4 ở trên
a) \(2KMnO_4\underrightarrow{t^0}K_2MnO_4+MnO_2+O_2\)
b) Đặt x là số mol của \(KMnO_4\)
\(\Rightarrow n_{K_2MnO_4}=\frac{1}{2}n_{KMnO_4}=\frac{1}{2}x\)
Ta có : \(m_{KMnO_4}-m_{K_2MnO_4}=2,4\left(g\right)\)
\(\Leftrightarrow158x-\frac{197}{2}x=2,4\)
\(\Leftrightarrow x\approx0,04\left(mol\right)\)
\(\Rightarrow m_{KMnO_4}=0,04\times158=6,32\left(g\right)\)
Đun nóng 40g thuốc tím thành phần chính là KMnO4 và 21 tạp chất trơ Tính khối lượng oxi thu được biết có 80% KMnO4 về khối lượng đã bị phân hủy
\(\%m_{KMnO_4}=100\%-21\%=79\%\)
\(m_{KMnO_4}=40.79\%=31,6g\)
\(n_{KMnO_4}=\frac{31,6}{158}=0,2mol\)
\(n_{KMnO_4\text{phản ứng}}=80\%.0,2=0,16mol\)
PTHH: \(2KMnO_4\rightarrow^{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
Từ phương trình \(n_{O_2}=\frac{1}{2}.n_{KMnO_4\text{phản ứng}}=0,08mol\)
\(m_{O_2}=32.0,08=2,56g\)
Đốt cháy hoàn toàn 18,6g Photpho thì cần dùng bao nhiêu lít ko khí có chứa 20% thể tích oxi?
Nếu dùng thuốc tím chứa 4& tạp chất về khối lượng để điều chế Oxi đủ cho phản ứng trên thì cần dùng bao nhiêu g chất này?
Help me - Gấp lắm
10,2 gam Nhôm tác dụng hết với khí oxi (đktc) A. Viết PTHH B. Tính thể tích oxi (đktc) đã phản ứng C. Tính khối lượng sản phẩm thủ được D. Để điều chế được thể tích oxi cần dùng cho phản ứng trên ta cần bảo nhiêu gam thuốc tím ( Kmno4 ) (Al=27;O=16;K=39;Mn=55)
a, PT: \(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
Ta có: \(n_{Al}=\dfrac{10,2}{27}=\dfrac{17}{45}\left(mol\right)\)
b, Theo PT: \(n_{O_2}=\dfrac{3}{4}n_{Al}=\dfrac{17}{60}\left(mol\right)\)
\(\Rightarrow V_{O_2}=\dfrac{17}{60}.22,4\approx6,347\left(l\right)\)
c, Theo PT: \(n_{Al_2O_3}=\dfrac{1}{2}n_{Al}=\dfrac{17}{90}\left(mol\right)\)
\(\Rightarrow m_{Al_2O_3}=\dfrac{17}{90}.102\approx19,267\left(g\right)\)
d, PT: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
Theo PT: \(n_{KMnO_4}=2n_{O_2}=\dfrac{17}{30}\left(mol\right)\)
\(\Rightarrow m_{KMnO_3}=\dfrac{17}{30}.158\approx89,53\left(g\right)\)
Đúng 1
Bình luận (0)