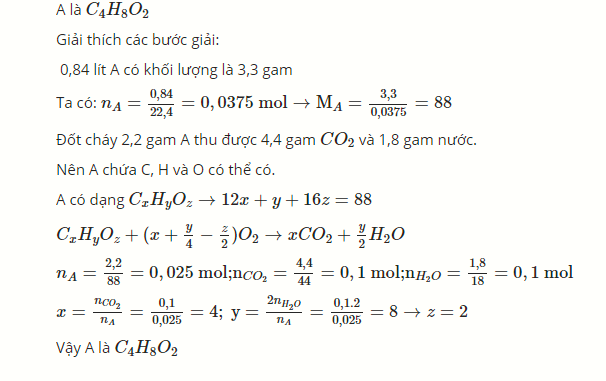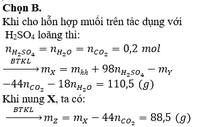Lập CTPT của hợp chất A gồm 82,35% N và H . Biết 4,48 lít A(đktc)có khối lượng là 3,4 gam

Những câu hỏi liên quan
đốt cháy hoàn toàn 2.2 gam hợp chất hữu cơ A thu được 4.4 gam CO₂ và 1.8 gam H₂O, ngoài ra không còn chất nào khác. Biết rằng 0.84 lít hơi hợp chất A(đktc) có khối lượng là 3.3 gam. Xác định CTPT của hợp chất A
Đốt cháy A thu được sản phẩm chứa C, H, O
=> A chứa C, H và có thể có O
\(n_{CO_2}=\dfrac{4,4}{44}=0,1\left(mol\right)\Rightarrow n_C=0,1\left(mol\right)\)
\(n_{H_2O}=\dfrac{1,8}{18}=0,1\left(mol\right)\Rightarrow n_H=0,2\left(mol\right)\)
Xét mC + mH = 0,1.12 + 0,2.1 = 1,4 (g) < 2,2 (g)
=> A chứa C, H, O
\(n_O=\dfrac{2,2-1,4}{16}=0,05\left(mol\right)\)
Xét nC : nH : nO = 0,1 : 0,2 : 0,05 = 2 : 4 : 1
=> CTPT: (C2H4O)n
\(M_A=\dfrac{3,3}{\dfrac{0,84}{22,4}}=88\left(g/mol\right)\)
=> n = 2
=> CTPT: C4H8O2
Đúng 2
Bình luận (0)
\(n_A=\dfrac{0,84}{22,4}=0,0375 (mol) \Rightarrow M_A = {3,3}{0,0375}=88 ( mol) \)
\(A có dạng : C_xH_yO_z \rightarrow 12x+y+16z = 88 \)
\(C_xH_yO_z + ( x+\dfrac{y}{4}-\dfrac{z}{2}) O_2 \rightarrow xCO_2+\dfrac{x}{y}H_2O \)
\(n_A = \dfrac{2,2}{88}=0,025 (mol) \)
\(n_{CO_2} = \dfrac{4,4}{44}=0,1(mol) \)
\(n_{H_2O} = \dfrac{1,8}{18}=0,1(mol) \)
\(x=\dfrac{n_{CO_2}}{n_A} = \dfrac{0,1}{0,025}=4;y=\dfrac{2n_{H_2O}}{n_A} =\dfrac{0,1.2}{0,025}=8 \rightarrow z=2\)
Đúng 0
Bình luận (0)
a. Lập công thức hoá học của hợp chất A biết MA17 gam/mol và phần trăm khối lượng của các nguyên tố lần lượt là %N 82,35% và %H 17,65%.
Đọc tiếp
a. Lập công thức hoá học của hợp chất A biết MA=17 gam/mol và phần trăm khối lượng của các nguyên tố lần lượt là %N= 82,35% và %H= 17,65%.
- Đặt công thức: NxHy
- Ta có tỉ lệ khối của các nguyên tố:
x.14/82,35 =y.1/17,65 =17/100 = 0,17
Suy ra : x =0,17.82,35/14 = 1
Suy ra : y = 0,17.17,65/1 = 3
Vậy CTHH là : NH3
( Dấu / là phép chia nhé chúc bạn làm bài tốt ![]() )
)
Đúng 1
Bình luận (0)
Lập công thức hóa học của các hợp chất: a) A gồm 40% Cu, 20% S, 40% O, biết khối lượng mol của A là 160. b) B gồm 82,35% N và 17,65% H, biết khối lượng mol của A là 17. c) C gồm 32,39% Na, 22,53% S và O, biết khối lượng mol của C là 142. d) D gồm 36,8% Fe, 21% S còn lại là O, biết khối lượng mol của D là 152
a)
\(m_{Cu}=\dfrac{160.40}{100}=64\left(g\right)=>n_{Cu}=\dfrac{64}{64}=1\left(mol\right)\)
\(m_S=\dfrac{160.20}{100}=32\left(g\right)=>n_S=\dfrac{32}{32}=1\left(mol\right)\)
\(m_O=\dfrac{40.160}{100}=64\left(g\right)=>n_O=\dfrac{64}{16}=4\left(mol\right)\)
=> CTHH: CuSO4
b)
\(m_N=\dfrac{82,35.17}{100}=14\left(g\right)=>n_N=\dfrac{14}{14}=1\left(mol\right)\)
\(m_H=\dfrac{17,65.17}{100}=3\left(g\right)=>n_H=\dfrac{3}{1}=3\left(mol\right)\)
=> CTHH: NH3
c)
\(m_{Na}=\dfrac{32,39.142}{100}=46\left(g\right)=>n_{Na}=\dfrac{46}{23}=2\left(mol\right)\)
\(m_S=\dfrac{22,53.142}{100}=32\left(g\right)=>n_S=\dfrac{32}{32}=1\left(mol\right)\)
\(m_O=142-46-32=64\left(g\right)=>n_O=\dfrac{64}{16}=4\left(mol\right)\)
=> CTHH: Na2SO4
d)
\(m_{Fe}=\dfrac{36,8.152}{100}=56\left(g\right)=>n_{Fe}=\dfrac{56}{56}=1\left(mol\right)\)
\(m_S=\dfrac{21.152}{100}=32\left(g\right)=>n_S=\dfrac{32}{32}=1\left(mol\right)\)
\(m_O=152-56-32=64\left(g\right)=>n_O=\dfrac{64}{16}=4\left(mol\right)\)
=> CTHH: FeSO4
Đúng 1
Bình luận (0)
Đốt cháy 1 hợp chất A cần vừa đủ 8,96 lít O2, sau phản ứng thu được 4,48 lít khí CO2 và 7,2 gam H2O. biết A có tỉ khối hơi so với He= 4, các thể tích khí đo ở đktc
a, Tính khối lượng A phản ứng
b, tính CTPT của A
a)
nO2=8.96/22,4=0.4 mol
---->mO2=0.4*32=12.8g
nCO2=4.48/22.4=0.2 mol
---->mCO2=0.2*44=8.8g
Áp dụng định luật bảo toàn khối lượng:
mA+mO2=mCO2+mH2O
---->mA=mCO2+mH2O-mO2=8.8+7.2-12.8=3.2g
b) Gọi CTPT của A là CxHy
4CxHy + (4x+y)O2-----> 4xCO2 + 2yH2O
Ta có:
dMA/MHe=(12x+y)/4=4
---->MA=12x+y=16(1)
nCxHy=1/x*nCO2=0.2/x=3.2/16=0.2mol(2)
-----> x=1 ; y=4
Vậy CTPT của A là CH4
Đúng 0
Bình luận (0)
9/ Lập CTHH của các hợp chất:
a) A gồm 40% Cu; 20% S; 40% O biết khối lượng mol của A là 160
b) B gồm 82,35% N và 17,65% H, biết khối lượng mol của B là 17
a, viết cthh có dạng \(Cu_xS_yO_z\)
\(m_{Cu}=\dfrac{40.160}{100}=64\)
-> \(n_{Cu}=\dfrac{64}{64}=1=>x=1\)
\(m_S=\dfrac{20.160}{100}=32\)
\(n_S=\dfrac{32}{32}=1=>y=1\)
\(m_O=\dfrac{40.160}{100}=32\)
\(->n_O=\dfrac{32}{16}=2=>z=2\)
=> cthh: \(CuSO_2\)
Đúng 0
Bình luận (1)
b, viết CTHH có dạng \(N_xH_y\)
\(m_N=\dfrac{82,35.17}{100}=14\)
-> \(n_N=\dfrac{14}{14}=1=>x=1\)
\(m_H=\dfrac{17,65.17}{100}=3\)
\(->n_H=\dfrac{3}{1}=3=>y=3\)
=> CTHH: \(CH_3\)
Đúng 0
Bình luận (0)
Hòa tan 115,3 gam hổn hợp X gồm MgCO3 và RCO3 bằng dung dịch H2SO4 loảng thu được dung dịch A, chất rắn B và 4,48 lít khí (ở đktc). Cô cạn dung dịch A thu được 12 gam muối khan. Mặt khác đem nung chất rắn B tới khối lượng không đổi thu được 11,2 lít khí CO2 (ở đktc) và chất rắn B1. Khối lượng của B1 là A. 110,3 gam B. 88,5 gam C. 83,8 gam D. 101,3 gam
Đọc tiếp
Hòa tan 115,3 gam hổn hợp X gồm MgCO3 và RCO3 bằng dung dịch H2SO4 loảng thu được dung dịch A, chất rắn B và 4,48 lít khí (ở đktc). Cô cạn dung dịch A thu được 12 gam muối khan. Mặt khác đem nung chất rắn B tới khối lượng không đổi thu được 11,2 lít khí CO2 (ở đktc) và chất rắn B1. Khối lượng của B1 là
A. 110,3 gam
B. 88,5 gam
C. 83,8 gam
D. 101,3 gam
1.Cho hỗn hợp X gồm 2 chất hữu cơ có cùng CTPT C2H7NO2 tác dụng vừa đủ với dung dịch NaOH, đun nóng thu được dung dịch Y và 4,48 lít (đktc) hỗn hợp Z gồm 2 khí (đều làm xanh quỳ tím ẩm). Tỉ khối của Z đối với hiđro bằng 13,75. Cô cạn dung dịch Y thu được khối lượng muối khan là: A. 16,5 gam. B. 14,3 gam. C. 8,9 gam. D. 15,7 gam.
Đọc tiếp
1.Cho hỗn hợp X gồm 2 chất hữu cơ có cùng CTPT C2H7NO2 tác dụng vừa đủ với dung dịch NaOH, đun nóng thu được dung dịch Y và 4,48 lít (đktc) hỗn hợp Z gồm 2 khí (đều làm xanh quỳ tím ẩm). Tỉ khối của Z đối với hiđro bằng 13,75. Cô cạn dung dịch Y thu được khối lượng muối khan là:
A. 16,5 gam.
B. 14,3 gam.
C. 8,9 gam. D. 15,7 gam.
M tb hh = 27,5 => hỗn hợp có NH3 , vì hh X có 2 chất HC pư với NaOH tạo khí có 2C => khí còn lại là CH3NH2 => X có CH3COONH4 và HCOOCH3NH3 . Pư :
CH3COONH4 + NaOH ---------> CH3COONa + NH3 + H2O
a a a
HCOOCH3NH3 + NaOH -------> HCOONa + CH3NH2 + H2O
b b b
ta có n hh = a + b = 0,2 mol
m hh = Mtb.n = 5,5 = 17a + 31b
từ hệ => a = 0,05 , b = 0,15 mol => m muối khan = 0,05.82 + 0,15 . 68 = 14,3g => B
Đúng 0
Bình luận (0)
bài 1: hợp chất A có tỉ khối so với H2 là 22. Hãy cho biết 5,6 lít khí A ở(đktc) có khối lượng là bao nhiêu gam?bài 2: tìm công thữ hóa học của những hợp chất có thành phần nguyên tố như sau:a) hợp chất A tạo bởi 2 nguyên tố: C và O có khối lượng mol là 44(g?mol),trong đó cacbon chiếm 27,3% về khối lượng,còn lại là % Ob) hợp chất B tạo bởi 3 nguyên tố: Na,C,O có khối lượng mol là 44(g/mol), thành phần các nguyên tố lần lượt là: 43,4% Na,11,3% C,45,3%c) một hợp chất khí A có thành phần % theo khố...
Đọc tiếp
bài 1: hợp chất A có tỉ khối so với H2 là 22. Hãy cho biết 5,6 lít khí A ở(đktc) có khối lượng là bao nhiêu gam?
bài 2: tìm công thữ hóa học của những hợp chất có thành phần nguyên tố như sau:
a) hợp chất A tạo bởi 2 nguyên tố: C và O có khối lượng mol là 44(g?mol),trong đó cacbon chiếm 27,3% về khối lượng,còn lại là % O
b) hợp chất B tạo bởi 3 nguyên tố: Na,C,O có khối lượng mol là 44(g/mol), thành phần các nguyên tố lần lượt là: 43,4% Na,11,3% C,45,3%
c) một hợp chất khí A có thành phần % theo khối lượng: 82,35% N,17,65% H. Hợp chất A có tỉ khối với H2 là 8,5. Hãy cho biết:
- CTHH của hợp chất A
- số mol nguyên tử của các nguyên tố có trong 0,5 mol hợp chất A.
bài1
ta có dA/H2=22 →MA=22MH2=22 \(\times\) 2 =44
nA=\(\frac{5,6}{22,4}\)=0,25
\(\Rightarrow\)mA=M\(\times\)n=11 g
Đúng 0
Bình luận (0)
MA=dA/\(H_2\)×M\(H_2\)=22×(1×2)=44g/mol
nA=VA÷22,4=5,6÷22,4=0,25mol
mA=nA×MA=0,25×44=11g
Đúng 0
Bình luận (0)
a)
MC=27,3×44÷100\(\approx\)12g/mol
% mO=100-27,3=72,7%
MO=72,7×44÷100\(\approx\)32g/mol
Công thức hóa học chung: CaxOy
Theo công thức hóa học có:
x×\(III\)=y×\(IV\)
Lập tỉ lệ: \(\dfrac{x}{y}=\dfrac{II}{IV}=\dfrac{2}{4}=\dfrac{1}{2}\)
=>x=1 và y=2
Công thức hóa học của hợp chất: CO\(_2\)
Đúng 0
Bình luận (0)
Cho mik hỏi nha.Có 3 câu: C1: một hợp chất khí A có 82,35% N và 17,65% H. Hãy cho biết CTHH của hợp chất A biết hợp chất này có tỉ khối đối với khí hidro là 8,5C2: một hợp chất khí được tạo bởi 2 nguyên tố H và C trong đó C chiếm 75% về khối lượng, biết 4,48 lít hợp chất( ở điều kiện tiêu chuẩn) có khôid lượng là 3,2gam. Xác định CTHH của hợp chất khí trênC3: một hợp chất khí có CTHH là M2O. Biết tỉ khối hơi của nó đối với H2 là 22. Tìm nguyên tố MCác bạn trả lời giúp mik nha !Cảm ơn !
Đọc tiếp
Cho mik hỏi nha.
Có 3 câu:
C1: một hợp chất khí A có 82,35% N và 17,65% H. Hãy cho biết CTHH của hợp chất A biết hợp chất này có tỉ khối đối với khí hidro là 8,5
C2: một hợp chất khí được tạo bởi 2 nguyên tố H và C trong đó C chiếm 75% về khối lượng, biết 4,48 lít hợp chất( ở điều kiện tiêu chuẩn) có khôid lượng là 3,2gam. Xác định CTHH của hợp chất khí trên
C3: một hợp chất khí có CTHH là M2O. Biết tỉ khối hơi của nó đối với H2 là 22. Tìm nguyên tố M
Các bạn trả lời giúp mik nha !
Cảm ơn !
câu 1
gọi CT NxHy
ta có
x: y = \(\frac{82,35}{14}:\frac{17,65}{1}\) = 1: 3
=> NH3
Đúng 0
Bình luận (0)
câu 2
gọi CT CxHy
ta có nCxHy = 4,48/22,4 = 0,2 => MCxHy = \(\frac{3,2}{0,2}\) = 16
ta có x = \(\frac{16.75\%}{12}=1\)
=> y = \(\frac{16-12}{1}\) = 4
=> CH4
Đúng 0
Bình luận (0)
câu 3
MM2O = 22.2 = 44
ta có 2M + 16 = 44 => M = 14 => Nito
=> CTHH : N2O
Đúng 0
Bình luận (0)