cho 8,3 g hỗn hợp nhôm , sắt tác dụng với HCl dư thu được 5,6 lít H2 (đktc) . tìm thành phần % về khối lượng của 2 kim loại

Những câu hỏi liên quan
Cho 8,3 g hỗn hợp gồm nhôm và sắt tác dụng với dung dịch
H
2
SO
4
loãng dư. Sau PƯ thu được 5,6 lít khí đo ở đktc. Tính thành phần phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp đầu. A. 32% và 68% B. 40% và 60% C. 32,5% và 67,5% D. 30% và 70%
Đọc tiếp
Cho 8,3 g hỗn hợp gồm nhôm và sắt tác dụng với dung dịch H 2 SO 4 loãng dư. Sau PƯ thu được 5,6 lít khí đo ở đktc. Tính thành phần phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp đầu.
A. 32% và 68%
B. 40% và 60%
C. 32,5% và 67,5%
D. 30% và 70%
Đáp án C
Gọi a, b là số mol của Al và Fe trong 8,3 g hỗn hợp ban đầu

Đúng 0
Bình luận (0)
Cho 8,3 g hỗn hợp gồm nhôm và sắt tác dụng vừa đủ với dung dịch HCl loãng, sau phản ứng thu được 5,6 lít khí (đktc).
a) Viết các phương trình hóa học.
b) Tính thành phần phần trăm theo khối lượng của mỗi kim loại ban đầu.
c) Tính khối lượng muối thu được sau phản ứng.
\(\text{Đặt }\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\\ n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\\ a,PTHH:\left\{{}\begin{matrix}2Al+6HCl\rightarrow2AlCl_3+3H_2\\Fe+2HCl\rightarrow FeCl_2+H_2\end{matrix}\right.\\ b,\text{Theo đề ta có HPT: }\left\{{}\begin{matrix}27x+56y=8,3\\\dfrac{3}{2}x+y=0,25\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,1\left(mol\right)\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}\%_{Al}=\dfrac{0,1\cdot27}{8,3}\approx32,53\%\\\%_{Fe}\approx67,47\%\end{matrix}\right.\)
\(c,\left\{{}\begin{matrix}n_{AlCl_3}=0,1\left(mol\right)\\n_{FeCl_2}=0,1\left(mol\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}m_{AlCl_3}=0,1\cdot133,5=13,35\left(g\right)\\m_{FeCl_2}=0,1\cdot127=12,7\left(g\right)\end{matrix}\right.\\ \Rightarrow\sum m_{muối}=13,35+12,7=26,05\left(g\right)\)
Đúng 2
Bình luận (1)
Cho 8,3 gam hỗn hợp các kim loại sắt và nhôm tác dụng với dung dịch HCl dư. Sau phản ứng kết thúc, người ta thu được 5,6 lít khí ở (đktc).
a. Viết phương trình hóa học xảy ra ? Tính thành phần phần trăm theo khối lượng của mỗi kim loại có trong hỗn hợp.
\(n_{H_2}=\dfrac{5,6}{22,4}=0,25(mol)\\ a,PTHH:Fe+2HCl\to FeCl_2+H_2\\ 2Al+6HCl\to 2AlCl_3+3H_2\)
\(b,\) Đặt \(n_{Fe}=x(mol);n_{Al}=y(mol)\)
\(\Rightarrow 56x+27y=8,3(1)\)
Theo PTHH: \(x+1,5y=0,25(2)\)
\((1)(2)\Rightarrow x=y=0,1(mol)\\ \Rightarrow \%_{Fe}=\dfrac{0,1.56}{8,3}.100\%=67,47\%\\ \%_{Al}=100\%-67,47\%=32,53\%\)
Đúng 1
Bình luận (0)
Cho hỗn hợp gồm bột nhôm và oxit sắt. Thực hiện hoàn toàn phản ứng nhiệt nhôm (giả sử chỉ có phản ứng oxit sắt thành Fe) thu được hỗn hợp chất rắn B có khối lượng 19,82 g. Chia hỗn hợp thành 2 phần bằng nhau: - Phần 1: cho tác dụng với một lượng dư dung dịch NaOH thu được 1,68 lít khí H2 (đktc). - Phần 2: cho tác dụng với một lượng dư dung dịch HCl thì có 3,472 lít khí H2 (đktc) thoát ra. Công thức của oxit sắt là A. Fe2O3. B. Fe3O4. C. FeO. D. Không xác định được.
Đọc tiếp
Cho hỗn hợp gồm bột nhôm và oxit sắt. Thực hiện hoàn toàn phản ứng nhiệt nhôm (giả sử chỉ có phản ứng oxit sắt thành Fe) thu được hỗn hợp chất rắn B có khối lượng 19,82 g. Chia hỗn hợp thành 2 phần bằng nhau:
- Phần 1: cho tác dụng với một lượng dư dung dịch NaOH thu được 1,68 lít khí H2 (đktc).
- Phần 2: cho tác dụng với một lượng dư dung dịch HCl thì có 3,472 lít khí H2 (đktc) thoát ra.
Công thức của oxit sắt là
A. Fe2O3.
B. Fe3O4.
C. FeO.
D. Không xác định được.
Đáp án A
Ta có sơ đồ phản ứng:
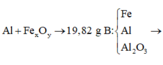
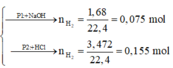
Phần 1:
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑
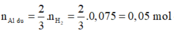
![]()
Phần 2:
2Al + 6HCl → 2AlCl3 + 3H2↑ (1)
0,05 → 0,075
Fe + 2HCl → FeCl2 + H2↑ (2)
![]()
![]()
![]()
![]()
Ta có phương trình phản ứng:
![]()
Khối lượng các chất trong 1 phần hỗn hợp B là 19,82/2 = 9,91 g
![]()
![]()
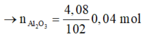
Ta có:
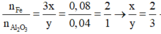
=> Oxit sắt cần tìm là Fe2O3
Đúng 0
Bình luận (0)
Cho hỗn hợp gồm bột nhôm và oxit sắt. Thực hiện hoàn toàn phản ứng nhiệt nhôm (giả sử chỉ có phản ứng oxit sắt thành Fe) thu được hỗn hợp chất rắn B có khối lượng 19,82 g. Chia hỗn hợp thành 2 phần bằng nhau: - Phần 1: cho tác dụng với một lượng dư dung dịch NaOH thu được 1,68 lít khí H2 (đktc). - Phần 2: cho tác dụng với một lượng dư dung dịch HCl thì có 3,472 lít khí H2 (đktc) thoát ra. Công thức của oxit sắt là A. Fe2O3. B. Fe3O4. C. FeO. D. Không xác định được.
Đọc tiếp
Cho hỗn hợp gồm bột nhôm và oxit sắt. Thực hiện hoàn toàn phản ứng nhiệt nhôm (giả sử chỉ có phản ứng oxit sắt thành Fe) thu được hỗn hợp chất rắn B có khối lượng 19,82 g. Chia hỗn hợp thành 2 phần bằng nhau:
- Phần 1: cho tác dụng với một lượng dư dung dịch NaOH thu được 1,68 lít khí H2 (đktc).
- Phần 2: cho tác dụng với một lượng dư dung dịch HCl thì có 3,472 lít khí H2 (đktc) thoát ra.
Công thức của oxit sắt là
A. Fe2O3.
B. Fe3O4.
C. FeO.
D. Không xác định được.
Cho 0,83g hỗn hợp gồm nhôm và sắt tác dụng với dung dịch
H
2
S
O
4
loãng dư, người ta thu được 0,56 lít khí (đktc). Tính thành phần phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp đầu. A. 32,5% và 65,7% B. 65,7% và 32,5% C. 67,5% và 32,5% D. 32,5% và 67,5%
Đọc tiếp
Cho 0,83g hỗn hợp gồm nhôm và sắt tác dụng với dung dịch H 2 S O 4 loãng dư, người ta thu được 0,56 lít khí (đktc). Tính thành phần phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp đầu.
A. 32,5% và 65,7%
B. 65,7% và 32,5%
C. 67,5% và 32,5%
D. 32,5% và 67,5%
2 A l + 3 H 2 S O 4 → A l 2 S O 4 3 + 3 H 2
x 3/2 x mol
F e + H 2 S O 4 → F e S O 4 + H 2
y y mol
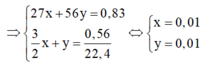
⇒ % m A l = 0,01.27 0,83 .100 = 32,53 % ⇒ % m F e = 100 % − 32,53 % = 67,47 %
⇒ Chọn D.
Đúng 0
Bình luận (0)
Bài 5: Cho 8,3 gam hỗn hợp kim loại Fe và Al tác dụng với HCl dư thu được 5,6 l khí H2 (đktc). Tính thành phần % khối lượng của từng kim loại trong hỗn hợp.
Gọi số mol Fe là x; Al là y(x,y>0)
Ta có khối lượng hỗn hợp: 56x+27y=8,3 g(I)
Cho hỗn hợp tác dụng với HCl ta được:
PTHH: Fe + 2HCl-> FeCl2 + H2
TPT : 1 1
TĐB: x -> x(1)
PTHH: 2Al + 6HCl-> 2AlCl3 + 3H2
TPT : 2 3
TĐB : y -> \(\dfrac{3y}{2}\)(2)
Từ (1) và (2)=)x + \(\dfrac{3y}{2}\)= \(\dfrac{5,6}{22,4}\left(II\right)\)
Từ (I) và (II) giải hệ ta được:
\(\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}m_{Fe}=0,1.56=5,6\left(g\right)\\m_{Al}=0,1.27=2,7\left(g\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{5,6}{8,3}.100\%\approx67,47\%\\\%m_{Al}=100\%-67,47\%=32,53\%\end{matrix}\right.\)
Tích cho mk nha cảm ơn mọi người
Đúng 1
Bình luận (4)
Cho 13,8 gam hỗn hợp X gồm kim loại kiềm R và Ca tác dụng hết với nước thu được 5,6 lít H2 (đktc) và dung dịch Y. Mặt khác, cho 8,58 gam kim loại R phản ứng hết với lượng dư dung dịch HCl thì thể tích khí H2 thoát ra lớn hơn 2,24 lít (đktc). 1. Tìm kim loại R? 2. Cho 15 lít hỗn hợp khí Z gồm N2 và CO2 (đktc) vào dung dịch Y. Sau khi phản ứng kết thúc thu được 8,5 gam kết tủa. Tính thành phần phần trăm về thể tích của mỗi khí trong hỗn hợp Z?
Đọc tiếp
Cho 13,8 gam hỗn hợp X gồm kim loại kiềm R và Ca tác dụng hết với nước thu được 5,6 lít H2 (đktc) và dung dịch Y. Mặt khác, cho 8,58 gam kim loại R phản ứng hết với lượng dư dung dịch HCl thì thể tích khí H2 thoát ra lớn hơn 2,24 lít (đktc).
1. Tìm kim loại R?
2. Cho 15 lít hỗn hợp khí Z gồm N2 và CO2 (đktc) vào dung dịch Y. Sau khi phản ứng kết thúc thu được 8,5 gam kết tủa. Tính thành phần phần trăm về thể tích của mỗi khí trong hỗn hợp Z?
1.
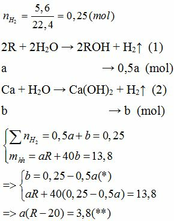
Vì b > 0, từ (*) => a < 0,25/0,5 = 0,5 thế vào (**)
=> R – 20 > 7,6
=> R > 27,6 (***)
Khi cho 8,58 gam R tác dụng với lượng dư HCl thì lượng H2 thoát ra lớn hơn 2,24 (lít)
2R + 2HCl → 2RCl + H2↑ (3)
Theo PTHH (3):
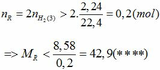
Từ (***) và (****) => 27, 6 < MR < 42,9
Vậy MR = 39 (K) thỏa mãn
2.
Ta có:
=> nKOH = nK = 0,2 (mol)
nCa(OH)2 = nCa = 0,15 (mol)
∑ nOH- = nKOH + 2nCa(OH)2 = 0,2 + 2.0,15 = 0,5 (mol)
Khi cho hỗn hợp Z ( N2, CO2) vào hỗn hợp Y chỉ có CO2 phản ứng
CO2 + OH- → HCO3- (3)
CO2 + 2OH- → CO32- + H2O (4)
CO32- + Ca2+ → CaCO3↓ (5)
nCaCO3 = 8,5/100 = 0,085 (mol) => nCO32-(5) = nCaCO3 = 0,085 (mol)
Ta thấy nCaCO3 < nCa2+ => phương trình (5) Ca2+ dư, CO32- phản ứng hết
TH1: CO2 tác dụng với OH- chỉ xảy ra phản ứng (4)
Theo (4) => nCO2 = nCO32-(4) = nCaCO3 = 0,085 (mol)
=> VCO2(đktc) = 0,085.22,4 = 1,904 (lít)
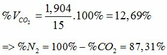
TH2: CO2 tác dụng với OH- xảy ra cả phương trình (3) và (4)
Theo (4): nCO2 = nCO32- = 0,085 (mol)
nOH- (4) = 2nCO32- = 2. 0,085 = 0,17 (mol)
=> nOH- (3)= ∑ nOH- - nOH-(4) = 0,5 – 0,17 = 0,33 (mol)
Theo PTHH (3): nCO2(3) = nOH- = 0,33 (mol)
=> ∑ nCO2(3+4) = 0,085 + 0,33 = 0,415 (mol)
=> VCO2 (ĐKTC) = 0,415.22,4 = 9,296 (lít)
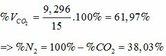
Đúng 0
Bình luận (0)
Cho 5,5g hỗn hợp 2 kim loại Nhôm và Sắt tác dụng với dung dịch axít HCl dư thu được 4,48 lít khí H2(đktc)
1.Viết PT phản ứng xảy ra
2.TÍnh thành phần, phần trăm khối lượng mỗi kim loại trong hỗn hợp ban đầu
3. Dẫn toàn bộ khí thu được ở trên qua ống sứ nung nóng có chứa 8g CuO.Tính khối lượng kim loại thu được
1)2 Al +6HCl--->2AlCl3 +3H2
Fe +2 HCl --->FeCl2 +H2
2) đặt nAl=x,nFe=y =>từ phương trình ở ý 1) và theo bài ra ta có;3/2.x+y=4.48/22.4 và 27x+56y=5.5.giải hệ hai phương trình=>x=0.1 và y=0.05=>mAl=27.0.1=2.7(gam)=>% về khối lượng của Al trong hỗn hợp=(2.7/5.5).100%=49.1%=>%về khối lượng của Fe trong hỗn hợp=100%-49.1%=50.9%.
3) pt : CuO + H2----> Cu +H2O.ta có nH2=0.2(mol),nCuO=0.1(mol)=>CuO pư hết và H2 dư=> nCu=nCuO=>mCuO=0.1 nhân 64=6.4 (gam).
Đúng 0
Bình luận (0)