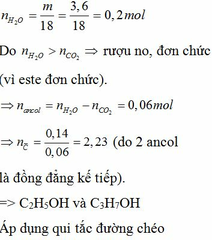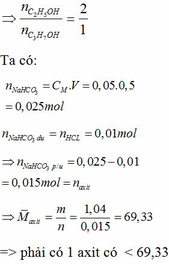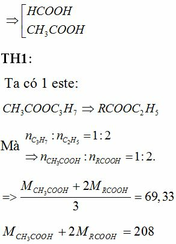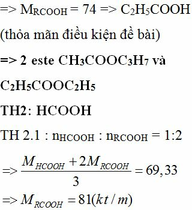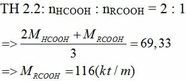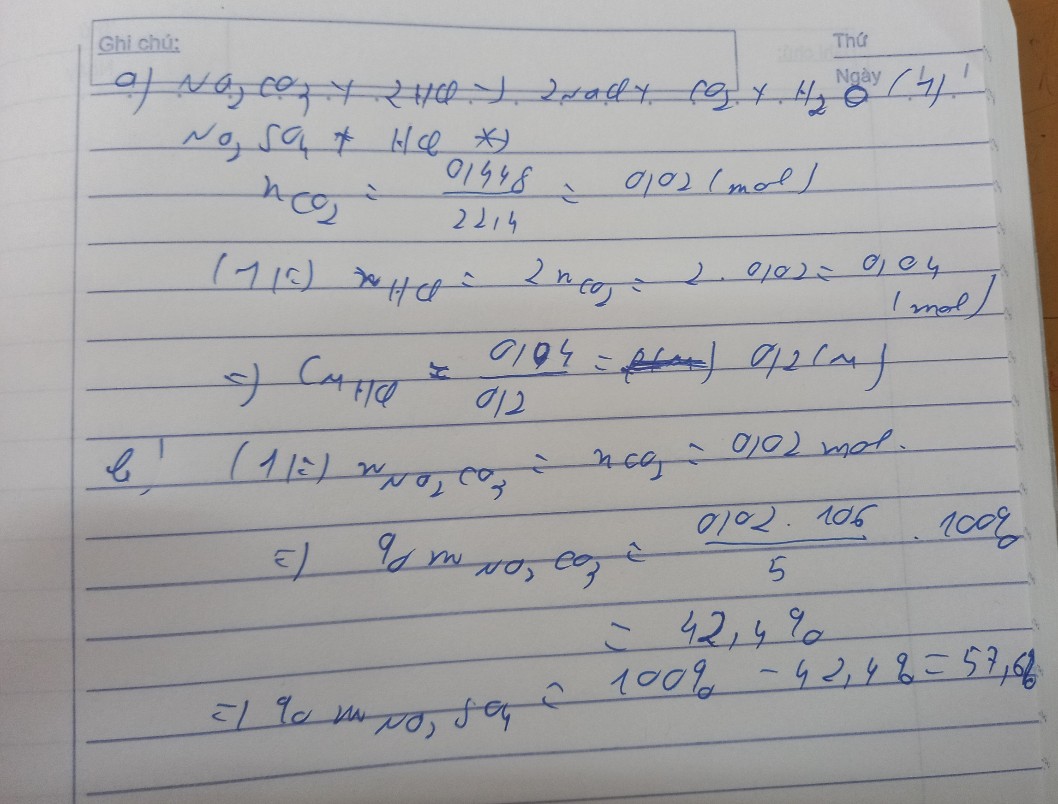Thổi 2,464 lit khí CO2 vào một dd NAOH thì được 9,46g hỗn hợp 2 muối Na2CO3 và NaHCO3. Hãy xác định thành phần khối lượng của hỗn hợp 2 muối đó. Nếu muốn chỉ thu được muối NaCO3 thì cần thêm bao nhiêu lit khí cacbonic nữa.

Những câu hỏi liên quan
Thổi 2,464 lít khí C
O
2
vào một dung dịch NaOH thì được 9,46 gam hỗn hợp 2 muối
N
a
2
C
O
3
và NaHC
O
3
. Nếu muốn chỉ thu được muối NaHC
O
3
thì cần thêm bao nhiêu lít khí cacbonic nữa? A. 0,336 lít B. 0,112 lít C. 0,448 lít D. 0,224 lít
Đọc tiếp
Thổi 2,464 lít khí C O 2 vào một dung dịch NaOH thì được 9,46 gam hỗn hợp 2 muối N a 2 C O 3 và NaHC O 3 . Nếu muốn chỉ thu được muối NaHC O 3 thì cần thêm bao nhiêu lít khí cacbonic nữa?
A. 0,336 lít
B. 0,112 lít
C. 0,448 lít
D. 0,224 lít
Chọn D
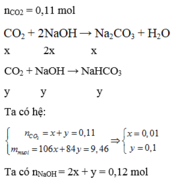
Để thu được NaHC O 3 thì chỉ xảy ra phản ứng:
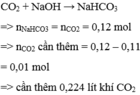
Đúng 0
Bình luận (1)
Thổi 2,464 lit khí CO\(_2\) vào một dd NaOH thì được 9,46g hỗn hợp 2 muối Na\(_2\)CO\(_3\) và NaHCO\(_3\). Hãy xác định thành phần khối lượng của hỗn hợp 2 muối đó. Nếu muốn chỉ thu được muối NaCO\(_3\) thì cần thêm bao nhiêu lit khí cacbonic nữa.
Hòa tan hoàn toàn 9,1gam hỗn hợp Na2CO3 và NaHCO3 trong dung dịch H2SO4 50% thì thu được 2,016l khí ở đktc. Xác định % khối lượng muối trong hỗn hợp và khối lượng dung dịch axit cần dùng
\(n_{Na_2CO_3} = a(mol) ; n_{NaHCO_3} = b(mol)\\ \Rightarrow 106a + 84b = 9,1(1)\\ Na_2CO_3 + H_2SO_4 \to Na_2SO_4 +C O_2 + H_2O\\ 2NaHCO_3 + H_2SO_4 \to Na_2SO_4 + 2CO_2 + 2H_2O\\ n_{CO_2} =a + b = \dfrac{2,016}{22,4} = 0,09(2)\\ (1)(2) \Rightarrow a = 0,07 ; b= 0,02\\ \%m_{Na_2CO_3} = \dfrac{0,07.106}{9,1}.100\%= 81,54\%\\ \%m_{NaHCO_3} = 100\% - 81,54\% = 18,76\%\\ n_{H_2SO_4} = a + 0,5b = 0,08(mol)\\ m_{dd\ H_2SO_4} = \dfrac{0,08.98}{50\%} = 15,68(gam)\)
Đúng 2
Bình luận (0)
- Gọi số mol Na2CO3 và NaHCO3 là a, b mol
PTKL : 106a + 84b = 9,1
BTC : a + b = 0,09
=> a = 0,07mol, b = 0,02mol .
=> mNa2CO3 = 7,42g ( 81,54% ), mNaHCO3 = 1,68g ( 18,46% )
BTH => nH2SO4 = 0,08 mol
=> mdd = 15,68g
Đúng 0
Bình luận (0)
Đun nóng hỗn hợp hai este đơn chức với dd NaOH vừa đủ thu được hỗn hợp 2 rượu đồng đẳng kế tiếp và hỗn hợp 2 muối. Đốt cháy hoàn toàn một lượng hỗn hợp rượu trên thu được 3,136 lít khí CO2 (đktc) và 3,6 gam H2O. Cho hỗn hợp hai muối trên tác dụng với dd H2SO4 vừa đủ được hỗn hợp hai axit cacboxylic. Cho từ từ 50ml dd NaHCO3 0,5M vào cốc đựng 1,04 gam hỗn hợp hai axit thu được ở trên, sau phản ứng cần phải dùng 10ml dd HCl 1M mới tác dụng vừa hết với lượng NaHCO3 dư. Xác định công thức cấu tạo củ...
Đọc tiếp
Đun nóng hỗn hợp hai este đơn chức với dd NaOH vừa đủ thu được hỗn hợp 2 rượu đồng đẳng kế tiếp và hỗn hợp 2 muối. Đốt cháy hoàn toàn một lượng hỗn hợp rượu trên thu được 3,136 lít khí CO2 (đktc) và 3,6 gam H2O. Cho hỗn hợp hai muối trên tác dụng với dd H2SO4 vừa đủ được hỗn hợp hai axit cacboxylic. Cho từ từ 50ml dd NaHCO3 0,5M vào cốc đựng 1,04 gam hỗn hợp hai axit thu được ở trên, sau phản ứng cần phải dùng 10ml dd HCl 1M mới tác dụng vừa hết với lượng NaHCO3 dư. Xác định công thức cấu tạo của hai este có trong hỗn hợp đầu. Biết khi đốt cháy 1 mol mỗi este thu được không quá 5mol CO2.
Hòa tan hoàn toàn hỗn hợp na2co3 và k2co3 bằng 400ml dd hcl 1,5M thu được 5,6l khí co2 (đktc) và một dd A. trung hòa axit còn dư tronh dd A bằng lượng dd naoh vừa đủ thu được dd B, rồi cô cạn dd B sau pứ được 39,9g hỗn hợp muối khan. tính thành phần % về khối lượng các muối cacbonat trong hỗn hợp đầu.
Có một hỗn hợp ba muối
N
H
4
H
C
O
3
,
N
a
H
C
O
3
,
C
a
(
H
C
O
3
)
2
. Khi nung 48,8 g hỗn hợp đó đến khối lượng không đổi, thu được 16,2 g bã rắn....
Đọc tiếp
Có một hỗn hợp ba muối N H 4 H C O 3 , N a H C O 3 , C a ( H C O 3 ) 2 . Khi nung 48,8 g hỗn hợp đó đến khối lượng không đổi, thu được 16,2 g bã rắn. Chế hoá bã rắn với dung dịch HCl lấy dư, thu được 2,24 lít khí (đktc).
Xác định thành phần phần trăm của các muối trong hỗn hợp.
Các phản ứng phân hủy muối khi nung :
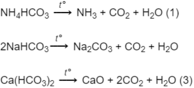
Bã rắn thu được sau khi nung gồm N a 2 C O 3 và CaO, chúng tan trong dung dịch HCl dư theo các phương trình hoá học :
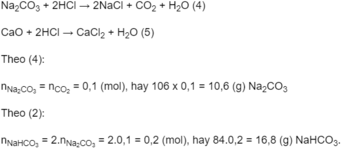
Số mol CaO có trong bã rắn: 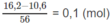
Theo (3):
![]()
Khối lượng N H 4 H C O 3 có trong hỗn hợp: 48,8 - (16,8 + 16,2) = 15,8 (g).
Thành phần phần trăm của hỗn hợp muối:
%
m
N
H
4
H
C
O
3
= 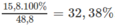
%
m
N
a
H
C
O
3
= 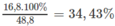
%
m
C
a
(
H
C
O
3
)
2
= 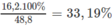
Đúng 0
Bình luận (0)
Hỗn hợp X gồm 2 muối Na2CO3 và K2CO3 có khối lượng 35 gam. Khi thêm từ từ và khuấy đều 0,8 lít dd HCl 0,5M?vào dd chứa 2 muối trên thì có 2,24 lít CO2 thoát ra ở dkc và được dd Y. Thêm Ca(OH)2 dư vào dd Y ta thu được kết tủa A. Tính khối lượng mỗi muối trong hỗn hợp X và tính khối lượng kết tủa A.
Gọi số mol 2 muối trên lần lượt là a, b. Ta có:
- Số mol ion CO3(2-) là a+b
Số mol ion H+ =số mol HCl = 0,4. Do thêm từ từ HCl vào dd muối nên:
H+ + CO3(2-) -------> HCO3(-) (1)
Vì có khí thoát ra nên xảy ra phản ứng 2 => CO3(2-) hết
H+ + HCO3(-) -------> CO2 + H2O (2)
Do
Do dd Y tạo kết tủa với Ca(OH)2 nên dd Y có chứa ion HCO3- => sau (2) H+ hết, HCO3- dư => mol H+ (2) = mol CO2 =0,1 => mol H+(1)=a+b=0,4 - 0,1 = 0,3
Giải hệ: a+b = 0,3
106a + 138b = 35
ta được a = 0,2 b = 0,1 => khối lượng mỗi muối ^-^
- dd Y chứa 0,3 - 0,1 = 0,2 mol ion HCO3-
HCO3- + OH- ------> CO3(2-) + H2O
Ca2+ + CO3(2-) -----> CaCO3
Mol CaCO3 = mol CO3(2-) = mol HCO3- =0,2 => Khối lượng kết tủa
Đúng 1
Bình luận (2)
https://i.imgur.com/xaNka0a.jpg
Cho 15,2 g hỗn hợp 2 muối NaCl và Na2CO3 tác dụng hết với 150 ml dung dịch h2SO4 . Thu được 1,8 lít khí đktc A/ xác định thành phần phần trăm và khối lượng của mỗi muối có trong hỗn hợp đầu
Hỗn hợp X gồm 2 muối Na2CO3 và K2CO3 có khối lượng 35 gam. Khi thêm từ từ và khuấy đều 0,8 lít dd HCl 0,5M?
vào dd chứa 2 muối trên thì có 2,24 lít CO2 thoát ra ở dkc và được dd Y. Thêm Ca(OH)2 dư vào dd Y ta thu được kết tủa A. Tính khối lượng mỗi muối trong hỗn hợp X và tính khối lượng kết tủa A Gọi số mol 2 muối trên lần lượt là a, b. Ta có:
- Số mol ion CO3(2-) là a+b
Số mol ion H+ =số mol HCl = 0,4. Do thêm từ từ HCl vào dd muối nên:
H+ + CO3(2-) -------> HCO3(-) (1)
Vì có khí thoát ra nên xảy ra phản ứng 2 => CO3(2-) hết
H+ + HCO3(-) -------> CO2 + H2O (2)
Do
Do dd Y tạo kết tủa với Ca(OH)2 nên dd Y có chứa ion HCO3- => sau (2) H+ hết, HCO3- dư => mol H+ (2) = mol CO2 =0,1 => mol H+(1)=a+b=0,4 - 0,1 = 0,3
Giải hệ: a+b = 0,3
106a + 138b = 35
ta được a = 0,2 b = 0,1 => khối lượng mỗi muối ^-^
- dd Y chứa 0,3 - 0,1 = 0,2 mol ion HCO3-
HCO3- + OH- ------> CO3(2-) + H2O
Ca2+ + CO3(2-) -----> CaCO3
Mol CaCO3 = mol CO3(2-) = mol HCO3- =0,2 => Khối lượng kết tủa^-^
Đúng 0
Bình luận (0)