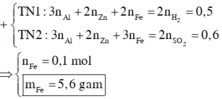Mình cần gấp lắm mong mn giúp đỡ
Cho m g hỗn hợp X gồm Fe, Mg và Ag vào dd H2SO4 loãng thu được 4,48l H2 (đktc). Mặt khác nếu hòa tan hoàn toàn m g hỗn hoepj X trên vào dd H2SO4 đặc nóng thì thu được 6,72l SO2 (đktc)
a) viết pt phản ứng
b) Tính khối lượng của từng KL trong hỗn hợp trên biết số mol Mg = số mol Ag