z là hợp chất gồm 2 ng tố, trong đó có 1 chất là kali và còn lại là phi kim x trong đó %mk =52,35%.xác định cthh biết z là muối.

Những câu hỏi liên quan
Cho sơ đồ chuyển hóa sau: a) Xác định các chất X, Y, Z, A, B, D, E, F biết rằng: - X là đơn chất của phi kim T, còn Y, Z là hợp chất hai nguyên tố, trong đó có chứa T. Dung dịch của Y làm quỳ tím chuyển đỏ. Z là muối Kali trong đó Kali chiếm 52,35% về khối lượng. - Từ D có thể tạo thành A bằng phản ứng với oxi xúc tác men giấm. b) Viết các phương trình phản ứng hóa học xảy ra ( ghi rõ điều kiện nếu có).
Đọc tiếp
Cho sơ đồ chuyển hóa sau:
![]()
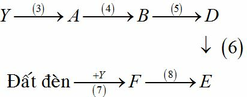
a) Xác định các chất X, Y, Z, A, B, D, E, F biết rằng:
- X là đơn chất của phi kim T, còn Y, Z là hợp chất hai nguyên tố, trong đó có chứa T. Dung dịch của Y làm quỳ tím chuyển đỏ. Z là muối Kali trong đó Kali chiếm 52,35% về khối lượng.
- Từ D có thể tạo thành A bằng phản ứng với oxi xúc tác men giấm.
b) Viết các phương trình phản ứng hóa học xảy ra ( ghi rõ điều kiện nếu có).
a) X là Cl2
Z là hợp chất 2 nguyên tố, Z là muối của Kali trong đó chiếm 52,35% về khối lượng => Z là KCl
Y là hợp chất 2 nguyên tố, trong đó có chứa Clo, dd Y làm quỳ tím chuyển sang màu đỏ => Y là axit => Y là HCl
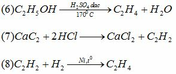
Đất đèn +HCl → F => F là C2H2
Ta có sơ đồ sau:
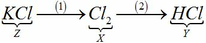

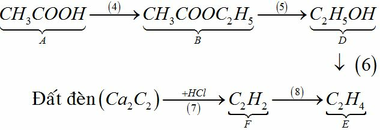
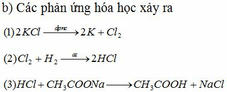
4 C H 3 C O O N a + C 2 H 5 O H ↔ H 2 S O 4 , t ∘ C H 3 C O O C 2 H 5 + H 2 O 5 C H 3 C O O C 2 H 5 + N a O H → C H 3 C O O N a + C 2 H 5 O H
Đúng 0
Bình luận (0)
Cho sơ đồ chuyển hóa sau: X → Y → Z→ Y→ X Biết: X là một phi kim; Y và Z là các hợp chất có chứa nguyên tố X. Dung dịch chất Y làm đỏ quì tím, Z là muối của natri, trong đó natri chiếm 39,316% về khối lượng. Xác định các chất X, Y, Z và hoàn thành các phương trình phản ứng theo sơ đồ chuyển hóa trên (mỗi mũi tên ứng với một phản ứng)
Đọc tiếp
Cho sơ đồ chuyển hóa sau:
X → Y → Z→ Y→ X
Biết: X là một phi kim; Y và Z là các hợp chất có chứa nguyên tố X. Dung dịch chất Y làm đỏ quì tím, Z là muối của natri, trong đó natri chiếm 39,316% về khối lượng. Xác định các chất X, Y, Z và hoàn thành các phương trình phản ứng theo sơ đồ chuyển hóa trên (mỗi mũi tên ứng với một phản ứng)
%Na = 39,316% => MZ = 58,5
=> Z là NaCl
=> X là H2 và Y là HCl
Pt: Cl2 + H2 → 2HCl
HCl + NaOH → NaCl + H2O
2NaCl + H2SO4đặc → Na2SO4 + 2HCl
4HCl + MnO2 → MnCl2 + Cl2↑ + 2H2O
Đúng 0
Bình luận (0)
Câu 2: Có sơ đồ biến hoá sau:
X Y Z Y X
Biết rằng, X là đơn chất của phi kim T; Y, Z là hợp chất gồm 2 nguyên tố trong đó chứa T. Dung dịch chất Y làm đỏ quỳ tím. Z là muối kali trong đó có 52,35%K. Xác định công thức các chất X, Y, Z và viết phương trình hoá học biểu diễn các biến hoá trên .
Một hợp chất gồm 2 nguyên tố C và H , trong đó C chiếm 82,76% phần còn lại là H, xác định CTHH của hợp chất trên , biết MHC = 58g
Đặt công thức của hợp chất là CxHy
=> mC = \(\frac{58\times82,76}{100}=48\left(gam\right)\)
=> nC = 48 / 12 = 4 (mol)
=> mH = 58 - 48 = 10 (gam)
=> nH = 10 / 1 = 10 (mol)
=> x : y = 4 : 10
=> Công thức hóa học: C4H10
Đúng 0
Bình luận (1)
X là 1 muối vô cơ trong phòng thi nghiệm Nung nóng 2 khí Y và Z trong đó khí Y không màu không mùi.Còn Z là 1 chất tao bởi 2 nguyên tố hidro và oxi xác định CTHH của X
Có sơ đồ biến hoá sau:
Biết rằng, X là đơn chất của phi kim T; Y, Z là hợp chất gồm 2 nguyên tố trong đó chứa T. Dung dịch chất Y làm đỏ quỳ tím. Z là muối kali trong đó có 52,35%K. Xác định công thức các chất X, Y, Z và viết phương trình hoá học biểu diễn các biến hoá trên
Đọc tiếp
Có sơ đồ biến hoá sau:

Biết rằng, X là đơn chất của phi kim T; Y, Z là hợp chất gồm 2 nguyên tố trong đó chứa T. Dung dịch chất Y làm đỏ quỳ tím. Z là muối kali trong đó có 52,35%K. Xác định công thức các chất X, Y, Z và viết phương trình hoá học biểu diễn các biến hoá trên
Chất A tạo bởi 3 nguyên tố X, Y, Z. Trong đó: X là kim loại phổ biến nhất trên Trái Đất, Z là phi kim phổ biến nhất trên Trái Đất. Trong A, % khối lượng của Z gấp 2 lần % khối lượng của Y, % khối lượng của X bằng 15,79%. Tìm CTHH của A biết 1 mol A nặng 342 gam.
X là kim loại phổ biến nhất trên Trái Đất ---> X là Al
Z là phi kim phổ biến nhất trên Trái Đất ---> Z là O
Ta có: \(\left\{{}\begin{matrix}\%Z=2.\%Y\\\%Y+\%Z+15,79\%=100\%\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}\%Z=56,14\%\\\%Y=28,07\%\end{matrix}\right.\)
\(\left\{{}\begin{matrix}m_{Al}=342.15,79\%=54\left(g\right)\\m_O=56,14\%.342=192\left(g\right)\\m_Y=342-54-192=96\left(g\right)\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}n_{Al}=\dfrac{54}{27}=2\left(mol\right)\\n_O=\dfrac{192}{16}=12\left(mol\right)\\n_Y=\dfrac{96}{M_Y}=k\left(mol\right)\left(đk:k\in N\text{*}\right)\end{matrix}\right.\)
CTHH là \(Al_2O_{12}Y_k\)
Vì tổng số oxi hoá của hợp chất luôn bằng không nên: (gọi số oxi hoá của Y là a)
\(2.\left(+3\right)+12.\left(-2\right)+ak=0\\ \Leftrightarrow ak-18=0\\ \Leftrightarrow ak=18\)
Hay \(a.\dfrac{96}{M_Y}=18\Leftrightarrow M_Y=\dfrac{16}{3}a\)
Vì a là số oxi hoá nên ta xét bảng
| a | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| MY | \(\dfrac{16}{3}\) | \(\dfrac{32}{3}\) | 16 | \(\dfrac{64}{3}\) | \(\dfrac{80}{3}\) | 32 | \(\dfrac{112}{3}\) |
| Loại | Loại | Loại | Loại | Loại | S (lưu huỳnh) | Loại |
\(\rightarrow k=\dfrac{96}{M_S}=\dfrac{96}{32}=3\left(TM\right)\)
CTHH là \(Al_2S_3O_{12}\) hay \(Al_2\left(SO_4\right)_3\)
Đúng 1
Bình luận (0)
a)Hợp chất Nicotin có 3 nguyên tố hóa học, trong đó C=74.07%,N=17.28%,H=8,65%
Hãy xác định CTHH của nicotin.Biết Nicotin có tỉ khối hơi so với H bằng 81
b)Hợp chất sắt(II) Sufat tạo bởi 3 nguyên tố, trong đó Fe=28%, S=24%, còn lại là Oxi
Hãy xác định CTHH của hợp chất. Biết khối lượng ml của hợp chất bằng 400g
cho mk sửa nha
a)Hợp chất Nicotin có 3 nguyên tố hóa học, trong đó C=74.07%,N=17.28%,H=8,65%
Hãy xác định CTHH của nicotin.Biết Nicotin có tỉ khối hơi so với H2 bằng 81
b)Hợp chất sắt(III) Sufat tạo bởi 3 nguyên tố, trong đó Fe=28%, S=24%, còn lại là Oxi
Hãy xác định CTHH của hợp chất. Biết khối lượng ml của hợp chất bằng 400g
Đúng 0
Bình luận (0)
a) Bạn lên trang của mình hoặc ib cho mình mik gửi link cho mình làm rồi nha Câu hỏi của Vy Tuong
b) Gọi CTDC là : FexSyOz
Khối lượng của nt trong hợp chất FexSyOz
%O = 100% - ( %S + %Fe ) = 100 -( 28 + 24 ) = 48%
\(m_{Fe}=\frac{M_{Fe_xS_yO_z}\times\%Fe}{100\%}=\frac{400\times28\%}{100\%}=112\left(g\right)\)
\(m_S=\frac{M_{Fe_xS_yO_z}\times\%S}{100\%}=\frac{400\times24\%}{100\%}=96\left(g\right)\)
\(m_O=\frac{M_{Fe_xS_yO_z}\times\%O}{100\%}=\frac{400\times48\%}{100\%}=192\left(g\right)\)
Số mol của mỗi nt trong 1 mol hợp chất FexSyOz là :
\(n_{Fe}=\frac{m}{M}=\frac{112}{56}=2\left(mol\right)\)
\(n_S=\frac{m}{M}=\frac{96}{32}=3\left(mol\right)\)
\(n_O=\frac{m}{M}=\frac{192}{16}=12\left(mol\right)\)
Suy ra trong 1 mol phân tử FexSyOz có : 2 nguyên tử Fe , 3 nguyên tử S , 12 nguyên tử O
Vậy CTHH là : \(Fe_2\left(S0_4\right)_3\)
Chúc bạn học tốt =)) ![]()
Đúng 0
Bình luận (3)
Câu 1 : Hợp chất A có thành phần % về khối lượng là : 85,7% C, còn lại là H. Hãy xác định CTHH của A, biết tỉ khối của khí A so với hidro là 14. Tìm CTHH của hợp chất ? Câu 2 : Một hợp chất khí có tỉ khối đối với không khí là 0,582 và trong đó N là 82,35%, còn lại là H a. Lập CTHH của hợp chất khíb,Tính thể tích ở điều kiện tiêu chuẩn của 3,4 gam hợp khí trên Câu 3 : Cho 4,8g Magie bằng dung dịch 14,6g axit clohidric HCl, thu được muối magie clorua và 0,4g khí hidro. a, viết PTHH của phản ứngb,...
Đọc tiếp
Câu 1 : Hợp chất A có thành phần % về khối lượng là : 85,7% C, còn lại là H. Hãy xác định CTHH của A, biết tỉ khối của khí A so với hidro là 14. Tìm CTHH của hợp chất ?
Câu 2 : Một hợp chất khí có tỉ khối đối với không khí là 0,582 và trong đó N là 82,35%, còn lại là H a. Lập CTHH của hợp chất khí
b,Tính thể tích ở điều kiện tiêu chuẩn của 3,4 gam hợp khí trên
Câu 3 : Cho 4,8g Magie bằng dung dịch 14,6g axit clohidric HCl, thu được muối magie clorua và 0,4g khí hidro. a, viết PTHH của phản ứng
b, tính khối lượng và số mol của MgCl2

















