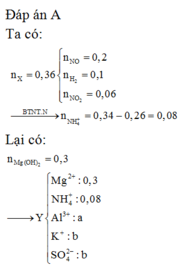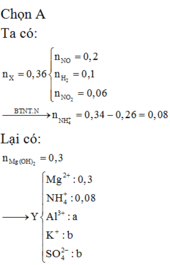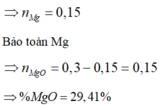40g hỗn hợp AL,AL2O3,MgO đc hòa tan bằng dung dịch NaOH 2M thì thể tích NaOH vừa đủ phản ứng là 300ml,đồng thời thoát ra 6,72dm3 H2(đktc).Tìm % khối lượng hỗn hợp đầu

Những câu hỏi liên quan
Cho 40g hỗn hợp Al, Al2O3, MgO được hòa tan bằng dung dịch NaOH 2M thì thể tích NaOH vừa đủ phản ứng là 300ml đồng thời thoát ra 6,72 dm3 khí H2. Tìm % khối lượng của các chất ban đầu.
\(n_{NaOH}=0,3.2=0,6mol\)
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3mol\)
- PTHH: 2Al+2NaOH+2H2O\(\rightarrow\)2NaAlO2+3H2
Al2O3+2NaOH\(\rightarrow\)2NaAlO2+H2O
\(n_{Al}=\dfrac{2}{3}n_{H_2}=\dfrac{2}{3}.0,3=0,2mol\)
\(m_{Al}=0,2.27=5,4g\)
\(n_{NaOH\left(2\right)}=0,6-n_{NaOH\left(1\right)}=0,6-0,2=0,4mol\)
\(n_{Al_2O_3}=\dfrac{1}{2}n_{NaOH\left(2\right)}=\dfrac{1}{2}.0,4=0,2mol\)
\(m_{Al_2O_3}=0,2.102=20,4g\)
\(m_{MgO}=40-5,4-20,4=14,2g\)
Từ đó: \(\%Al=\dfrac{5,4.100}{40}=13,5\%\)
\(\%Al_2O_3=\dfrac{20,4.100}{40}=51\%\)
%MgO=100%-13,5%-51%=35,5%
Đúng 0
Bình luận (0)
2Al + 2NaOH + 2H2O ----->2NaAlO2 + 3H2
Al2O3 + 2NaOH----->2NaAlO2 + H2O
nH2 = 0,3 mol
=> nAl = nNaOH = 0,3.2/3 = 0,2 mol
=> mAl = 0,2 . 27 = 5,4 => %Al = 13,5 %
theo đề bài nNaOH = 0,6 => n_NaOH còn lại = 0,6 - 0,2 = 0,4
=> nAl2O3 = 1/2nNaOH = 0,4/2 = 0,2
=> mAl2O3 = 0,2 . 102 = 20,4 => %Al2O3 = 51 %
=> %MgO = 100 - ( 13,5 + 51 ) = 35,5 %
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 15,6 gam hỗn hợp X gồm Al và Al2O3 bằng lượng vừa đủ V ml dung dịch
NaOH 1M, sau phản ứng thu được 6,72 lít khí H2 (đktc).
a. Viết các PTHH xảy ra.
b. Tính khối lượng mỗi chất trong hỗn hợp X.
c. Tính thể tích dung dịch NaOH đã dùng.
\(n_{H2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
a) Pt : \(2Al+2NaOH+2H_2O\rightarrow2NaAlO_2+3H_2|\)
2 2 2 2 3
0,2 0,2 0,3
\(Al_2O_3+2NaOH\rightarrow2NaAlO_2+H_2O|\)
1 2 2 1
0,1 0,2
b) \(n_{Al}=\dfrac{0,3.2}{3}=0,2\left(mol\right)\)
\(m_{Al}=0,2.27=5,4\left(g\right)\)
\(m_{Al2O3}=15,6-5,4=10,2\left(g\right)\)
c) Có : \(m_{Al2O3}=10,2\left(g\right)\)
\(n_{Al2O3}=\dfrac{10,2}{102}=0,1\left(mol\right)\)
\(n_{NaOH\left(tổng\right)}=0,2+0,2=0,4\left(mol\right)\)
\(V_{ddNaOH}=\dfrac{0,4}{1}=0,4\left(l\right)=400\left(ml\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (0)
Câu 2: Hòa tan hoàn toàn 12,9 gam hỗn hợp gồm Al và Al2O3 bằng lượng dung dịch NaOH(vừa đủ), thu được 3,36 lít H2 (ở đktc).
a. Viết các phương trình phản ứng hóa học xảy ra.
b. Tính thành phần khối lượng của mỗi chất trong hỗn hợp ban đầu đã dùng.
giúp mình với ạ cảm ơn ..
Lượng khí hidro thoát ra là 0,15 mol.
a) Al2O3 + 2NaOH \(\rightarrow\) 2NaAlO2 + H2O
2Al + 2NaOH + 2H2O \(\rightarrow\) 2NaAlO2 + 3H2.
b) Lượng Al phản ứng bằng 2/3 số mol khí hidro thoát ra và bằng 0,1 mol.
\(\Rightarrow\) %mnhôm=\(\dfrac{27.0,1}{12,9}\).100%\(\approx\)20,93%, %mnhôm oxit\(\approx\)100%-20,93%\(\approx\)79,07%.
Đúng 3
Bình luận (0)
Hòa tan hết m gam hỗn hợp gồm Al, Mg, MgO trong dung dịch hỗn hợp chứa 0,34 mol HNO3 và KHSO4. Sau phản ứng thu được 8,064 lít hỗn hợp khí X ở đktc gồm NO, H2 và NO2 với tỷ lệ mol tương ứng là 10 : 5 : 3 và dung dịch Y chỉ chứa muối. Cho NaOH dư vào Y thì thấy có 2,28 mol NaOH tham gia phản ứng, đồng thời có 17,4 gam kết tủa xuất hiện. Phần trăm khối lượng của MgO trong hỗn hợp ban đầu là: A. 29,41% B. 26,28% C. 32,14% D. 28,36%
Đọc tiếp
Hòa tan hết m gam hỗn hợp gồm Al, Mg, MgO trong dung dịch hỗn hợp chứa 0,34 mol HNO3 và KHSO4. Sau phản ứng thu được 8,064 lít hỗn hợp khí X ở đktc gồm NO, H2 và NO2 với tỷ lệ mol tương ứng là 10 : 5 : 3 và dung dịch Y chỉ chứa muối. Cho NaOH dư vào Y thì thấy có 2,28 mol NaOH tham gia phản ứng, đồng thời có 17,4 gam kết tủa xuất hiện. Phần trăm khối lượng của MgO trong hỗn hợp ban đầu là:
A. 29,41%
B. 26,28%
C. 32,14%
D. 28,36%
Hòa tan hết m gam hỗn hợp gồm Al, Mg, MgO trong dung dịch hỗn hợp chứa 0,34 mol HNO3 và KHSO4. Sau phản ứng thu được 8,064 lít hỗn hợp khí X ở đktc gồm NO, H2 và NO2 với tỷ lệ mol tương ứng là 10 : 5 : 3 và dung dịch Y chỉ chứa muối. Cho NaOH dư vào Y thì thấy có 2,28 mol NaOH tham gia phản ứng, đồng thời có 17,4 gam kết tủa xuất hiện. Phần trăm khối lượng của MgO trong hỗn hợp ban đầu là: A. 29,41% B. 26,28% C. 32,14% D. 28,36%
Đọc tiếp
Hòa tan hết m gam hỗn hợp gồm Al, Mg, MgO trong dung dịch hỗn hợp chứa 0,34 mol HNO3 và KHSO4. Sau phản ứng thu được 8,064 lít hỗn hợp khí X ở đktc gồm NO, H2 và NO2 với tỷ lệ mol tương ứng là 10 : 5 : 3 và dung dịch Y chỉ chứa muối. Cho NaOH dư vào Y thì thấy có 2,28 mol NaOH tham gia phản ứng, đồng thời có 17,4 gam kết tủa xuất hiện. Phần trăm khối lượng của MgO trong hỗn hợp ban đầu là:
A. 29,41%
B. 26,28%
C. 32,14%
D. 28,36%
Hòa tan hết m gam hỗn hợp gồm Al, Mg, MgO trong dung dịch hỗn hợp chứa HNO3(0,34 mol) và KHSO4. Sau phản ứng thu được 8,064 lít (đktc) hỗn hợp khí X gồm NO, H2 và NO2 với tỉ lệ mol tương ứng 10 : 5 : 3 và dung dịch Y chỉ chứa muối. Cho NaOH dư vào Y thì thấy có 2,28 mol NaOH tham gia phản ứng, đồng thời thấy có 17,4 gam kết tủa xuất hiện. Phần trăm khối lượng MgO trong hỗn hợp ban đầu là A. 29,41%. B. 26,28%. C. 32,14%. D. 28,36%.
Đọc tiếp
Hòa tan hết m gam hỗn hợp gồm Al, Mg, MgO trong dung dịch hỗn hợp chứa HNO3(0,34 mol) và KHSO4. Sau phản ứng thu được 8,064 lít (đktc) hỗn hợp khí X gồm NO, H2 và NO2 với tỉ lệ mol tương ứng 10 : 5 : 3 và dung dịch Y chỉ chứa muối. Cho NaOH dư vào Y thì thấy có 2,28 mol NaOH tham gia phản ứng, đồng thời thấy có 17,4 gam kết tủa xuất hiện. Phần trăm khối lượng MgO trong hỗn hợp ban đầu là
A. 29,41%.
B. 26,28%.
C. 32,14%.
D. 28,36%.
Nung 78,88 gam hỗn hợp X gồm Al, Al2O3, Fe3O4 và Cr2O3 trong khí trơ, đến phản ứng hoàn toàn thu được rắn Y. Chia Y làm 2 phần bằng nhau. Phần 1 cho vào dung dịch NaOH loãng dư thấy lượng NaOH phản ứng là 16,0 gam, đồng thời thoát ra 896 ml khí H2 (đktc). Hòa tan hết phần 2 trong dung dịch HCl dư, đun nóng thu được dung dịch Z chứa 98,64 gam muối. Phần trăm khối lượng của Al2O3 trong X là A. 5,17% B. 10,34%. C. 13,79%. D. 12,07%.
Đọc tiếp
Nung 78,88 gam hỗn hợp X gồm Al, Al2O3, Fe3O4 và Cr2O3 trong khí trơ, đến phản ứng hoàn toàn thu được rắn Y. Chia Y làm 2 phần bằng nhau. Phần 1 cho vào dung dịch NaOH loãng dư thấy lượng NaOH phản ứng là 16,0 gam, đồng thời thoát ra 896 ml khí H2 (đktc). Hòa tan hết phần 2 trong dung dịch HCl dư, đun nóng thu được dung dịch Z chứa 98,64 gam muối. Phần trăm khối lượng của Al2O3 trong X là
A. 5,17%
B. 10,34%.
C. 13,79%.
D. 12,07%.
Đáp án A
Cho phần 1 tác dụng với 0,4 mol NaOH thấy thoát ra 0,04 mol H2.
Do vậy Al dư 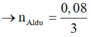
BTNT: ![]()
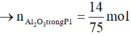
Ta có khối lượng mỗi phần là 39,44 gam.
![]()
Phần 2 tan trong HCl thu được dung dịch Z chứa 98,64 gam muối.
![]()
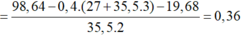
Giải được số mol Cr và Fe trong mỗi phần là 0,12 và 0,24 mol.
Bảo toàn O:
![]()
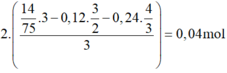
Đúng 0
Bình luận (0)
Nung 78,88 gam hỗn hợp X gồm Al, Al2O3, Fe3O4 và Cr2O3 trong khí trơ, đến phản ứng hoàn toàn thu được rắn Y. Chia Y làm 2 phần bằng nhau. Phần 1 cho vào dung dịch NaOH loãng dư thấy lượng NaOH phản ứng là 16,0 gam, đồng thời thoát ra 896 ml khí H2 (đktc). Hòa tan hết phần 2 trong dung dịch HCl dư, đun nóng thu được dung dịch Z chứa 98,64 gam muối. Phần trăm khối lượng của Al2O3 trong X là A. 5,17%. B. 10,34%. C. 13,79%. D. 12,07%.
Đọc tiếp
Nung 78,88 gam hỗn hợp X gồm Al, Al2O3, Fe3O4 và Cr2O3 trong khí trơ, đến phản ứng hoàn toàn thu được rắn Y. Chia Y làm 2 phần bằng nhau. Phần 1 cho vào dung dịch NaOH loãng dư thấy lượng NaOH phản ứng là 16,0 gam, đồng thời thoát ra 896 ml khí H2 (đktc). Hòa tan hết phần 2 trong dung dịch HCl dư, đun nóng thu được dung dịch Z chứa 98,64 gam muối. Phần trăm khối lượng của Al2O3 trong X là
A. 5,17%.
B. 10,34%.
C. 13,79%.
D. 12,07%.
Đáp án A
Cho phần 1 tác dụng với 0,4 mol NaOH thấy thoát ra 0,04 mol H2.
Do vậy Al dư
→ n A l d ư = 0 , 08 3 B T N T : n A l ( P 1 ) = n N a O H = 0 , 4 → n A l 2 O 3 t r o n g P 1 = 14 75 m o l
Ta có khối lượng mỗi phần là 39,44 gam.
→ m C r + m F e = 19 , 68 g a m
Phần 2 tan trong HCl thu được dung dịch Z chứa 98,64 gam muối.
→ n C r + n F e = 98 , 64 - 0 , 4 ( 27 + 35 , 5 . 3 ) - 19 , 68 35 , 5 . 2 = 0 . 36
Giải được số mol Cr và Fe trong mỗi phần là 0,12 và 0,24 mol.
Bảo toàn O:
n A l 2 O 3 t r o n g X = 2 14 75 . 3 - 0 , 12 . 3 2 - 0 , 24 . 4 3 3 = 0 , 04 m o l → % A l 2 O 3 = 5 , 17 %
Đúng 0
Bình luận (0)
Nung 78,88 gam hỗn hợp X gồm Al, Al2O3, Fe3O4 và Cr2O3 trong khí trơ, đến phản ứng hoàn toàn thu được rắn Y. Chia Y làm 2 phần bằng nhau. Phần 1 cho vào dung dịch NaOH loãng dư thấy lượng NaOH phản ứng là 16,0 gam, đồng thời thoát ra 896 ml khí H2 (đktc). Hòa tan hết phần 2 trong dung dịch HCl dư, đun nóng thu được dung dịch Z chứa 98,64 gam muối. Phần trăm khối lượng của Al2O3 trong X là: A. 5,17% B. 12,07% C. 13,79% D. 10,34%
Đọc tiếp
Nung 78,88 gam hỗn hợp X gồm Al, Al2O3, Fe3O4 và Cr2O3 trong khí trơ, đến phản ứng hoàn toàn thu được rắn Y. Chia Y làm 2 phần bằng nhau. Phần 1 cho vào dung dịch NaOH loãng dư thấy lượng NaOH phản ứng là 16,0 gam, đồng thời thoát ra 896 ml khí H2 (đktc). Hòa tan hết phần 2 trong dung dịch HCl dư, đun nóng thu được dung dịch Z chứa 98,64 gam muối. Phần trăm khối lượng của Al2O3 trong X là:
A. 5,17%
B. 12,07%
C. 13,79%
D. 10,34%