Muối Kali nitơrát (KNO3) dễ phân hủy theo phản ứng: 2KNO3 -> 2KNO2 + O2
Tính khối lượng KNO3 để có đủ O2 cho phản ứng với 40g hỗn hợp gồm lưu huỳnh và than, trong đó than chiếm 60% về khối lượng. ( Hỗn hợp KNO3, S và C dùng làm thuốc súng.
Hòa tan hoàn toàn hỗn hợp H gồm Mg (5a mol) và Fe3O4 (a mol) trong dung dịch chứa KNO3 và 0,725 mol HCl (vừa đủ), cô cạn dung dịch sau phản ứng thì thu được lượng muối khan nặng hơn khối lượng hỗn hợp H là 26,23 gam. Biết kết thúc phản ứng thu được 0,08 mol hỗn hợp khí Z chứa H2 và NO, tỉ khối của Z so với H2 bằng 11,5. Phần trăm khối lượng muối khan có giá trị gần nhất với
A. 17%.
B. 18%.
C. 26%.
D. 6%.
Nhiệt phân hoàn toàn hỗn hợp 2 muối KNO3 và Cu(NO3)2 có khối lượng 5,4 gam. Sau khi phản ứng kết thúc thu được hỗn hợp khí X. Biết \(\overline{M_x}\)= 32,1818. Vậy khối lượng của mỗi muối nitrat trong hỗn hợp bằng:
A. 18 gam và 60 gam
B. 19,2 gam và 74,2 gam
C. 20,2gam và 75,2 gam
D. 30 gam và 70 gam
Hỗn hợp hơi gồm NO2 và O2.
Từ tỷ khối của hỗn hợp 32,1818, lập sơ đồ đường chéo
=>\(\dfrac{n_{NO_2}}{n_{O_2}}\) = \(\dfrac{909}{69091}\)
Đặt nKNO3 = a mol và nCu(NO3)2 = b mol
=> 101 a + 188 b = 5,4 gam.(1)
Nhiệt phân muối thu được : (0,5a + 0,5b) mol O2 và 2b mol NO2.
→ \(\dfrac{2b}{0,5a+0,5b}\) = \(\dfrac{909}{69091}\). (2).
=>a=0,05 ; b=1,76.10-4
Bạn xem lại đề !
Nhiệt phân hoàn toàn hỗn hợp 2 muối KNO3 và Fe(NO3)2 sau phản ứng thu được hỗn hợp X gồm 2 khí có tỉ khối so với H2 là 21,6. Phần trăm khối lượng của Fe(NO3)2 là
A. 60%.
B. 40%.
C. 78,09%.
D. 34,3%.
Hòa tan hoàn toàn m gam hỗn hợp X gồm Fe, Fe3O4, FeS (trong đó nguyên tố oxi chiếm 12,5% về khối lượng) trong dung dịch chứa a mol KNO3 và 0,43 mol H2SO4 (loãng), sau phản ứng thu được khi NO (sản phẩm khử duy nhất của N+5 và dung dịch Y. Cho Y phản ứng vừa đủ với 740ml dung dịch KOH 1M, thu được 21,4 gam kết tủa và dung dịch Z chứa 101,14 gam hỗn hợp muối. Giá trị của a là
A. 0,38.
B. 0,40.
C. 0,42.
D. 0,44.
Đốt cháy 13,44 lít hỗn hợp khí gồm C2H2 và CH4 trong khí Õi vừa đủ đến phản ứng kết thúc.Biết trog hỗn hợp này V-C2H2 gấp 2 lần VCH4
a.Tính: VO2 cần dùng và VCO2 sinh ra
b.Tính khối lượng KMnO4 cần phân hủy để có lượng khí O2 dùng cho phản ứng trên biết hiệu suất phản ứng đạt 80% ( Thể tích các chất khí đo được ở đktc)
a)
\(\left\{{}\begin{matrix}n_{C_2H_2}+n_{CH_4}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\\\dfrac{n_{C_2H_2}}{n_{CH_4}}=2\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}n_{C_2H_2}=0,4\left(mol\right)\\n_{CH_4}=0,2\left(mol\right)\end{matrix}\right.\)
PTHH: 2C2H2 + 5O2 --to--> 4CO2 + 2H2O
0,4----->1------------->0,8
CH4 + 2O2 --to--> CO2 + 2H2O
0,2-->0,4---------->0,2
=> VO2 = (1+0,4).22,4 = 31,36(l)
=> VCO2 = (0,8 + 0,2).22,4 = 22,4 (l)
b)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
2,8<---------------------------------1,4
=> \(m_{KMnO_4\left(PTHH\right)}=2,8.158=442,4\left(g\right)\)
=> mKMnO4 (thực tế) = 442,4 : 80% = 553(g)
Lấy m gam hỗn hợp rắn gồm Mg, Zn, FeCO3, FeS2 (trong đó nguyên tố oxi chiếm 16,71% khối lượng hỗn hợp) nung trong bình chứa 0,16 mol O2, sau phản ứng hoàn toàn thu được hỗn hợp chất rắn X không chứa nguyên tố lưu huỳnh và hỗn hợp khí Y (có tỉ khối so với H2 là 27). Cho X vào dung dịch chứa 0,72 mol HCl và 0,03 mol NaNO3, sau phản ứng hoàn toàn thấy dung dịch thu được chỉ chứa muối clorua và 1,12 lít (đktc) hỗn hợp hai khí thoát ra có khối lượng là 0,66 gam (trong đó có một khí hóa nâu ngoài không khí). Giá trị của m gần nhất với giá trị nào sau đây?
A. 23.
B. 22.
C. 24.
D. 25.
Lấy m gam hỗn hợp rắn gồm Mg, Zn, FeCO3, FeS2 (trong đó nguyên tố oxi chiếm 16,71% khối lượng hỗn hợp) nung trong bình chứa 0,16 mol O2, sau phản ứng hoàn toàn thu được hỗn hợp chất rắn X không chứa nguyên tố lưu huỳnh và hỗn hợp khí Y (có tỉ khối so với H2 là 27). Cho X vào dung dịch chứa 0,72 mol HCl và 0,03 mol NaNO3, sau phản ứng hoàn toàn thấy dung dịch thu được chỉ chứa muối clorua và 1,12 lít (đktc) hỗn hợp hai khí thoát ra có khối lượng là 0,66 gam (trong đó có một khí hóa nâu ngoài không khí). Giá trị của m gần nhất với giá trị nào sau đây?
A. 23.
B. 22
C. 24.
D. 25
Chọn A.
Khi nung hỗn hợp trên với O2 thu được hai khí CO2 và SO2 có số mol bằng nhau (vì M = 54)
Quy đổi chất rắn X thành M (kim loại) và O
Khi cho X tác dụng với HCl và NaNO3 thu được dung dịch Na+ (0,03 mol), Mn+, NH4+, Cl- (0,72 mol) và hỗn hợp hai khí gồm H2: 0,03 mol và NO: 0,02 mol

Hòa tan hoàn toàn hỗn hợp X gồm Mg (5a mol) và Fe3O4 (a mol) trong dung dịch chứa KNO3 và 0,725 mol HCl, cô cạn dung dịch sau phản ứng thì thu được lượng muối khan nặng hơn khối lượng hỗn hợp X là 26,23g. Biết kết thúc phản ứng thu được 0,08 mol hỗn hợp khí Z chứa H2 và NO, tỉ khối của Z so với H2 bằng 11,5. Phần trăm khối lượng sắt có trong muối khan có giá trị gần nhất với
A. 17%.
B. 18%.
C. 26%.
D. 6%.
Đáp án A
Do tạo H2 => ion NO3- đã chuyển hết thành NO
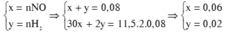
Đặt x = nKNO3
Bảo toàn N => nKNO3 = nNO + nNH4+ => nNH4+ = x – 0,06
nHCl = nH+ = 4nNO + 2nH2 + 10nNH4+ + 2nO => 0,725 = 4.0,06 + 2.0,02 + 10(x – 0,06) + 8a
=> 8a + 10x = 1,045 (1)
mmuối = mMg + mFe + mK+ + mNH4+ + mCl- = 24.5a + 56.3a + 39x + 18(x – 0,06) + 35,5.0,725
= 288a + 57x + 24,6575
Mà mmuối – mX = 26,23 => 288a + 57x + 24,6575 – 24.5a – 232a = 26,23 => –64a + 57x = 1,5725 (2)
(1), (2) a = 0,04 và x = 0,0725 => mmuối = 288a + 57x + 24,6575 = 40,31g
=> %mFe trong muối = 56.3.0,04.100%/40,31 = 16,67%
Hòa tan hoàn toàn hỗn hợp X gồm Mg (5a mol) và Fe3O4 (a mol) trong dung dịch chứa KNO3 và 0,725 mol HCl, cô cạn dung dịch sau phản ứng thì thu được lượng muối khan nặng hơn khối lượng hỗn hợp X là 26,23g. Biết kết thúc phản ứng thu được 0,08 mol hỗn hợp khí Z chứa H2 và NO, tỉ khối của Z so với H2 bằng 11,5. Phần trăm khối lượng sắt có trong muối khan có giá trị gần nhất với
A. 17%.
B. 18%.
C. 26%.
D. 6%.