Số lít khí oxi (ở đktc) cần dùng để đốt cháy hoàn toàn 0,2 gam khí hiđro là
(Cho NTK: H =1 ; O=16)
A.3,36.
B.2,24.
C.1,12.
D.11,2.
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là:
A. 70,0 lít
B. 78,4 lít
C. 84,0 lít
D. 56,0 lít
Đáp án A
Hỗn hợp khí gồm CH4, C2H6 và C3H8 là các hidrocacbon.
Mà khi đốt cháy 1 hidrocacbon bất kì ta luôn có:
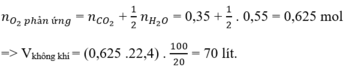
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là :
A. 78,4 lít
B. 56,0 lít
C. 70,0 lít
D. 84,0 lít
Đốt cháy hoàn toàn một thể tích khí thiên nhiêm gồm: metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là
A. 84,0 lít
B. 70,0 lít
C. 78,4 lít
D. 56,0 lít
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là
A. 70,0 lít
B. 84,0 lít
C. 56,0 lít.
D. 78,4 lít.
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là:
A. 70,0 lít.
B. 78,4 lít.
C. 84,0 lít.
D. 56,0 lít.
Bài 1: Đốt cháy hoàn toàn 1,3 gam C2H2 cần dùng bao nhiêu lít khí oxi ở đktc ? bao nhiêu lít (đktc) không khí chứa 20% thể tích khí oxi
\(2C_2H_2+5O_2-^{t^o}\rightarrow4CO_2+2H_2O\\ n_{C_2H_2}=\dfrac{1,3}{26}=0,05\left(mol\right)\\ n_{O_2}=\dfrac{5}{2}n_{C_2H_2}=0,125\left(mol\right)\\ \Rightarrow V_{O_2}=2,8\left(l\right)\\ Vìtrongkhôngkhíchứa20\%O_2\\ \Rightarrow V_{kk}=\dfrac{2,8}{20\%}=14\left(l\right)\)
Để đốt cháy hoàn toàn 32 gam S cần dùng bao nhiêu lít không khí ở đktc? (S = 32) (Biết oxi chiếm 1/5 thể tích không khí và sản phẩm thu được là khí SO2) A. 112 lít B. 224 lít C. 336 lít D. 448 lít
\(pthh:S+O_2\overset{t^o}{--->}SO_2\)
\(n_S=\dfrac{32}{32}=1\left(mol\right)\)
Theo pt: \(n_{O_2}=n_S=1\left(mol\right)\)
\(\Rightarrow V_{kk}=1.22,4.5=112\left(lít\right)\)
Chọn A
A là hỗn hợp gồm Na, Fe, Cu.
-TN1: Đốt cháy hoàn toan m gam A cần 5,04 lít khí oxi ở đktc.
-TN2: Cho m gam A vào dung dịch HCl dư thoát ra 5,6 lít khí hiđro ở đktc.
-TN3: Cho m gam A vào nước dư thoát ra 2,24 lít khí hiđro ở đktc.
1. Viết các phương trinh hóa học xảy ra.
2. Tính thành phần phần trăm theo số mol của từng chất trong hỗn hợp A và tính m?
$1)$
$4Na+O_2\xrightarrow{t^o}2Na_2O$
$3Fe+2O_2\xrightarrow{t^o}Fe_3O_4$
$2Cu+O_2\xrightarrow{t^o}2CuO$
$2Na+2HCl\to 2NaCl+H_2$
$Fe+2HCl\to FeCl_2+H_2$
$2Na+2H_2O\to 2NaOH+H_2$
$2)$
$n_{O_2}=0,225(mol)$
$n_{H_2(TN_2)}=0,25(mol)$
$n_{H_2(TN_3)}=0,1(mol)$
Theo PT: $\begin{cases} n_{Na}=2n_{H_2(TN_3)}=0,2(mol)\\ 0,5n_{Na}+n_{Fe}=n_{H_2(TN_2)}=0,25(mol)\\ 0,25n_{Na}+\dfrac{2}{3}n_{Fe}+0,5n_{Cu}=n_{O_2}=0,225(mol) \end{cases}$
$\to\begin{cases} n_{Na}=0,2(mol)\\ n_{Fe}=0,15(mol)\\ n_{Cu}=0,15(mol) \end{cases}$
$\to \begin{cases} \%n_{Na}=\dfrac{0,2}{0,2+0,15+0,15}.100\%=40\%\\ \%n_{Fe}=\%n_{Cu}=\dfrac{0,15}{0,2+0,15+0,15}.100\%=30\% \end{cases}$
$\to m=0,2.23+0,15.56+0,15.64=22,6(g)$
thể tích khí oxi ( ở đktc ) tối thiểu cần dùng để đốt cháy hoàn toàn 6,72 lít khí C2H4 ( ở đktc) là
A:6,72 lít
B:11,2 lít
C:13,44 lít
D:20,16 lít
TK
a) C2H4 + O2 ---> 2CO2 + 2H2O
0,3 ---->. 0,6
- V CO2 = 0,6×22,4 = 13,44 lít
b) CO2 + Ca(OH)2 ---> CaCO3 + H2O
0,6 ---> 0,6
m Ca(OH)2 = 0,6×74 = 44,4 g
\(n_{C_2H_4=\dfrac{6,72}{22,4}=0,3}\) ( mol )
\(C_2H_4+3O_2\underrightarrow{t^o}2H_2O+2CO_2\)
0,3 -> 0,9 /mol
\(V=0,9.22,4=20,16\left(l\right)\) . Chọn D