Bài 9: Đốt cháy hoàn toàn 5,2g hợp chất hữu cơ A rồi cho sản phẩm lần lượt qua bình H2SO4 đđ thì khối lượng bình tăng 1,8g và qua bình đựng nước vôi trong dư thì có 15g kết tủa. Xác định CTPT của A biết ĐS: C3H4O4

Những câu hỏi liên quan
Đốt cháy hoàn toàn 10,4g chất hữu cơ A rồi cho sản phẩm cháy lần lượt qua bình 1 đựng H2SO4đ và bình 2 chứa nước vôi trong dư, thấy khối lượng bình 1 tăng 3,6g, bình 2 thu được 30g kết tủa. Khi hoá hơi 5,2g A thu được một thể tích đúng bằng thể tích của 1,6 gam oxi ở cùng điều kiện. Xác định CTPT của A.
Đốt cháy hoàn toàn 3,52g hợp chất hữu cơ(A) rồi cho sản phẩm lần lượt qua bình(1) chứa H2SO4 đặc và bình(2) chứa nước vôi trong dư. Khi kết thúc thí nghiệm thì khối lượng bình(1) tăng 2,88g; bình(2) tăng 7,04g.a) Tìm CTĐGNb) Xác định công thức phân tử của(A). Khi hóa hơi 7,04g (A) thu được một thể tích đúng bằng thể tích của 2,24g khí N2 ở cùng điều kiện.
Đọc tiếp
Đốt cháy hoàn toàn 3,52g hợp chất hữu cơ(A) rồi cho sản phẩm lần lượt qua bình(1) chứa H2SO4 đặc và bình(2) chứa nước vôi trong dư. Khi kết thúc thí nghiệm thì khối lượng bình(1) tăng 2,88g; bình(2) tăng 7,04g.
a) Tìm CTĐGN
b) Xác định công thức phân tử của(A). Khi hóa hơi 7,04g (A) thu được một thể tích đúng bằng thể tích của 2,24g khí N2 ở cùng điều kiện.
Đốt cháy hoàn toàn 14 gam một hợp chất hữu cơ Z, rồi dẫn toàn bộ hỗn hợp sản phẩm cháy lần lượt qua hai bình: bình 1 đựng H2SO4 đặc, bình 2 đựng dung dịch nược vôi trong dư. Thấy khối lượng bình 1 tăng 9 gam và ở bình 2 xuất hiện 75 gam kết tủa. Biết 2,8 gam Z có thể tích đúng bằng thể tích của 1,4 gam khí nitơ ở cùng điều kiện về nhiệt độ và áp suất. Xác định CTPT của Z.
Đọc tiếp
Đốt cháy hoàn toàn 14 gam một hợp chất hữu cơ Z, rồi dẫn toàn bộ hỗn hợp sản phẩm cháy lần lượt qua hai bình: bình 1 đựng H2SO4 đặc, bình 2 đựng dung dịch nược vôi trong dư. Thấy khối lượng bình 1 tăng 9 gam và ở bình 2 xuất hiện 75 gam kết tủa. Biết 2,8 gam Z có thể tích đúng bằng thể tích của 1,4 gam khí nitơ ở cùng điều kiện về nhiệt độ và áp suất. Xác định CTPT của Z.
Đốt cháy hoàn toàn 10,4 gam hợp chất hữu cơ rồi cho sản phẩm lần lượt qua bình 1 đựng H2SO4 đặc, bình 2 chứa nước vôi trong dư, thấy khối lượng bình 1 tăng 3,6 gam, bình 2 thu được 30 gam kết tủa. Khi hóa hơi 5,2 gam A thu được một thể tích đúng bằng thể tích của 1,6 gam O2 ở cùng điều kiện nhiệt độ và áp suất. Xác định CTPT của A
Ta có: \(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\Rightarrow n_H=0,2.2=0,4\left(mol\right)\)
\(n_C=n_{CO_2}=n_{CaCO_3}=\dfrac{30}{100}=0,3\left(mol\right)\)
⇒ mC + mH = 0,3.12 + 0,4.1 = 4 (g) < 10,4 (g)
→ A chứa C, H và O.
⇒ mO = 10,4 - 4 = 6,4 (g) ⇒ nO = 0,4 (mol)
Gọi CTPT của A là CxHyOz.
⇒ x:y:z = 0,3:0,4:0,4 = 3:4:4
→ CTPT của A có dạng (C3H4O4)n.
Mà: \(n_{A\left(5,2\left(g\right)\right)}=n_{O_2}=\dfrac{1,6}{32}=0,05\left(mol\right)\Rightarrow M_A=\dfrac{5,2}{0,05}=104\left(g/mol\right)\)
\(\Rightarrow n=\dfrac{104}{12.3+4+16.4}=1\)
Vậy: CTPT của A là C3H4O4.
Đúng 3
Bình luận (0)
Khi đốt cháy hoàn toàn 9,4 gam hợp chất hữu cơ X chứa C, H,O có CTPT trùng CTDGN . Dẫn sản phẩm thu được qua bình 1 đựng H2SO4 đặc , bình 2 đựng nước vôi trong dư, thấy bình 1 tăng 5,4 gam; bình 2 tăng 26, 4 gam. có 50 gam kết tủa và khối lượng dung dịch giảm 13,6 gam. X có khả năng phản ứng với dung dịch NaOH. Cho 4,7 gam X vào 100ml dung dịch NaOH 1 M . Cô cạn dung dịch thu được m gam rắn. Giá trị của m là?
Đọc tiếp
Khi đốt cháy hoàn toàn 9,4 gam hợp chất hữu cơ X chứa C, H,O có CTPT trùng CTDGN . Dẫn sản phẩm thu được qua bình 1 đựng H2SO4 đặc , bình 2 đựng nước vôi trong dư, thấy bình 1 tăng 5,4 gam; bình 2 tăng 26, 4 gam. có 50 gam kết tủa và khối lượng dung dịch giảm 13,6 gam. X có khả năng phản ứng với dung dịch NaOH. Cho 4,7 gam X vào 100ml dung dịch NaOH 1 M . Cô cạn dung dịch thu được m gam rắn. Giá trị của m là?
Có lẽ đoạn đề ". có 50 gam... 13,6 gam." bị thừa bạn nhỉ?
\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\Rightarrow n_H=0,3.2=0,6\left(mol\right)\)
\(n_{CO_2}=\dfrac{26,4}{44}=0,6\left(mol\right)=n_C\)
⇒ mC + mH = 0,6.12 + 0,6.1 = 7,8 (g) < 9,4 (g)
→ X gồm C, H và O.
⇒ mO = 9,4 - 7,8 = 1,6 (g) \(\Rightarrow n_O=\dfrac{1,6}{16}=0,1\left(mol\right)\)
Gọi CTPT của X là CxHyOz.
⇒ x:y:z = 0,6:0,6:0,1 = 6:6:1
Mà: CTPT của X trùng với CTĐGN.
→ X là C6H6O.
- X có pư với NaOH → CTCT: C6H5OH.
\(n_X=\dfrac{4,7}{94}=0,05\left(mol\right)\), \(n_{NaOH}=0,1.1=0,1\left(mol\right)\)
PT: \(C_6H_5OH+NaOH\rightarrow C_6H_5ONa+H_2O\)
Xét tỉ lệ: \(\dfrac{0,05}{1}< \dfrac{0,1}{1}\), ta được NaOH dư.
Chất rắn thu được sau cô cạn gồm: NaOH dư và C6H5ONa.
Theo PT: \(n_{NaOH\left(pư\right)}=n_{C_6H_5ONa}=n_{C_6H_5OH}=0,05\left(mol\right)\)
\(\Rightarrow n_{NaOH\left(dư\right)}=0,1-0,05=0,05\left(mol\right)\)
⇒ m chất rắn = 0,05.40 + 0,05.116 = 7,8 (g)
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 2,3 gam một hợp chất hữu cơ X chỉ thu được CO2, H2O. Sản phẩm cháy cho hấp thụ hết vào bình đựng dung dịch nước vôi trong dư, thấy có 10 gam kết tủa xuất hiện và khối lượng bình đựng dung dịch nước vôi tăng 7,1 gam. Xác định CTPT của X
Ta có :
$n_{CO_2} = n_{CaCO_3} = \dfrac{10}{100} = 0,1(mol)$
$\Rightarrow n_{H_2O} = \dfrac{7,1 - 0,1.44}{18} = 0,15(mol)$
Bảo toàn C, H :
$n_C = n_{CO_2} = 0,1(mol)$
$n_H = 2n_{H_2O} = 0,3(mol)$
$\Rightarrow n_O = \dfrac{2,3 - 0,1.12 - 0,3}{16} = 0,05(mol)$
$n_C : n_H : n_O = 0,1 : 0,3 : 0,05 = 2 : 6 : 1$
Vậy CTPT của X có thể là $C_2H_6O$
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 3,04 gam hợp chất hữu cơ X rồi cho sản phẩm cháy qua bình đựng dung dịch Ca(OH)2 dư thấy có 12 gam kết tủa và khối lượng bình tăng thêm 8,16 gam. Tỉ khối của X so với H2 bằng 38. Xác định CTPT của X
$CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O$
$n_{CO_2} = n_{CaCO_3} = \dfrac{12}{100} = 0,12(mol)$
Ta có : $m_{bình\ tăng} = m_{CO_2} + m_{H_2O}$
$\Rightarrow m_{H_2O} = 8,16 - 0,12.44 = 2,88(gam)$
$\Rightarrow n_{H_2O} = 0,16(mol)$
Bảo toàn nguyên tố C, H :
$n_C = n_{CO_2} = 0,12(mol)$
$n_H = 2n_{H_2O} = 0,32(mol)$
$\Rightarrow m_O = m_X - m_C - m_H = 1,28(gam) \Rightarrow n_O = \dfrac{1,28}{16} = 0,08(mol)$
Ta có :
$n_C : n_H : n_O = 0,12 : 0,32 : 0,08 = 3 : 8 : 2$
Vậy CTPT của X : $(C_3H_8O_2)_n$
$M_X = 76n = M_{H_2}.38 = 76 \Rightarrow n = 1$
Vậy CTPT là $C_3H_8O_2$
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 10,2 gam chất hữu cơ A rồi cho toàn bộ sản phẩm cháy qua bình đựng dung dịch Ca(OH)2 dư thì thấy khối lượng bình tăng 31 gam và trong bình có 50 gam kết tủa. Biết tỉ khối hơi của A so với khí metan (CH4) bằng 6,375. Xác định công thức phân tử của A?
\(n_{CO_2}=n_{CaCO_3}=0,5\left(mol\right)\)
=> \(n_C=0,5\left(mol\right)\)
\(m_{binhtang}=m_{CO_2}+m_{H_2O}=0,5.44+m_{H_2O}=31\)
=> \(m_{H_2O}=9\left(g\right)\Rightarrow n_{H_2O}=0,5\left(mol\right)\)
=> \(n_H=1\left(mol\right)\)
\(M_A=16.6,375=102\)
\(m_O=10,2-0,5.12-0,5.2=3,2\left(g\right)\)
=>\(n_O=0,2\left(mol\right)\)
Gọi CTPT của A là CxHyOz
Ta có : x:y:z = 0,5 :1 : 0,2 =2,5 : 5 :1 = 5 :10: 2
=> CTĐGN của A : (C5H10O2)n
Ta có : \(102.n=102\)
=> n=1
Vậy CTPT của A : C5H10O2
Đúng 2
Bình luận (4)
Đốt cháy hoàn toàn 1 hidrocacbon A ( là chất khí, đkc) rồi dẫn sản phẩm lần lượt qua bình 1 đựng H2SO4 đặc và bình 2 chứa NaOH dư người ta thấy khối lượng bình I tăng 1,8g và khối lượng bình 2 tăng 3,52 gam. XĐ CTPT của A. A. C4H10 B. C3H8 C. C5H12 D. C6H14
Đọc tiếp
Đốt cháy hoàn toàn 1 hidrocacbon A ( là chất khí, đkc) rồi dẫn sản phẩm lần lượt qua bình 1 đựng H2SO4 đặc và bình 2 chứa NaOH dư người ta thấy khối lượng bình I tăng 1,8g và khối lượng bình 2 tăng 3,52 gam. XĐ CTPT của A.
A. C4H10
B. C3H8
C. C5H12
D. C6H14
Đáp án A
Khối lượng bình 1 tăng là khối lượng của H2O => nH2O = 1,8/18 = 0,1 mol
Khối lượng bình 2 tăng là khối lượng của CO2 => nCO2 = 3,52/44 = 0,08 mol
Nhận thấy: nCO2 < nH2O => hidrocacbon là ankan;
Số mol ankan là nankan = 0,1 – 0,08 = 0,02 mol
Phương trình phản ứng:
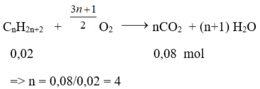
CTPT của A là C4H10
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 6 gam hợp chất hữu cơ A rồi cho sản phẩm thu được qua bình 1 đựng H2SO4 đặc, sau đó qua bình 2 đựng dung dịch Ca(OH)2 dư. Sau phản ứng thấy khối lượng bình tăng thêm 3,6 gam, ở bình 2 có 20 gam kết tủa. a) Hãy xác định công thức phân tử của A b) Viết các công thức cấu tạo có thể có của A, biết A làm quỳ tím chuyển sang màu đỏ.
a, \(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\Rightarrow n_H=0,2.2=0,4\left(mol\right)\)
\(n_{CO_2}=n_{CaCO_3}=\dfrac{20}{100}=0,2\left(mol\right)=n_C\)
⇒ mC + mH = 0,2.12 + 0,4.1 = 2,8 (g) < mA
→ A gồm C, H và O.
⇒ mO = 6 - 2,8 = 3,2 (g) \(\Rightarrow n_O=\dfrac{3,2}{16}=0,2\left(mol\right)\)
Gọi CTPT của A là CxHyOz.
⇒ x:y:z = 0,2:0,4:0,2 = 1:2:1
→ CTPT của A có dạng (CH2O)n
Không biết đề có cho thêm dữ kiện liên quan đến MA không bạn nhỉ?
Đúng 1
Bình luận (0)















