
Những câu hỏi liên quan
Nhỏ từ từ dung dịch HCl 1M vào 100 g dung dịch kiềm m mở (OH)n nồng độ 1,71% để M(OH)n phản ứng hết phân dung 20 ml dung dịch HCl xác định kim loại trong hai Hydioxide biết rằng hóa trị kim loại có thể là HÓA TRỊ I Hoặc II hoặc III
CTHH: \(R\left(OH\right)_n\)
\(n_{HCl}=0,02.1=0,02mol\\ nHCl+R\left(OH\right)_n\rightarrow RCl_n+nH_2O\)
\(0,02\) \(\dfrac{0,02}{n}\)
Ta có: \(m_{ddR\left(OH\right)_n}=100g\)
\(m_{R\left(OH\right)_n}=\dfrac{1,71.100}{100}=1,71g\\ \Leftrightarrow\dfrac{0,2}{n}\cdot(R+17n)=1,71\\ \Leftrightarrow0,02R=1,37n\)
| n | 1 | 2 | 3 |
| R | 68,5 | 137 | 205,5 |
Vậy n = 2 thì R là Ba
Đúng 2
Bình luận (0)
Số mol HCl đã phản ứng là: nHCl = CM(HCl).VHCl = 1.0,02 = 0,02 (mol).
Xét phản ứng: nHCl + M(OH)n → MCln + nH2O
Số mol: 0,02 → 002 over n mol
Khối lượng của M(OH)n đã phản ứng:
Gọi khối lượng nguyên tử M là x. Ta có:
Hay 0,02x = 1,37n
Ta có bảng giá trị:
n
1
2
3
x
68,5
137
205,5
Giá trị phù hợp là n = 2 và x = 137. Kim loại Ba.
Đúng 0
Bình luận (0)
Hòa tan hết 5,4 gam kim loại C trong lượng vừa đủ dung dịch Ba(OH)2. Cho từ từ dung dịch HCl vào dung dịch sau phản ứng thấy có kết tủa, sau đó kết tủa tan vừa hết thì ngừng, thấy đã dùng hết 800 ml dung dịch HCl 1M. Xác định kim loại C trên A. A1 B. Cr C. Be D. Đ/a khác
Đọc tiếp
Hòa tan hết 5,4 gam kim loại C trong lượng vừa đủ dung dịch Ba(OH)2. Cho từ từ dung dịch HCl vào dung dịch sau phản ứng thấy có kết tủa, sau đó kết tủa tan vừa hết thì ngừng, thấy đã dùng hết 800 ml dung dịch HCl 1M. Xác định kim loại C trên
A. A1
B. Cr
C. Be
D. Đ/a khác
Cho m gam kim loại M hoà tan hoàn toàn trong 100 ml dung dịch HCl 0,1M (D = 1,05 g/ml) được dung dịch X có khối lượng là 105,11 gam. Xác định m và M, biết rằng kim loại có hoá trị từ I đến III.
Khối lượng dung dịch HCl :
m dd = V x D = 100 x 1,05 = 105 (gam)
n HCl = 0,1 x 0,1 = 0,01 (mol)
Gọi hoá trị của kim loại M là n
Phương trình hoá học của phản ứng :
2M + 2nHCl → 2 MCl n + n H 2 (1)
Áp dụng định luật bảo toàn khối lượng
m + m HCl = m muối + m H 2
m = 105,11 + 0,01/2 x 2 - 105 = 0,12g
Theo phương trình hóa học (1) :
n M = 0,01/n mol → 0,01/n x M = 0,12 → M = 12n
Kẻ bảng
| n | 1 | 2 | 3 |
| M | 12 | 24 | 36 |
| loại | nhận | loại |
Vậy kim loại M là Mg.
Đúng 1
Bình luận (0)
Hòa tan 4,9 g Cu(OH)2 bằng 150 ml dung dịch HCl 2M. Để trung hòa hết lượng acid dư cần dùng 25 ml dung dịch M(OH)2 22,8% (d=1,3 g/ml). Xác định kim loại M.
\(Cu\left(OH\right)_2+2HCl->CuCl_2+H_2O\\ n_{Cu\left(OH\right)_2}=\dfrac{4,9}{98}=0,05< \dfrac{n_{HCl}}{2}=\dfrac{2.0,15}{2}=0,15\Rightarrow HCl:dư\left(0,05mol\right)\\ M\left(OH\right)_2+2HCl->MCl_2+H_2O\\ Có:0,228.25.1,3.2:\left(M+34\right)=0,05.36,5\\ M=-33\left(loại\right)\)
Vậy không có kim loại M thoả đề
Đúng 1
Bình luận (2)
Cho 100 mL dung dịch AgNO3 vào 50 g dung dịch 1,9% muối chloride của một kim loại M hoá trị II, phản ứng vừa đủ thu được 2,87 g kết tủa AgCl. Biết PTHH của phản ứng là:MgCl2 + 2AgNO3 → M(NO3)2 + 2AgCl (rắn)a) Xác định kim loại M.b) Xác định nồng độ mol của dung dịch AgNO3.
Đọc tiếp
Cho 100 mL dung dịch AgNO3 vào 50 g dung dịch 1,9% muối chloride của một kim loại M hoá trị II, phản ứng vừa đủ thu được 2,87 g kết tủa AgCl. Biết PTHH của phản ứng là:
MgCl2 + 2AgNO3 → M(NO3)2 + 2AgCl (rắn)
a) Xác định kim loại M.
b) Xác định nồng độ mol của dung dịch AgNO3.
Hoà tan hoàn toàn 16.25gam kim loại M(chưa rõ hoá trị) vào dung dịch axit HCL. Khi phản ứng kết thúc thu được 5.6 lít khí hiđrô (ở đktc). a) Xác định kim loại M. b) Tính thể tích dung dịch HCL 0,2M cần dùng để hoà tan hết lượng kim loại này.
a) Gọi Kl cần tìm là X có hóa trị chưa biết là n
2X+ 2nHCl = 2XCln+ nH2
Có nH2=0,25 mol --> nX= 0,5/n mol ---> mX=0,5.MX/n=16,25 --> MX=32,5n
n=1 => MX=32,5( không có Kl nào tm)
n=2 => MX=65( Zn)
b) nHCl= 2nH2=2.0,25=0,5 mol
==> VddHCl cần = 0,5/0,2=2,5 lit
Đúng 0
Bình luận (0)
hòa tan hoàn toàn 7,8 gam kim loại kiềm trong dung dịch hcl 10% sau phản ứng thu được dung dịch x và 2,24 lít khí
a .xác định tên của kim loại trên
b. tìm nồng độ phần trăm của các chất trong dung dịch sau phản ứng biết HCl dùng dư 20% so với lượng phản ứng
Xem chi tiết
Gọi kim loại cần tìm là A
a) PTHH: \(A+H_2O\rightarrow AOH+\dfrac{1}{2}H_2\uparrow\)
\(AOH+HCl\rightarrow ACl+H_2O\)
b) Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\) \(\Rightarrow n_A=0,2mol\)
\(\Rightarrow M_A=\dfrac{7,8}{0,2}=39\) \(\Rightarrow\) Kim loại cần tìm là Kali
b) Ta có: \(\left\{{}\begin{matrix}n_{KCl}=0,2mol\\n_{HCl\left(pư\right)}=0,2mol\Rightarrow n_{HCl\left(dư\right)}=0,2\cdot20\%=0,04\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{KCl}=0,2\cdot74,5=14,9\left(g\right)\\m_{HCl\left(dư\right)}=0,04\cdot36,5=1,46\left(g\right)\end{matrix}\right.\)
Mặt khác: \(m_{H_2}=2\cdot0,1=0,2\left(g\right)\)
\(\Rightarrow m_{dd}=m_K+m_{ddHCl}-m_{H_2}=7,8+\dfrac{0,24\cdot36,5}{10\%}-0,2=95,2\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{KCl}=\dfrac{14,9}{95,2}\cdot100\%\approx15,65\%\\C\%_{HCl\left(dư\right)}=\dfrac{1,46}{95,2}\cdot100\%\approx1,53\%\end{matrix}\right.\)
Đúng 0
Bình luận (0)
Hòa tan hết 6,5475 gam kim loại T trong một lượng vừa đủ dung dịch NaOH 1M. Cho từ từ dung dịch HCl vào dung dịch sau phản ứng thấy có kết tủa, sau đó kết tủa tan vừa hết thì ngừng, thấy đã dùng hết 970 ml dung dịch HCl 1M. Xác định kim loại T. A.Al B.Cr C.Zn D.Be
Đọc tiếp
Hòa tan hết 6,5475 gam kim loại T trong một lượng vừa đủ dung dịch NaOH 1M. Cho từ từ dung dịch HCl vào dung dịch sau phản ứng thấy có kết tủa, sau đó kết tủa tan vừa hết thì ngừng, thấy đã dùng hết 970 ml dung dịch HCl 1M. Xác định kim loại T.
A.Al
B.Cr
C.Zn
D.Be
Có thứ tự các phản ứng xảy ra như sau:
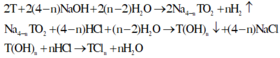
Do đó
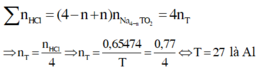
Đáp án A.
Đúng 0
Bình luận (0)
Hòa tan hết 2,6 gam kim loại C trong dung dịch trong lượng vừa đủ dung dịch HCl. Cho từ từ dung dịch NaOH vào dung dịch sau phản ứng thấy có kết tủa, sau đó kết tủa tan vừa hết thì ngừng hẳn, thấy đã dùng hết 160 ml dung dịch NaOH 1M. Xác định kim loại C trên A. A1 B. Cr C. Be D. Đ/a khác
Đọc tiếp
Hòa tan hết 2,6 gam kim loại C trong dung dịch trong lượng vừa đủ dung dịch HCl. Cho từ từ dung dịch NaOH vào dung dịch sau phản ứng thấy có kết tủa, sau đó kết tủa tan vừa hết thì ngừng hẳn, thấy đã dùng hết 160 ml dung dịch NaOH 1M. Xác định kim loại C trên
A. A1
B. Cr
C. Be
D. Đ/a khác
















