Cho biết năng lượng liên kết giảm dần theo thứ tự từ fluorine đến iodine:
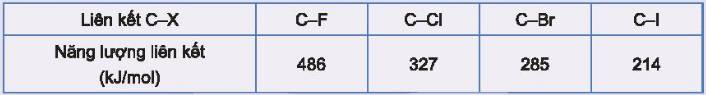
Từ giá trị năng lượng C – X ở trên, hãy so sánh khả năng phân cắt liên kết C – X của các dẫn xuất halogen.
Biết năng lượng liên kết của lưu huỳnh S32, crôm Cr52, urani U238 theo thứ tự lần lượt là 270MeV; 447MeV; 1785MeV. Thứ tự tăng dần về độ bền vững của các hạt nhân trên là:
A. S; U; Cr.
B. U; S; Cr
C. Cr; S; U
D. S; Cr; U.
Biết năng lượng liên kết của lưu huỳnh S 32 , crôm C r 52 , urani U 238 theo thứ tự lần lượt là 270MeV; 447MeV; 1785MeV. Thứ tự tăng dần về độ bền vững của các hạt nhân trên là:
A. S; U; Cr
B. U; S; Cr
C. Cr; S; U
D. S; Cr; U
Biết năng lượng liên kết của lưu huỳnh S32, crôm Cr52, urani U238 theo thứ tự lần lượt là 270MeV; 447MeV; 1785MeV. Thứ tự tăng dần về độ bền vững của các hạt nhân trên là
A. S; U; Cr.
B. U; S; Cr.
C. Cr; S; U.
D. S; Cr; U.
Năng lượng liên kết của liên kết C – C (trong phân tử ethane) là 368 kJ mol-1 và năng lượng liên kết của liên kết C = C (trong phân tử ethene) là 636 kJ mol-1. Hãy cho biết liên kết nào (σ hay π) dễ bị bẻ gãy hơn khi phân tử tham gia phản ứng.
Liên kết đơn C – C có gồm 1 liên kết σ có năng lượng là 368 kJ mol-1.
Liên kết đôi C = C gồm 1 liên kết σ và liên kết π có năng lượng là 636 kJ mol-1.
=> Năng lượng của liên kết π là: 636 – 368 = 268 (kJ mol-1)
Vì năng lượng của liên kết σ (368 kJ mol-1) lớn hơn năng của liên kết π (268 kJ mol-1) nên khi phân tử tham gia phản ứng, liên kết π dễ bị bẻ gãy hơn.
Sử dụng bảng giá trị năng lượng liên kết ở Phụ lục 2.
a) Hãy tính tổng năng lượng liên kết trong mỗi phân tử H2S và H2O.
b) Nhiệt độ để bắt đầu phá vỡ liên kết (nhiệt độ phân hủy) trong hai chất trên ứng với một trong hai nhiệt độ sau: 400oC hoặc 1000oC. Em hãy dự đoán nhiệt độ phân hủy của chất nào cao hơn. Vì sao?
a)
- Phân tử H2S:
+ Năng lượng liên kết của S – H là: 368 kJ mol-1.
+ Vì có 2 liên kết S – H
⟹ Tổng năng lượng liên kết trong phân tử H2S là: 368.2 = 736 (kJ mol-1)
- Phân tử H2O:
+ Năng lượng liên kết của O – H là: 464 kJ mol-1.
+ Vì có 2 liên kết O – H
⟹ Tổng năng lượng liên kết trong phân tử H2O là: 464.2 = 928 (kJ mol-1)
b)
- Ta thấy năng lượng liên kết của H2S là 38 kJ mol-1 ; của H2O là 928 kJ mol-1.
⟹ Năng lượng liên kết của H2S < H2O.
⟹ Liên kết của H2O bền hơn H2S.
⟹ Nhiệt độ phân hủy của H2O > H2S.
Các hạt nhân H 2 1 ; triti H 1 3 ; heli H 2 4 e có năng lượng liên kết lần lượt là 2,22 MeV; 8,49 MeV và 28,16 MeV. Các hạt nhân trên được sắp xếp theo thứ tự giảm dần về độ bền vững của hạt nhân là
A. ![]()
B. ![]()
C. ![]()
D. ![]()
Các hạt nhân đơtêri H 1 2 , triti H 1 3 , heli H 2 4 e có năng lượng liên kết lần lượt là 2,22 MeV, 8,49 MeV, 28,16 MeV. Các hạt nhân trên được sắp xếp theo thứ tự giảm dần về độ bền vững của hạt nhân là
A. H 1 2 , H 1 3 , H 2 4 e .
B. H 1 2 , H 2 4 e , H 1 3 .
C. H 2 4 e , H 1 3 , H 1 2 .
D. H 1 3 , H 2 4 e , H 1 2 .
Các hạt nhân đơteri![]() ; triti
; triti ![]() và heli
và heli ![]() có năng lượng liên kết lần lượt là 2,22 MeV; 8,49 MeV và 28,16 MeV. Các hạt nhân trên được sắp xếp theo thứ tự giảm dần về độ bền vững của hạt nhân là
có năng lượng liên kết lần lượt là 2,22 MeV; 8,49 MeV và 28,16 MeV. Các hạt nhân trên được sắp xếp theo thứ tự giảm dần về độ bền vững của hạt nhân là
A. ![]()
B. ![]()
C. ![]()
D. ![]()
+ Độ bền vững của hạt nhân được xét dựa trên năng lượng liên kết riêng: ![]()
+ ![]() có Wlkr = 1,11 MeV;
có Wlkr = 1,11 MeV; ![]() có Wlkr = 2,83 MeV;
có Wlkr = 2,83 MeV; ![]() có Wlkr = 7,04 MeV.
có Wlkr = 7,04 MeV.
→ Độ bền vững hạt nhân sắp xếp theo thứ tự giảm dần là: ![]()
Đáp án C
Tra cứu các giá trị năng lượng liên kết ở phụ lục 2
a) Hãy tính biến thiên enthalpy chuẩn ∆rH0298 của 2 phản ứng dưới đây:
F2(g) + H2(g) → 2HF (g)
O2(g) + 2H2(g) → 2H2O(g)
b) Ở hai phản ứng trên, fluorine và oxygen đều đóng vai trò là chất oxi hóa. Dựa vào giá trị ∆rH0298, cho biết phản ứng oxi hóa – khử nào thuận lợi hơn.
a)
- Xét phản ứng: F2(g) + H2(g) → 2HF (g)
+ Ta có: ∆rH0298 = Eb(F2) + Eb(H2) – 2xEb(HF) = 159 + 436 – 2x565 = -535 (kJ/mol)
- Xét phản ứng: O2(g) + 2H2(g) → 2H2O(g)
+ Ta có: ∆rH0298 = Eb(O2) + 2xEb(H2) – 2x2xEb(OH) = 142 + 2x436 – 2x2x464 = -842 (kJ/mol)
b)
Giá trị biến thiên enthalpy của phản ứng (2) âm hơn giá trị biến thiên enthalpy của phản ứng (1)
=> Phản ứng oxi hóa – khử (2) diễn ra thuận lợi hơn
a) Phương trình F2(g) + H2(g) → 2HF(g)
Δ𝑟𝐻0298 = -535 kJ
Phương trình: O2(g) + 2H2(g) → 2H2O (g)
Δ𝑟𝐻0298 = -842 kJ
b ) Phản ứng của oxygen thuận lợi hơn