Biến thiên enthalpy chuẩn của phản ứng tổng hợp ammonia từ nitrogen và hydrogen có giá trị âm nhưng vì sao quá trình Haber lại chọn nhiệt độ phản ứng khá cao, vào khoảng 400 °C – 600 °C?

Những câu hỏi liên quan
Ở 472 °C, hằng số cân bằng của phản ứng tổng hợp ammonia từ nitrogen và hydrogen theo quá trình Haber là Kc 0,105. Giả sử, kết quả phân tích cho thấy tại thời điểm cân bằng, nồng độ của nitrogen và hydrogen trong buồng phản ứng lần lượt là 0,0201 M và 0,0602 M.a) Hãy tính nồng độ mol của ammonia có trong buồng phản ứng tại thời điểm cân bằng.b) Làm thế nào để tách được ammonia ra khỏi hỗn hợp?
Đọc tiếp
Ở 472 °C, hằng số cân bằng của phản ứng tổng hợp ammonia từ nitrogen và hydrogen theo quá trình Haber là Kc = 0,105. Giả sử, kết quả phân tích cho thấy tại thời điểm cân bằng, nồng độ của nitrogen và hydrogen trong buồng phản ứng lần lượt là 0,0201 M và 0,0602 M.
a) Hãy tính nồng độ mol của ammonia có trong buồng phản ứng tại thời điểm cân bằng.
b) Làm thế nào để tách được ammonia ra khỏi hỗn hợp?
Quá trình lên men rượu vang xảy ra phản ứng hóa học sauC6H12O6(s) ---- 2C2H5OH(1)+2CO2(g)a. Tính biến thiên enthalpy chuẩn của phản ứng theo nhiệt tạo thành chuẩn của các chất (biết nhiệt tạo thành chuẩn của C6H12O6(s) C2H5OH(l); CO2(g) có giá trị lần lượt là –1274kJ/mol: 277,69 kJ/mol 393,51kJ/molb, Tính lượng nhiệt tòa ra hay thu vào khi lên men 3 kg nhỏ (chứa khoảng 7% đường glucose) ở điều kiện chuẩn
Đọc tiếp
Quá trình lên men rượu vang xảy ra phản ứng hóa học sau
C6H12O6(s) ----> 2C2H5OH(1)+2CO2(g)
a. Tính biến thiên enthalpy chuẩn của phản ứng theo nhiệt tạo thành chuẩn của các chất (biết nhiệt tạo thành chuẩn của C6H12O6(s) C2H5OH(l); CO2(g) có giá trị lần lượt là –1274kJ/mol: 277,69 kJ/mol 393,51kJ/mol
b, Tính lượng nhiệt tòa ra hay thu vào khi lên men 3 kg nhỏ (chứa khoảng 7% đường glucose) ở điều kiện chuẩn
Câu 30: Xét quá trình đốt cháy khí propane C3H8(g):
C3H8(g) + 5O2(g) 3CO2(g) + 4H2O(g)
a) Tính biến thiên enthalpy chuẩn của phản ứng dựa vào bảng nhiệt tạo thành của hợp chất và dựa vào dựa vào bảng năng lượng liên kết.
Biết nhiệt tạo thành của C3H8(g); CO2(g) và H2O(g) lần lượt là : 105,00; 393,50 và 241,82 kJ/mol.
Biết EC-H 418 kJ/mol; EC-C 346 kJ/mol; EOO 494 kJ/mol; ECO 732 kJ/mol và EO-H 459 kJ/mol.
b) So sánh hai giá trị đó và nếu có sự khác biệt, hãy giải thích tại sao lại...
Đọc tiếp
Câu 30: Xét quá trình đốt cháy khí propane C3H8(g):
C3H8(g) + 5O2(g) 3CO2(g) + 4H2O(g)
a) Tính biến thiên enthalpy chuẩn của phản ứng dựa vào bảng nhiệt tạo thành của hợp chất và dựa vào dựa vào bảng năng lượng liên kết.
Biết nhiệt tạo thành của C3H8(g); CO2(g) và H2O(g) lần lượt là : 105,00; 393,50 và 241,82 kJ/mol.
Biết EC-H = 418 kJ/mol; EC-C = 346 kJ/mol; EO=O = 494 kJ/mol; EC=O = 732 kJ/mol và EO-H = 459 kJ/mol.
b) So sánh hai giá trị đó và nếu có sự khác biệt, hãy giải thích tại sao lại có sự khác biệt đó ?
Dựa vào giá trị biến thiên enthalpy chuẩn của phản ứng, hay cho biết phản ứng giữa nitrogen với hydrogen hay với oxygen diễn ra thuận lợi hơn.
Phản ứng giữa nitrogen với hydrogen có enthalpy: -91,8kJ
Phản ứng giữa nitrogen với oxygen có enthalpy: 182,6 kJ
=> phản ứng giữa nitrogen với hydrogen thuận lợi hơn. (do có enthalpy nhỏ hơn)
Đúng 0
Bình luận (0)
- Vận dụng được kiến thức về cân bằng hoá học, tốc độ phản ứng, enthalpy cho phản ứng tổng hợp ammonia trong quá trình Haber – Bosch.
- Nhận biết được ion ammonium trong phân đạm.
- Trong công nghiệp, quá trình sản xuất ammonia thường được thực hiện ở nhiệt độ 400 oC – 450 oC, áp suất 150 – 200 bar, xúc tác Fe.
N2(g) + 3H2(g) ⇌ 2NH3(g) ΔrHo = -91,8 kJ
+ Về áp suất: người ta đã tăng áp suất của hệ phản ứng trong buồng tổng hợp lên đến gần 200 bar. Đó là do khi tăng áp suất, cân bằng chuyển dịch theo chiều làm giảm áp suất của hệ - tức chiều giảm số mol khí, hay chiều tạo ammonia (chiều thuận).
+ Về nhiệt độ: Vì phản ứng thuận toả nhiệt (ΔrHo = -91,8 kJ < 0) nên cần phải giảm nhiệt độ để cân bằng chuyển dịch theo chiều thuận, tạo ammonia. Tuy nhiên, khi thực hiện phản ứng ở nhiệt độ quá thấp thì tốc độ của phản ứng nhỏ, phản ứng diễn ra chậm. Thực tế, người ta đã chọn nhiệt độ phù hợp, khoảng 400 oC - 450 oC.
+ Việc sử dụng xúc tác là bột sắt trong quá trình Haber có tác dụng làm cho phản ứng nhanh đạt tới trạng thái cân bằng.
- Nhận biết ion ammonium trong phân đạm: Khi đun nóng hỗn hợp phân đạm chứa muối ammonium với dung dịch kiềm sinh ra khí ammonia có mùi khai.
Phương trình hoá học minh hoạ:
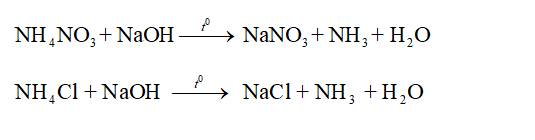
Đúng 0
Bình luận (0)
Biến thiên enthalpy chuẩn của một phản ứng hóa học A. tùy thuộc nhiệt độ xảy ra phản ứng B. tùy thuộc vào đường đi từ chất đầu đến sản phẩm C. không phụ thuộc vào bản chất và trạng thái của các chất trong phản ứng.D. phụ thuộc vào cách viết hệ số tỉ lượng của phản ứng
Đọc tiếp
Biến thiên enthalpy chuẩn của một phản ứng hóa học
A. tùy thuộc nhiệt độ xảy ra phản ứng
B. tùy thuộc vào đường đi từ chất đầu đến sản phẩm
C. không phụ thuộc vào bản chất và trạng thái của các chất trong phản ứng.
D. phụ thuộc vào cách viết hệ số tỉ lượng của phản ứng
Biến thiên enthalpy chuẩn của một phản ứng hóa học
A. tùy thuộc nhiệt độ xảy ra phản ứng
B. tùy thuộc vào đường đi từ chất đầu đến sản phẩm
C. không phụ thuộc vào bản chất và trạng thái của các chất trong phản ứng.
D. phụ thuộc vào cách viết hệ số tỉ lượng của phản ứng
Đúng 0
Bình luận (0)
Trong công nghiệp, đơn chất nitrogen kết hợp với hydrogen tạo thành ammonia là một hợp chất quan trọng trong sản xuất phân bón, hoá chất.
Tại sao phản ứng trên cần thực hiện ở nhiệt độ cao? Đơn chất nitrogen đóng vai trò gì trong phản ứng đó?
- Phản ứng giữa nitrogen và hydrogen cần được thực hiện ở nhiệt độ cao do liên kết ba giữa 2 nguyên tử N trong phân tử nitrogen có năng lượng liên kết rất lớn (945 kJ/ mol) nên khó bị phá vỡ.
- Phương trình hoá học:
\({\mathop {\rm{N}}\limits^{\rm{0}} _{\rm{2}}}{\rm{(g) + 3}}{{\rm{H}}_{\rm{2}}}\)⇌ \({\rm{2}}\mathop {\rm{N}}\limits^{{\rm{ - 3}}} {{\rm{H}}_{\rm{3}}}\)
Số oxi hoá của nitrogen giảm từ 0 xuống -3 nên trong phản ứng này đơn chất nitrogen đóng vai trò là chất oxi hoá.
Đúng 0
Bình luận (0)
c) Tính biến thiên enthanpy của phản ứng tạo thành ammonia (sử dụng năng lượng liên kết).
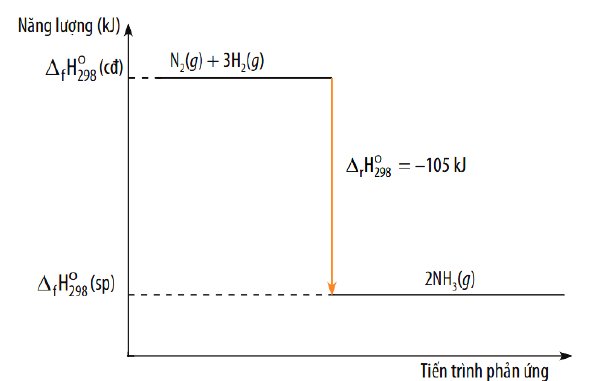
Cho biết phản ứng thu nhiệt hay toả nhiệt và vẽ sơ đồ biểu diễn biến thiên enthalpy của phản
ứng 3H2 (g) + N2 (g) → 2NH3 (g)
Liên kết Eb (kJ/ mol)
H – N 386
H – H 436
N ≡ N 945
\(\Delta_rH^{^{ }o}_{298}=3\cdot436+945-2\left(3\cdot386\right)=-63kJ\cdot mol^{-1}\)
Sơ đồ:
Đúng 1
Bình luận (0)
Trong các phản ứng hoá học, có một loại phản ứng trong đó các chất sản phẩm có khả năng phản ứng để tạo thành các chất đầu. Do vậy, phản ứng xảy ra không hoàn toàn và thường có hiệu suất không cao. Phản ứng tổng hợp ammonia từ nitrogen và hydrogen thuộc loại phản ứng này. Các phản ứng này được gọi là phản ứng gì? Để tăng hiệu suất của chúng, cần điều chỉnh những điều kiện phản ứng như nhiệt độ, áp suất, nồng độ,... như thế nào?
Đọc tiếp
Trong các phản ứng hoá học, có một loại phản ứng trong đó các chất sản phẩm có khả năng phản ứng để tạo thành các chất đầu. Do vậy, phản ứng xảy ra không hoàn toàn và thường có hiệu suất không cao. Phản ứng tổng hợp ammonia từ nitrogen và hydrogen thuộc loại phản ứng này. Các phản ứng này được gọi là phản ứng gì? Để tăng hiệu suất của chúng, cần điều chỉnh những điều kiện phản ứng như nhiệt độ, áp suất, nồng độ,... như thế nào?
- Trong các phản ứng hoá học, loại phản ứng trong đó các chất sản phẩm có khả năng phản ứng để tạo thành các chất đầu được gọi là phản ứng thuận nghịch.
- Để tăng hiệu suất của chúng, cần điều chỉnh những điều kiện phản ứng như nhiệt độ, áp suất, nồng độ,... dựa theo nguyên lí Le Chatelier: “Một phản ứng thuận nghịch đang ở trạng thái cân bằng khi chịu một tác động bên ngoài như biến đổi nồng độ, áp suất, nhiệt độ thì cân bằng sẽ chuyển dịch theo chiều làm giảm tác động đó”.
Đúng 0
Bình luận (0)












